
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Теоретическая часть. При анализе результатов по давлению насыщенных паров летучего растворителя над растворами малолетучих веществ Рауль обнаружил (1887 г) следующую
При анализе результатов по давлению насыщенных паров летучего растворителя над растворами малолетучих веществ Рауль обнаружил (1887 г) следующую закономерность: при постоянной температуре давление пара растворителя над раствором пропорционально его молярной концентрации в растворе.
 (III.1.1)
(III.1.1)
где  и pi — давление пара растворителя над чистым растворителем и над раствором соответственно, xi — молярная доля растворителя в растворе.
и pi — давление пара растворителя над чистым растворителем и над раствором соответственно, xi — молярная доля растворителя в растворе.
Это соотношение можно получить исходя из того, что при равновесии химический потенциал вещества одинаков во всех сосуществующих фазах. В условиях равновесия “раствор – пар”, химический потенциал компонента жидкого раствора  будет равен химическому потенциалу пара этого компонента
будет равен химическому потенциалу пара этого компонента  над раствором:
над раствором:
 (III.1.2)
(III.1.2)
С учетом зависимости химического потенциала от парциального давления пара i‑ ого компонента для идеальных газов
 (III.1.3)
(III.1.3)
и выражения (II.7) равенство (III.1.2) преобразуется в
 (III.1.4)
(III.1.4)
Давление пара вещества над чистым растворителем равно pi °, поэтому при xi = 1 (чистое вещество) уравнение (III.1.4) переходит в

 (III.1.5)
(III.1.5)
В свою очередь, подстановка (III.1.5) в (III.1.4) дает закона Рауля (III.1.1).
Уравнение (III.1.1) можно записать и в другом виде. Для бинарного раствора
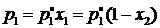
или
 (III.1.6)
(III.1.6)
т.е, согласно закону Рауля относительное понижение давления пара над раствором равно молярной доле введенной примеси. Заметим, что выражение (III.1.6) более наглядно, чем (III.1.1) показывает, что рассматриваемый закон выражает коллигативные свойства растворов.
Закон Рауля может быть применен и случаю, когда оба (или более) компонента раствора являются летучими. В этом случае соотношение (III.1.1) следует применять к расчету величины парциального давления пара для каждого компонента в отдельности. Для нахождения величины общего давления пара, рассчитанные значения парциальных давлений пара суммируются (закон Дальтона).
Не нашли, что искали? Воспользуйтесь поиском: