
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Свободная энергия термодинамической системы как компромисс между энтропией и внутренней энергией
В разделе 1.1. (см. пример – «система двух шаров») показано, что наиболее вероятное (естественное) состояние физической системы соответствует максимуму статистической энтропии, т.е. абсолютно неупорядоченному расположению элементов. В этой связи возникает вопрос, почему же в природе зачастую наблюдаются высоко упорядоченные атомно-кристаллические структуры, в виде минералов естественного происхождения. Факт появления этих структур при естественных механизмах эволюции физических систем (т.е. без необходимости использования специальных технологических приемов) в корне противоречит универсальному природному принципу - установлению максимальной энтропии в процессе стремления термодинамической системы к своему равновесному состоянию.
Ввиду важности этого вопроса (парадокса) для конструкторско-технологической практики создания микро- и наноразмерных устройств, рассмотрим подробнее процесс образования кристаллических структур с позиции традиционных представлений и методов анализа равновесной термодинамики.
В общем случае, при рассмотрении процесса эволюции термодинамической системы к своему равновесному состоянию, необходимо учитывать оба (оговоренных в разделе 1) принципа экстремума: «минимум внутренней энергии системы» и «максимум энтропии системы». Отметим, что эти принципы преследуют противоположные цели и поэтому противоречат друг другу:
· принцип «минимума внутренней энергии системы» способствует протеканию процесса пространственно-упорядоченной расстановке индивидуальных атомов, результатом которого является образование в веществе кристаллической структуры;
· принцип «максимума энтропии системы» способствует протеканию процесса разупорядочения кристаллической структуры в веществе, результатом которого является образование в кристаллической структуре дефектов атомного масштаба, и в конечном итоге, полное разрушение кристаллической структуры (например: переход в аморфную фазу вещества).
Одновременное удовлетворение указанных физических принципов (хотя бы в частичном объеме) предполагает выполнение некого компромиссного условия, учитывающего взаимосвязь этих физических принципов в термодинамических системах. Это компромиссное условие может быть сформировано на основе использования термодинамического потенциала - «свободная энергия системы» [10]:
 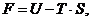
| (1.15) |
где: 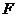 - свободная энергия термодинамической системы;
- свободная энергия термодинамической системы;  - внутренняя энергия системы (сумма кинетической и потенциальной энергии взаимодействия всех микрочастиц);
- внутренняя энергия системы (сумма кинетической и потенциальной энергии взаимодействия всех микрочастиц); 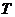 - температура в градусах Кельвина;
- температура в градусах Кельвина;  - энтропия системы.
- энтропия системы.
Для дальнейшего рассмотрения ключевым моментом является тот факт, что в состоянии термодинамического равновесия свободная энергия системы 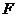 имеет минимальное значение. В общем случае термодинамический потенциал
имеет минимальное значение. В общем случае термодинамический потенциал 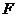 может являться функцией различных переменных. Однако, в свете рассматриваемого вопроса, представляет интерес не полное смысловое наполнение термодинамического потенциала
может являться функцией различных переменных. Однако, в свете рассматриваемого вопроса, представляет интерес не полное смысловое наполнение термодинамического потенциала 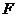 , а только та его часть, которая непосредственно связана с концентрацией дефектов атомного масштаба (вакансии, атомы внедрения, инородные атомы). Для выделения только этой составляющей термодинамического потенциала
, а только та его часть, которая непосредственно связана с концентрацией дефектов атомного масштаба (вакансии, атомы внедрения, инородные атомы). Для выделения только этой составляющей термодинамического потенциала 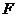 , выражение (1.15) целесообразно представить в виде:
, выражение (1.15) целесообразно представить в виде:
 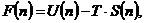
| (1.16) |
где 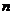 - концентрация дефектов атомного масштаба в кристаллической структуре.
- концентрация дефектов атомного масштаба в кристаллической структуре.
Далее, не умаляя общности рассмотрения, а в целях упрощения анализа, будет принято, что в кристаллической структуре наблюдаются атомные дефекты только одного типа (например: вакансии).
Не нашли, что искали? Воспользуйтесь поиском: