
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Элемент № 7 ( – азот).
Задача № 1 (Строение многоэлектронных атомов).
1. Описать состав атома: число протонов, нейтронов, электронов:

 – равно заряду ядра атома;
– равно заряду ядра атома;
 – равно числу протонов;
– равно числу протонов;
 .
.
2. Записать электронную формулу атома, указать внешний электронный уровень и орбиталь, на которую идет последний электрон. Сделать вывод о типе элемента. Изобразить электронно-структурную формулу валентного уровня:

Элемент семейства  , так как последний электрон идет на
, так как последний электрон идет на  -подуровень.
-подуровень.

3. Используя электронную формулу, определить положение элемента в периодической системе Д.И. Менделеева:
Элемент находится:
2 период – т.к. максимальное значение главного квантового числа равно 2;
V группа – т.к. число валентных электронов равно 5;
главная подгруппа – т.к. последний электрон идет на  -подуровень.
-подуровень.
4. Определить допустимые значения степеней окисления. Указать наиболее устойчивые степени окисления для данного элемента. Привести примеры соединений данного элемента в устойчивых степенях окисления:

Устойчивость степеней окисления объясняется стабильностью электронной конфигурации атома в этих состояниях. В степени окисления  атом имеет полностью пустой 2 уровень:
атом имеет полностью пустой 2 уровень:  . В степени окисления
. В степени окисления  , орбитали 2-го уровня полностью заполнены (устойчивая 8-электронная оболочка благородного газа):
, орбитали 2-го уровня полностью заполнены (устойчивая 8-электронная оболочка благородного газа):  .
.
 ;
;

5. Исходя из электронной формулы определить характер свойств простого вещества. Охарактеризовать физические и химические свойства простого вещества:
Азот образует простое вещество – неметалл, т.к. атом на внешнем энергетическом уровне имеет 5 электронов и не имеет вакантных орбиталей.
Физические свойства: Азот  - газ без цвета и запаха, в твердом состоянии белый,
- газ без цвета и запаха, в твердом состоянии белый,  . Плохо растворяется в воде. Основной компонент воздуха
. Плохо растворяется в воде. Основной компонент воздуха 
Химические свойства: химически азот весьма инертен, вступает в реакции при высокой температуре или в электрическом разряде:




При комнатной температуре реагирует только с литием:

6. Записать формулы и привести уравнения реакций, характеризующих химические свойства характеристических соединений: высшего оксида и гидроксида:
Высший оксид –  – кислотный.
– кислотный.
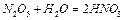


Высший гидроксид –  – кислота.
– кислота.


Не нашли, что искали? Воспользуйтесь поиском: