
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Зависимость скорости ферментативной реакции от концентрации субстрата
Зависимость скорости ферментативной реакции от концентрации субстрата описывается уравнением Михаэлиса – Ментон.
Простейшая кинетическая схема, для которой справедливо уравнение Михаэлиса:
k1 k2
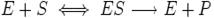
k -1
ЕS –субстратно-ферментный комплекс, это неустойчивое короткоживущее промежуточное соединение Применяем метод стационарных концентраций – скорость образования и распада промежуточных соединений равны
k1 [E] [S] = k2 [ES] +k3[ES]
перенесем в одну сторону:
k1 [E] [S] – k2 [ES] –k3[ES] = 0
[E] = [Е]о – [ES]
[Е]о-начальная концентрация фермента.
k1 [E]о [S] – k1 [ES] [S] – k2 [ES] –k3[ES] = 0
[ES] = k1 [E]о[S]/(k1[S] + k2 +k3)
V= k3[ES] = k1k3[E]о[S]/(k1[S] + k2+k3)
Разделим на k1 и подставим
(k2+k3)/ k1 = КМ
Vмах=Eо[S]
Получим
V= Vмах [S]/([S ] + КМ)
Проанализируем.
При низких концентрациях субстрата [S ]<<КМ, пренебрегаем в знаменателе значением [S ]. Получаем V=Vмах[S]/( КМ), Скорость растет линейно с ростом концентрации субстрата.
При высоких концентрациях субстрата если [S ] >> КМ, то пренебрегаем в знаменателе КМ и получим V= Vмах [S]/[S ], V= Vмах.
Таким образом,-при низких концентрациях субстрата скорость возрастает линейно, по мере насыщения фермента рост активности замедляется, а когда все молекулы фермента насыщаются субстратом, активность становится постоянной и равна vmax.
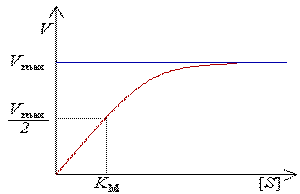
Если [S ]= КМ, то V= Vмах [S]/([S ] + [S ]), V= Vмах/2, таким образом, КМ численно равна такой концентрации субстрата, при которой скорость равна половине максимальной.
Константа Михаэлиса – численно равна концентрации субстрата, при которой скорость равна половине максимальной. Константа Михаэлиса отражает сродство фермента к субстрату. Чем меньше константа Михаэлиса, тем больше сродство фермента к субстрату.
Скорость, с которой вещества реагируют друг с другом, зависит и от их концентрации. Таким образом, изменение количества хотя бы одного из субстратов изменяет скорость реакции.
Для того, чтобы избежать влияния диффузии на скорость процесса в клетке повышены концентрации субстратов.
Не нашли, что искали? Воспользуйтесь поиском: