
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Примеры решения задач. Пример 1. Как изменится скорость реакции 2NО(г) + О2(г) ⇄ 2NO2(г), если одновременно концентрацию NО увеличить в 2 раза
Пример 1. Как изменится скорость реакции 2NО(г) + О2(г) ⇄ 2NO2(г) , если
одновременно концентрацию NО увеличить в 2 раза, а концентрацию О2 уменьшить в 8 раз?
Р е ш е н и е. 1) Зависимость скорости химической реакции от концентрации реагирующих веществ выражается законом действующих масс, поэтому записываем математическое выражение этого закона для данной реакции в начальный момент времени: 
Согласно условию концентрацию NO увеличили в 2 раза, т.е. С'NO=2С NO, а концентрацию О2 уменьшили в 8 раз, т.е. С'o2 = Сo2 /8.
2) Записываем выражение для скорости реакции в конечный момент времени: υ' = k × (С' NO)2 × С'o2 или 
3)  Определяем, как изменяется скорость реакции. Для этого рассматриваем отношение
Определяем, как изменяется скорость реакции. Для этого рассматриваем отношение  = 1/2
= 1/2
Ответ: при одновременном увеличении концентрации NО в 2 раза и уменьшении концентрации О2 в 8 раз скорость реакции уменьшается в 2 раза.
Пример 2. Определите, во сколько раз изменятся скорости прямой и обратной реакций в системе 2SO2 (г) + О2 (г) ⇄ 2SО3 (г), если объем газовой смеси уменьшить в 3 раза. Каково направление смещения равновесия в этой системе?
Р е ш е н и е. 1) Записываем выражения для скоростей прямой и обратной реакций, используя закон действующих масс:  ,
, 
2) Рассматриваем, что происходит в реакционной системе при уменьшении ее объема. Уменьшение объема гомогенной системы в 3 раза приводит к увеличению концентрации каждого из реагирующих веществ также в 3 раза, т.е. математически это записываем в виде: С'so2 = 3С so2, С'о2 = 3Сo2 и С'so3 = 3С so3.
3) Записываем выражение для скоростей прямой и обратной реакций после изменения объема системы:
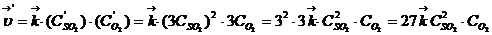
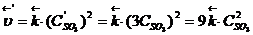
4) Определяем, во сколько раз изменяются скорости прямой и обратной реакций:  ;
; 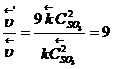
Таким образом, при уменьшении объема газовой смеси в 3 раза скорость прямой реакции увеличится в 27 раз, а скорость обратной реакции – в 9 раз.
5) Устанавливаем направление смещения равновесия в этой системе. В связи с тем, что скорость прямой реакции увеличилась в 27 раз, а обратной – только в 9 раз, равновесие сместится в направлении протекания прямой реакции, т.е. в сторону образования SO3.
Пример 3. Рассчитайте температурный коэффициент скорости химической реакции, если известно, что константа скорости этой реакции при 140°С равна 5,5 × 10-4, а при 185°С – 9,2 × 10-3.
Дано: Т1 =140° С, k1 =5,5 × 10 -4; Т2= 185°С, k2 = 9,2∙× 10-3. Найти γ.
Р е ш е н и е. 1) Зависимость скорости химической реакции от температуры описывается правилом Вант-Гоффа в форме: 
Но для проведения расчетов это уравнение необходимо прологарифмировать, т.е. 


2) Рассчитываем температурный коэффициент скорости этой реакции.
а) вычисляем температуру по абсолютной шкале:
T1 = 140 + 273 = 413 К, Т2 = 185 + 273 = 458 К;
б) рассчитаем численное значение γ:
 , lg 16,7 = 4,5 lgγ
, lg 16,7 = 4,5 lgγ
отсюда  , т.е. lg γ = 0,27, и тогда γ = 1,87.
, т.е. lg γ = 0,27, и тогда γ = 1,87.
Ответ: температурный коэффициент этой реакции равен 1,87.
Пример 4. При синтезе аммиака N2 + ЗН2 ⇄ 2NНз равновесие установилось  при следующих концентрациях реагирующих веществ (моль/л) [ N2 ] = 4; [ H2 ] = 2 и [ NH3 ] = 6. Рассчитайте константу равновесия и исходные концентрации Н2 и N2.
при следующих концентрациях реагирующих веществ (моль/л) [ N2 ] = 4; [ H2 ] = 2 и [ NH3 ] = 6. Рассчитайте константу равновесия и исходные концентрации Н2 и N2.
Дано: [ Н2 ]=2 моль/л, [ N2 ] = 4 моль/л, [ NH3 ] = 6 моль/л. Найти Кс, Сисх (Н2), Cиcx (N2).
Р е ш е н и е. 1) Записываем выражение для константы равновесия в этой системе и рассчитываем ее значение: 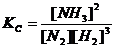 ;
; 


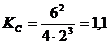
2) Определяем исходные концентрации Н2 и N2.
Для обратимых реакций ни одно из реагирующих веществ не расходуется полностью. Поэтому исходная концентрация вещества А складывается из равновесной концентрации этого вещества [А] и концентрации этого вещества, которая была израсходована на реакцию к моменту установления равновесия (условно обозначим ее X (А). Таким образом, выражение для исходной концентрации вещества А может быть представлено в виде: Сисх(А) = [А] + Х(А).
а) Для определения Сисх(N2) и Сисх(Н2) обращаемся к уравнению реакции, согласно которому на образование 2 моль NH3 требуется 1 моль N2 и 3 моль Н2. Но поскольку равновесная концентрация NH3 равна 6 моль/л, то при этом было израсходовано 6/2 = 3 моль N2 и 3×(6 / 2) = 9 моль Н2.
б) Рассчитаем Сисх(N2) и Сисх(Н2):
Сисх(Н2) = [Н2] + Х(Н2) = 2 + 9 = 11 моль/л,
Cисх(N2) = [N2] + X(N2) = 4 + 3 = 7 моль/л.
Ответ: константа равновесия реакции равна 1,1. Исходные концентрации Н2 и N2 составляют 11 моль/л и 7 моль/л соответственно.
Пример 5. Установите направление смещения равновесия в системе
2Н2О(г)+ 2О2(г) ⇄ 2Н2О2 (г), ∆ Н = – 483,7 кДж
при понижении температуры и уменьшении общего давления.
Р е ш е н и е. Влияние внешнего воздействия на состояние химического равновесия в системах, в которых протекают обратимые реакции, оценивается с помощью принципа Ле Шателье-Брауна.
1) Рассматриваем влияние температуры на состояние равновесия в данной системе. Термохимическое уравнение реакции показывает, что ∆Н < 0, следовательно, прямая реакция экзотермическая. При понижении температуры согласно принципу Ле Шателье-Брауна система будет стремиться ослабить внешнее воздействие (т.е. повысить Т), а это возможно за счет реакции, протекающей с выделением теплоты, т.е. экзотермической реакции. Следовательно, понижение температуры приведет к смещению равновесия в направлении протекания прямой реакции.
2) Оцениваем влияние изменения давления на состояние равновесия в данной системе. Из уравнения реакции видно, что прямая реакция сопровождается уменьшением объема системы 2V (Н2О) + 2V (О2) ≠ 2V (Н2О2), т.е. ∆V ≠ 0. Поэтому общее давление (Робщ) будет влиять на состояние равновесия в данной системе. Уменьшение Робщ согласно принципу Ле Шателье-Брауна вызовет противодействие системы (увеличение Робщ) за счет смещения равновесия в сторону протекания реакции, сопровождающейся увеличением Робщ, т.е. в сторону обратной реакции. Действительно, обратная реакция приводит к увеличению числа моль газообразных веществ в системе, а это значит, что при протекании обратной реакции Робщ в системе увеличивается.
1.7. Электролитическая диссоциация. Реакции ионного обмена
Электролитическая диссоциация – это процесс распада молекул электролита на ионы под действием полярных молекул растворителя.
Электролиты – это вещества, расплавы или водные растворы которых проводят электрический ток. К ним относятся растворы кислот, расплавы и растворы щелочей и солей. Неэлектролиты – это вещества, которые не проводят электрический ток. К ним относятся многие органические вещества.
Электролиты, которые практически полностью диссоциируют на ионы, называются сильными; электролиты, которые частично диссоциируют на ионы, называются слабыми. Для количественной оценки полноты диссоциации введено понятие степени диссоциации. Степенью диссоциации электролита называют отношение числа молекул, распавшихся на ионы, к общему числу молекул, находящихся в растворе.
Обычно степень диссоциации (α) выражают в долях единицы или %:
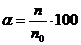 , (12)
, (12)
где n – число частиц, подвергшихся электролитической диссоциации;
n 0 – общее число частиц в растворе.
Сильные электролиты – почти все соли, растворимые основания (NaOH, KOH, Ba(OH)2 и др.), неорганические кислоты (H2SO4, HCl, HNO3, HBr, HI и др).
Слабые электролиты – нерастворимые основания и NH4OH, неорганические кислоты (H2CO3,, H2S, HNO2, H3PO4 и др.), органические кислоты и вода H2O.
Сильные электролиты диссоциируют на ионы практически нацело (т.е. процесс диссоциации является необратимым) и одностадийно:
HCl = H+ + Cl– H2SO4 = 2H+ + SO42–
Слабые электролиты диссоциируют частично (т.е. процесс диссоциацииявляется обратимым) и ступенчато. Например, для многоосновных кислот на каждой стадии происходит отрыв одного иона водорода:
1. H2SO3 ⇄ H+ + HSO3- 2. HSO3- ⇄ H+ + SO32-
Таким образом, число стадий многоосновных кислот определяется основностью кислоты (числом ионов водорода), а число стадий многокислотных оснований будет определяться кислотностью основания (или числом гидроксильных групп): NH4OH ⇄ NH4+ + OH–. Процесс электролитической диссоциации завершается установлением в системе состояния химического равновесия, которое характеризуется константой равновесия: 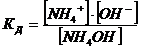
Константа равновесия процесса электролитической диссоциации называется константой диссоциации – КД. Константа диссоциации зависит от природы электролита, природы растворителя, температуры, но не зависит от концентрации электролита.
Между КД и α существует количественная связь:
 (13)
(13)
Соотношение (13) называют законом разбавления Оствальда: степень диссоциации слабого электролита возрастает с разбавлением раствора.
Для слабых электролитов, когда α << 1, КД = α2С.
Вода является слабым электролитом, поэтому диссоциирует обратимо:
H 2O ⇄ H+ + OH– ∆H = +56,5кДж/моль
Константа диссоциации воды: 
Степень диссоциации воды очень мала (это очень слабый электролит). Так как вода присутствует в большом избытке, то ее концентрация может считаться величиной постоянной и составляет  , тогда
, тогда
КД [ H2O] = [H+]∙[OH-] = 55,6∙1,8∙10-16 = 10-14
[ H+]∙[OH-] = 10-14 = KW – ионное произведение воды
Так как в воде концентрации катионов водорода и гидроксид-ионов равны, то: [ H+] = [OH-] =  .
.
Растворение в воде других веществ (кислот, оснований, солей) изменяет концентрацию ионов Н+ или ОН–, а их произведение всегда остается постоянным и равным 10-14 при Т=250С. Концентрация ионов Н+ может служить мерой кислотности или щелочности раствора. Обычно для этой цели используется водородный показатель: pH = -lg[H+]. Таким образом, водородный показатель – это десятичный логарифм концентрации ионов водорода, взятый с обратным знаком.
Не нашли, что искали? Воспользуйтесь поиском: