
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Работа 6.4. Определение буферной емкости раствора
Цель работы: определение значения буферной емкости раствора по кислоте и основанию (по заданию преподавателя) потенциометрическим методами.
Реактивы: буферный раствор (по заданию преподавателя); растворы соляной кислоты и едкого натра концентрации 0,1моль/л, дистиллированная вода.
Оборудование: конические колбы вместимостью 50 мл, бюретки на 25 мл, пипетки вместимостью 10мл, стаканы вместимостью 50 мл, фильтровальная бумага, рН-метр.
Методика работы
В двух конических колбах вместимостью 50 мл готовят буферные растворы (по заданию преподавателя) с заданным соотношением компонентов объемом 30 мл.
Затем проводят исследования зависимости рН буферного раствора от количества добавленной кислоты. Для этого в один из буферных растворов добавляют порциями по 0,05 мл раствор соляной кислоты концентрации 0,1 моль/л до тех пор, пока pH раствора не изменится на единицу. После добавления каждой порции раствора кислоты определяют pH на pH-метре.
Данные заносят в табл. 6.2.
Таблица 6.2
Результаты титрования и измерения рН
| Объем добавленной кислоты V кисл, мл | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | ... | |
| рH |
Используя полученные данные, аналитически вычисляют значение буферной емкости по кислоте (В кисл) по формуле
 ,
,
где C кисл – молярная концентрация эквивалентов кислоты, моль/л; V кисл – объем раствора кислоты, мл; V б – объем буферного раствора, мл; рН0 - значения pH исходного раствора; рН1 – значение рН контрольного раствора.
Буферную емкость растворов определяют также графически по тангенсу угла наклона зависимости рН= f (V кисл), где tg a = DрН/ V кисл, а DрН = рН0 – рН1.
Аналогичные исследования проводят для нахождения значения буферной емкости по основанию (В осн). В заданный буферный раствор добавляют сильное основание (NaOH) концентрации 0,1 моль/л. После добавления каждой порции раствора основания определяют pH на pH-метре.
Полученные данные заносят в табл. 6.3.
Таблица 6.3
Результаты титрования и измерения рН
| Объем добавленного основания V осн., мл | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | … | |
| рH |
Значение буферной емкости по основанию вычисляют аналитически и графически так же, как и для определения В кпо аналогичной формуле:
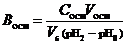 .
.
где C осн – молярная концентрация эквивалентов основания, моль/л; V осн – объем раствора основания, мл; V б – объем буферного раствора, мл; рН0 - значения pH исходного раствора; рН2 – значение рН контрольного раствора.
Вопросы для самостоятельной подготовки и контроля
1. Какие системы называются буферными? Их состав.
2. Буферные системы и механизм их действия.
3. Какие методы определения рН буферных смесей вы знаете? Приведите формулу расчета рН буферных систем.
4. От каких факторов и как зависит рН буферных растворов?
5. Что называется буферной емкостью? Как она рассчитывается и какие факторы оказывают влияние на ее значение?
6. Какие методы определения буферной емкости вы знаете?
7. Какие электроды применяются для определения рН?
8. Биологическое значение буферных систем.
Не нашли, что искали? Воспользуйтесь поиском: