
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Распределение Максвелла
В равновесном состоянии в системе, состоящей из огромного числа частиц, например в некотором объеме газа, при отсутствии внешних воздействий не происходит макроскопических изменений: параметры системы остаются постоянными. Постоянным остается и среднее значение скорости молекул. Ответ на вопрос, сколько молекул, или какая их часть движется с определенной скоростью в данный момент, был теоретически получен Максвеллом.
Введем понятие пространства скоростей. Для каждой молекулы откладываем компоненты ее скорости по трем взаимно перпендикулярным осям (рис. 1.3.1).

Каждая точка в пространстве скоростей соответствует одной молекуле с определенной скоростью. Вектор скорости идет от начала координат к рассматриваемой точке.
Рассмотрим, как будут распределены молекулы, содержащиеся в единичном объеме газа по скоростям.
Эти молекулы будут изображаться совокупностью из n точек. Из-за столкновений молекул какие-то точки будут выходить из элемента объема, а другие входить в него. Однако среднее число точек в данном элементе объема сохраняется.
Закон Максвелла описывается некоторой функцией f(v), которая называется функция распределения молекул по скоростям. Функция f(v) определяет относительное число молекул dN(v)/N, скорости которых лежат в интервале от v до v+dv, т.е.
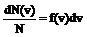 , откуда
, откуда  .
.
Применяя методы теории вероятностей, Максвелл нашел эту функцию:
 (1.3.1)
(1.3.1)
Из формулы видно, что конкретный вид функции зависит от рода газа (от массы молекулы m0) и от параметра состояния (температуры T).
График функции f(v) приведен на рис.1.3.2. Функция f(v) начинается от нуля, достигает максимума при vв и затем асимптотически стремится к нулю. Кривая не симметрична относительно vв.
Распределение Максвелла - это распределение по скоростям молекул идеального газа, находящегося в состоянии термодинамического равновесия.
Интегрируя распределение Максвелла, можно рассчитать средние величины. Средний квадрат скорости (средняя квадратичная скорость)

Рис.1.3.2.
Рис.1.3.2
 1.3.2)
1.3.2)

|
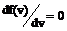 откуда следует, что
откуда следует, что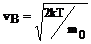 (1.3.3)
(1.3.3)
Для того, чтобы найти число молекул, обладающих скоростями в интервале от v1 до v2, необходимо определить площадь под соответствующим участком кривой (рис.1.3.2.)

При увеличении температуры максимум кривой Максвелла смещается в сторону больших скоростей и вид кривой изменяется. Распределения для двух разных температур приведены на рис.1.3.3. Поскольку площадь, ограниченная кривой, остается неизменной, следовательно, при повышении температуры кривая распределения молекул по скоростям будет растягиваться и понижаться.
 |
Рис.1.3.3 Т1< Т.
Среднее значение абсолютной величины скорости (среднее значение скорости равно нулю, так как отрицательное и положительное значения компонент равноправны) определяется по формуле
 (1.3.4)
(1.3.4)
Таким образом, скорости, характеризующие состояние газа:
1) наиболее вероятная  ;
;
2) средняя скорость  ;
;
3) средняя квадратичная  .
.
Эти скорости связаны соотношением
vВ: ávñ: ávквñ @1:1,13:1,22,
то есть средняя квадратичная скорость имеет наибольшую величину.
Исходя их распределения молекул по скоростям, перейдя к новой переменной Е=m0v2/2, можно получить функцию распределения молекул по энергиям
 (1.3.5)
(1.3.5)
Тогда средняя кинетическая энергия молекулы идеального газа равна
 (1.3.6)
(1.3.6)
Для того, чтобы рассчитать количество молекул DN, скорости которых находятся в промежутке от v до v+Dv, удобно ввести относительную скорость u=v/vВ, где vВ - наиболее вероятная скорость. Тогда DN - число молекул, относительные скорости которых находятся в интервале u, u+Du, т.е. v/vв, v+Dv/vВ, где должно быть Dv†v. Таким образом, имеем
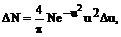
где N - полное число молекул газа, DN/N - относительное число (доля) молекул, имеющих скорости в интервале u, u+Du. График этой зависимости соответствует рис.1.3.2, если по оси абсцисс отложить u, а по оси ординат величину DN/(NDu) - функцию распределения.
Пример7. Определить среднеквадратичную скорость молекул азота при температуре 27°С. Как зависит средне квадратичная скорость от молекулярной массы и температуры?
Т=300°К, m=28 кг/кмоль, k=1,38×10-23Дж/град.
Решение. 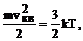 где
где 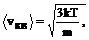
 ;
;
Таким образом 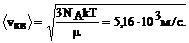
Средняя квадратичная скорость прямо пропорциональна корню квадратному из температуры и обратно пропорциональна корню квадратному из молекулярной массы.
Не нашли, что искали? Воспользуйтесь поиском: