
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
В ГОМОГЕННЫХ И ГЕТЕРОГЕННЫХ СИСТЕМАХ
163. Константа равновесия системы 2NO + O2 ↔2NO2 найдена равной 1,21. Равновесные концентрации [NО] = 0,72 и [NO2] = 0,84 моль 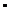 л–1. Найти первоначальную и равновесную концентрацию кислорода.
л–1. Найти первоначальную и равновесную концентрацию кислорода.
164. Куда сместится равновесие в системе
MgC12 + 2NH4OH ↔ Mg(OH)2 + 2NH4C1
при добавлении концентрированного раствора хлорида аммония, т.е. будет ли Mg(OH)2 растворяться или осадок будет увеличиваться?
165. Константа равновесия гомогенной системы СО(г) + Н2О(г) ↔ СО2(г) + Н2(г)
при некоторой температуре равна 1. Вычислите равновесные концентрации всех реагирующих веществ, если исходные концентрации [CO] = 0,1 моль 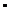 л–1; [H2O] = 0,4 моль
л–1; [H2O] = 0,4 моль 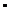 л–1
л–1
166. Куда сместится равновесие в системе AlO  + H2O ↔AlO
+ H2O ↔AlO  + 2ОН–;
+ 2ОН–;
а) при разбавлении раствора;
б) при прибавлении щелочи;
в) при прибавлении кислоты?
167. Реакция СО + С12 ↔ СОС12 протекает в объеме 10 л. Состав равновесной смеси: 14 г СО; 35,5 г С12 и 49,5 г СОС12. Вычислить константу равновесия реакции.
168. Равновесные концентрации веществ в обратимой реакции 2SO2 + O2 ↔ 2SO3 составляют (моль 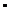 л–1): [SO2] = 0,002; [O2] = 0,004; [SO3] = 0,003. Вычислить исходные концентрации кислорода и оксида серы (IV). Вычислить константу равновесия.
л–1): [SO2] = 0,002; [O2] = 0,004; [SO3] = 0,003. Вычислить исходные концентрации кислорода и оксида серы (IV). Вычислить константу равновесия.
169. В сосуд объемом 0,5 л помещено 0,5 моля водорода и 0,5 моля азота. К моменту равновесия образовалось 0,02 моля аммиака. Вычислить константу равновесия.
170. Окисление аммиака идет по уравнению 4NH3 + 5О2 = 4NO + 6H2O.
Через некоторое время после начала реакции концентрации участвующих в ней веществ были (моль/л): [NH3] = 0,009; [O2] = 0,02; [NO] = 0,003. Вычислить: а) концентрацию водяного пара в этот момент; б) исходную концентрацию аммиака и кислорода.
171. Начальная концентрация пятихлористого фосфора в реакции
PCl5 ↔ PCl3 + Cl2
0,2 моль/л. К моменту наступления равновесия прореагировали 50% исходного количества пятихлористого фосфора. Найти общую концентрацию участвующих в реакции веществ в состоянии равновесия.
172. Исходные концентрации азота и водорода в реакции N2 + 3H2 ↔ 2NH3
были (моль/л): [N2] =2, [H2] = 8. К моменту наступления равновесия прореагировало 10% исходного количества азота. Вычислить давление газовой смеси в этот момент, если температура ее была 5000С.
173. Для обратимой реакции H2 + J2 ↔ 2HJ при 5090С константа скорости прямой реакции 0,16, а константа скорости обратной реакции 0,0047. Вычислить константу равновесия.
174. Константа равновесия обратимой реакции 2N0 + О2 ↔ 2NO2 при 4940С равна 2,2. Сколько молей кислорода надо ввести на каждый литр N0, чтобы окислить 40% N0 в NO2, если исходная концентрация N0 равна 0,04 моль/л?
175. В состоянии равновесия обратимой реакции PCl5 ↔ PCl3 + Cl2
концентрации участвующих в реакции веществ были (моль/л): [PCl5]=0,005, [PCl3]=0,060, [Cl2]=0,080. Вычислить равновесные концентрации этих веществ после сдвига равновесия вследствие увеличения концентрации хлора в два раза.
РАСТВОРЫ.
Не нашли, что искали? Воспользуйтесь поиском: