
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Определение уровня глюкозы в крови с помощью глюкометра One Touch ultra.
Занятие №1.
Актуальность темы.
Углеводы широко распространены в природе. Они входят в состав живых организмов и вместе с белками, липидами
и нуклеиновыми кислотами определяют специфичность их строения и функционирования. Углеводы участвуют во
многих метаболических процессах и прежде всего они являются основными поставщиками энергии, выполняют
структурную роль. Из них в процессе метаболизма образуется большое число органических соединений, которые
служат исходными субстратами для синтеза липидов, аминокислот, нуклеотидов. Производные углеводов участвуют
в детоксикации ксенобиотиков и инактивации веществ эндогенного происхождения. Углеводы могут
синтезироваться с использованием других метаболитов: некоторых аминокислот, глицерина, молочной кислоты.
Учебные и воспитательные цели:
1. Общая цель занятия:
- привить знания о химическом строении и значении углеводов для жизнедеятельности организма.
2. Частные цели
- уметь определять глюкозу, фруктозу и крахмал в растительных продуктах качественными реакциями.
1. Входной контроль знаний:
1.1. Тесты.
1.2. Устный опрос.
2. Основные вопросы темы:
2.1. Понятие об углеводах, биологическая роль и химическое строение отдельных представителей
(моносахаридов, дисахаридов).
2.2. Протеогликаны, гликопротеины.
2.3. Переваривание и всасывание углеводов в желудочно-кишечном тракте. Роль клетчатки. Непереносимость
углеводов. Мальабсорбция дисахаридов.
3. Лабораторно-практические работы:
3.1. Качественные реакции:
- на глюкозу – реакция Троммера, реакция Фелинга, реакция Ниландера;
- на фруктозу – реакция Селиванова.
3.2. Обнаружение глюкозы и фруктозы в объектах растительного происхождения.
Выходной контроль
4.1. Ситуационные задачи.
5. Литература:
5.1. Материал лекций.
5.2. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. М.: «Медицина», 2004г., с. 169-187, 319-327,
357-359, 361-362
Основные вопросы темы
2.1. Понятие об углеводах, биологическая роль и химическое строение отдельных представителей
(моносахаридов, дисахаридов).
Углеводы вместе с белками, липидами и нуклеиновыми кислотами входят в состав живых организмов и определяют специфичность их строения и функционирования. На долю углеводов приходится около 75% массы пищевого рациона и более 50% от суточного количества необходимых калорий. Углеводы являются поставщиками энергии и выполняют структурную роль. Из углеводов в процессе метаболизма образуются вещества, которые служат исходными субстратами для синтеза липидов, аминокислот, нуклеотидов.
Углеводы – это альдегидо- или кетоноспирты.
Функции углеводов:
1. Энергетическая;
2. Углеводы (рибоза, дезоксирибоза) входят в состав нуклеиновых кислот, свободных мононуклеотидов (АТФ, ГТФ, цАМФ и др.), коферментов (НАД, НАДФ, ФАД);
3. Структурная: гликопротеины – коллаген; белки-рецепторы; гликокаликс, белки определяющие принадлежность к группе крови; факторы свертывания крови; ферменты, гормоны; гликозаминогликаны и др;
4. Защитная: иммуноглобулины, интерферон, муцины, фибриноген, гликозаминогликаны и др.;
5. Дезинтоксикационная - входят в состав ФАФС (фосфоаденозинфосфосульфат) и УДФГК (уридиндифосфоглюкуроновая кислота).
Суточная потребность – 500 грамм.
Классификация:
1. Моносахариды – производные многоатомных спиртов, содержащих альдегидную или кетонную группу. В
зависимости от количества углеродных атомов моносахариды делятся на:
Истинные:
- триозы
- тетрозы
- пентозы (рибоза, дезоксирибоза)
- гексозы (глюкоза, галактоза, фруктоза) и др.
Производные моносахаридов:
- уроновые кислоты – если вместо СН2ОН группы в 6 положении – СООН группа (у глюкозы – глюкуроновая
кислота; у галактозы – галактоуроновая кислота). Они входят в состав гликозаминогликанов;
- аровые кислоты – если в 6 и 1 положениях – СООН группы (у глюкозы – глюкаровая, у галактозы –
галактаровая);
- аминосахара – если во 2 положении – NН2группа (у глюкозы – глюкозамин, у галактозы – галактозамин). Они
входят в состав гликозамингликанов;
- N-гликозиды (рибоза, дезоксирибоза, соединенные с азотистым основанием в нуклеотиде - N-гликозидной
связью). Входят в состав РНК, ДНК, АТФ, НАД, ФАД и др.;
- фосфорные эфиры моносахаридов – замещение атомов Н на остатки фосфорной кислоты: глюкозо-6-фосфат;
фруктозо-1,6-дифосфат; рибозо-5-фосфат и др.

2. Олигосахариды (в их состав входят от 2 до 10 остатков моносахаридов)
Дисахариды:
- мальтоза состоит из 2 молекул α-Dглюкозы, соединенных α-1,4-гликозидной связью. Она имеет свободный
полуацетальный гидроксил, обладает восстанавливающими свойствами;
- лактоза (молочный сахар) состоит из β-Dгалактозы и α-Dглюкозы соединенные β-1,4-гликозидной связью.
Имеет свободный полуацетальный гидроксил и обладает восстанавливающими свойствами.
- сахароза состоит из α-Dглюкозы и β-Dфруктозы, соединенные α-1,2-гликозидной связью. Свободного
полуацетального гидроксила не имеет, поэтому не обладает восстанавливающими свойствами.
3. Полисахариды:
- гомополисахариды (крахмал, клетчатка, гликоген);
- гетерополисахариды (гликопротеины, протеогликаны, гликолипиды).).
2.2. Протеогликаны, гликопротеины.
Протеогликаны – это сложные белки, состоящие из белков и углеводов. Углеводы, входящие в состав
протеогликанов называются глкозаминргликанами.
Классификация гликозаминогликанов:
1. гиалуроновая кислота
2. хондроитин-4-сульфат
3. хондроитин-6-сульфат
4. дерматансульфат
5. кератансульфат
6. гепарин.
Они широко распространены в организме человека: кожа, сухожилия, хрящи, кости, синовиальная жидкость,
стекловидное тело, роговица, пупочный канатик, слизистые рта, носа, бронхов, кровеносных сосудов.
Функции гликозаминогликанов:
1. защитно-механическая;
2. гиалуроновая кислота является «биологическим цементом» т.е. заполняя межклеточное вещество, укрепляет соединительную ткань, тем самым препятствует проникновению в организм болезнетворных микроорганизмов;
3. обладают высокой гидрофильность, т.е. удерживают воду и катионы, принимая участие в регуляции водно-солевого обмена;
4. обладают высокой вязкостью – участвуют в формировании пищевого комка, облегчая процессы проглатывания;
5. гепарин – естественный антикоагулянт (предотвращает процессы свертывания крови).
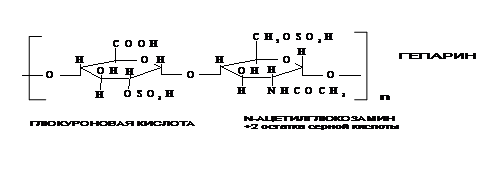
Строение гликозаминогликанов:
1. в структуру мономера гиалуроновой кислоты входят: глюкуроновая кислота, соединенная с N-
ацетилглюкозамином;
2. в структуру мономера гепарина входят: глюкуроновая кислота, N-ацетилглюкозамин и 2 остатка серной
кислоты.
2.3. Переваривание и всасывание углеводов в желудочно-кишечном тракте. Роль клетчатки. Непереносимость
углеводов. Мальабсорбция дисахаридов.
Попадая в желудочно-кишечный тракт, углеводы под действием ферментов распадаются на моносахариды и всасываются эпителиальными клетками тощей и подвздошной кишок с помощью специальных механизмов транспорта через мембраны этих клеток (путем облегченной диффузии и активного транспорта).
В ротовой полости пища измельчается при пережевывании, смачиваясь при этом слюной, рН которой равна 6,8. Под влиянием α-амилазы слюны (эндоамилаза) происходит расщепление в крахмале α-1,4-гликозидных связей. Она не расщепляет α-1,6-гликозидные связи в крахмале, поэтому крахмал переваривается лишь частично с образованием крупных фрагментов – декстринов и небольшого количества мальтозы. α-амилаза не гидролизует гликозидные связи в дисахаридах.
В желудке действие амилазы слюны прекращается, т.к. рН желудочного сока равен 1,5-2,5. Однако, внутри
пищевого комка активность амилазы может некоторое время сохранятся, пока рН не изменится в кислую
сторону.
В 12-перстной кишке рН равна 7,5-8,0. Из поджелудочной железы в кишечник поступает панкреатическая α-амилаза. Этот фермент также является эндогликозидазой т.к. расщепляет α-1,4-гликозидные связи в крахмале и декстринах. Продукты переваривания: олигосахариды, содержащие 3-8 остатков глюкозы, мальтоза, изомальтоза – дисахарид, состоящий из 2 молекул α-Dглюкозы, соединенных α-1,6-гликозидной связью. Дальнейшее их переваривание происходит в нижних отделах тонкого кишечника под действием мальтазы, изомальтазы. Дисахариды пищи сахароза и лактоза также расщепляются в тонком кишечнике сахаразой и лактазной (полостное пищеварение).
Процесс переваривания заканчивается на поверхности эпителиальных клеток кишечника (мембранное,
пристеночное пищеварение). Эпителиальные клетки покрыты микроворсинками, над которыми располагается
волокнистая сеть - гликокаликс (гликопротеин). В нем располагаются ферменты гидролизующие мальтозу,
сахарозу, лактозу, которые не расщепилисьв полости кишечника.
Скорость всасывания моносахаридов различна, глюкоза и галактоза всасываются быстрее, чем другие
моносахариды. Транспорт моносахаридов в клетке слизистой оболочке кишечника может осуществляться
различными способами: путем облегченной диффузии и активного транспорта. При высокой концентрации
глюкозы в просвете кишечника она транспортируется в клетку путем облегченной диффузии. При низкой
концентрации – глюкоза всасывается путем активного транспорта.
Механизм активного транспорта.
Глюкоза и Nа+ соединяются с разными участками белка-переносчика. При этом Nа+ поступает в клетку по градиенту концентрации и одновременно транспортируется глюкоза против градиента концентрации. Чем больше градиент Nа+, тем больше поступления глюкозы в энтероциты. Если концентрация Nа+ уменьшается, транспорт глюкозы снижается. Свободная энергия, необходимая для активного транспорта образуется благодаря гидролизу АТФ, связанному с натриевым насосом, который «откачивает» из клетки Nа+ в обмен на К+. Глюкоза соединяется с другим белком-переносчиком путем облегченной диффузии всасывается в кровь.
Роль клетчатки.
1. раздражая нервные окончания слизистой оболочки кишечника, усиливает перистальтику кишечника;
2. увеличивает секрецию кишечного сока;
3. способствует формированию каловых масс;
4. адсорбирует холестерол;
5. адсорбирует тяжелые металлы, радионуклиды;
6. подвергаясь в кишечнике спиртовому брожению, подавляет размножение гнилостных бактерий.
Мальабсорбция – группа заболеваний, связанная с нарушением:
1. переваривания углеводов в ЖКТ (дефект ферментов);
2. нарушение всасывания продуктов распада моносахаридов.
Примером первой группы заболеваний является лактазная недостаточность (дисахаридазная).
У детей различают 2 формы:
- транзиторная (до года жизни), связанная с незрелостью фермента лактазы;
- генетическая – мутация гена, ответственного за синтез фермента лактазы.
У взрослых:
- дефект лактазы вследствие экспрессии гена лактазы возрастного характера, при этом непереносимость молока у лиц африканского и азиатского происхожде6ния. Средняя частота данной формы в странах Европы – 7-12%, в Китае 80%, в отдельных районах Африки – 97% (исторически сложившийся рацион питания);
- приобретенного характера- при кишечных заболеваниях (гастриты, колиты, энтериты). Как известно, активность лактазы ниже, чем других дисахаридаз, поэтому понижение её активности становится более заметным.
Проявление во всех случаях: осмотическая диарея, которую вызывают нерасщепленные дисахариды и невсосавшиеся моносахариды, поступающие в дистальные отделы кишечника, изменяют осмотическое давление, частично подвергаются ферментативному расщеплению микроорганизмами, с образованием кислот, газов, усиливается приток воды в кишечник, увеличивается объем кишечного содержимого, увеличивается перистальтика, появляются метеоризм и боли.
3. Лабораторно-практические работы:
3.1. Качественные реакции:
- на глюкозу – реакция Троммера, реакция Фелинга, реакция Ниландера;
- на фруктозу – реакция Селиванова.
РЕАКЦИЯ ТРОММЕРА:
К 10 каплям 1% раствора глюкозы прибавить 5 капель 10% раствора NaOH и 2 капли 1% CuSO4 нагревают до
кипения. Образуется осадок желтого цвета СuOH или кирпично-красного цвета Cu2O.
РЕАКЦИЯ ФЕЛИНГА:
К 10 каплям 1% раствора глюкозы прибавить 5 капель реактива Фелинга-1 и 5 капель реактива Фелинга-2,
нагреть до кипения. Образуется осадок кирпично-красного цвета- Cu2O.
РЕАКЦИЯ НИЛАНДЕРА:
В пробирку наливают 10 капель 1% раствора глюкозы. Прибавляют 5 капель реактива Ниландера, кипятят 1-2
минуты. Образуется осадок черного цвета (восстановление висмута).
РЕАКЦИЯ СЕЛИВАНОВА:
В пробирку наливают 10 капель реактива Селиванова, добавляют 1-2 капли раствора фруктозы и нагревают до
кипения. Наблюдается красное окрашивание.
3.2. Обнаружение глюкозы и фруктозы в объектах растительного происхождения.
Углеводы моркови. В пробирку помещают 1 г. мелко нарезанной моркови, добавляют 2 мл воды и
встряхивают 2 мин. Надосадочную жидкость разливают поровну в 2 пробирки.
В одной пробирке открывают глюкозу реакцией Фелинга, в другой – фруктозу – с помощью реакции
Селиванова.
Реакция Фелинга – в 1-ю пробирку прибавляют 3 капли реактива Фелинга-1 и 3 капли реактива Фелинга-2.
Жидкость нагревают до кипения. Выпадает осадок кирпично-оранжевого цвета закиси меди.
Реакция Селиванова – во 2-ю пробирку добавляют 20 капель реактива Селиванова. Жидкость нагревают до
кипения, развивается красное окрашивание.
Углеводы меда. В 2 пробирки отмеривают по 6 капель раствора меда. В одну пробирку прибавляют 3 капли
реактива Фелинга-1 и 3 капли реактива Фелинга-2. Пробирку нагревают до кипения. Во 2-ю пробирку
прибавляют 20 капель реактива Селиванова и нагревают до кипения.
Открытие крахмала в картофеле. На срез картофеля наносят 2-3 капли раствора J2. Наблюдают появление
синего окрашивания.
Занятие №2.
Учебные и воспитательные цели:
Общая цель занятия:
- знать основы метаболизма глюкозы в организме.
Частные цели занятия:
- иметь представление о методах определения глюкозы в крови;
- уметь определять уровень глюкозы в крови с помощью глюкометра One Touch ultra.
1. Входной контроль знаний:
1.1. Тесты.
1.2. Устный опрос.
2. Основные вопросы темы:
2.1. Общая схема источников и путей использования глюкозы в организме.
2.2. Аэробный распад – основной путь катаболизма глюкозы у человека. Физиологическое значение.
2.3. Анаэробный распад глюкозы. Биологическая роль. Эффект Пастера.
2.4. Глюконеогенез и его значение. Регуляция.
2.5. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
3. Лабораторно-практическая работа:
3.1. Определение глюкозы в крови с помощью глюкометра One Touch ultra.
Выходной контроль
4.1. Ситуационные задачи.
5. Литература:
5.1. Материал лекций.
5.2. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. М.: «Медицина», 2004г., с. 327-334, 338-353,
359-362.
Основные вопросы темы
2.1. Общая схема источников и путей использования глюкозы в организме
|

2.2. Аэробный распад – основной путь катаболизма глюкозы у человека. Физиологическое значение.
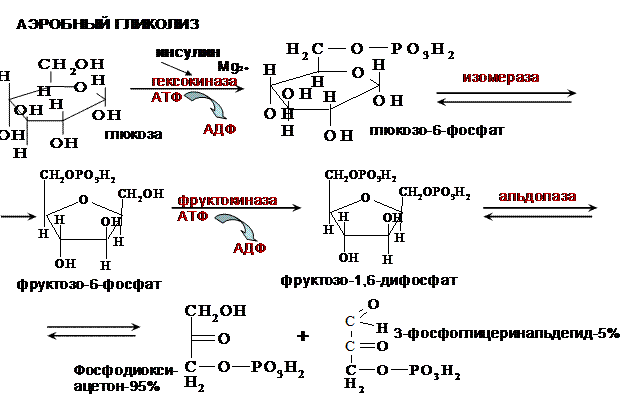
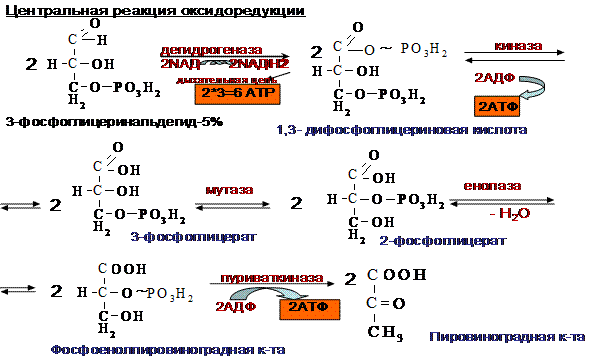
АЭРОБНЫЙ ГЛИКОЛИЗ – процесс окисления глюкозы до СО2 и Н2О, протекающий в присутствии кислорода. Все ферменты, катализирующие реакции находятся в цитозоле клетки.
Выделяют 2 этапа:
1. Подготовительный – глюкоза фосфорилируется и расщепляется на 2 молекулы фосфотриоз. Используются 2 молекулы АТФ.
2. Этап, сопряженный с синтезом АТФ. Фосфотриозы превращяются в ПВК, которая далее окисляется до СО2 и Н2О (ЦТК). Таким образом, выход АТФ – 38 молекул.
Основное физиологическое значение – использование энергии, которая освобождается в этом процессе для синтеза АТФ. Метаболиты гликолиза используются для синтеза новых соединений (фр-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата – структурного компонента нуклеозидов; 3-фосфоглицерат включается в синтез аминокислот: серин, глицин, цистеин). Являются субстратами для НАД-зависимых дегидрогеназ дых. цепи (глицеральдегид -3-фосфат, пируват, изоцитрат, α-кетоглутарат, малат). В печени и жировой ткани ацетил-КоА, образующийся из ПВК, используется как субстрат при биосинтезе жирных кислот, холестерина.

В1 недостаточность – известно что это водорастворимый витамин – тиамин – антиневритный, входит в состав как минимум 3 ферментов. Например, в виде ТДФ участвует в пируватдегидрогеназном комплексе (окисление ПВК до ацетил КоА). При его отсутствии из ацетил-КоА, в частности не образуется ацетилхолин, вследствии чего, возникают полиневриты, в основе которых лежат дегенеративные изменения нервов, затем паралич (Бери-бери), нарушения со стороны сердечно-сосудистой деятельности – нарушения ритма сердца, увеличения его размеров, боли, со стороны ЖКТ – снижение кислотности, потеря аппетита, атония кишечника.
2.3.Анаэробный распад глюкозы. Биологическая роль. Эффект Пастера.
АНАЭРОБНЫЙ ГЛИКОЛИЗ – процесс расщепления глюкозы с образованием конечного продукта лактата. Он протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи. АТФ образуется за счет субстратного фосфорилирования (2 АТФ). Протекает в мышцах, в первые минуты мышечной работы, в эритроцитах (в которых отсутствуют митохондрии), а также в разных органах в условиях ограниченного снабжения их кислородом, в том числе в опухолевых клетках. Этот процесс служит показателем повышенной скорости деления клеток при недостаточной обеспеченности их системой кровеносных сосудов.
Сходство анаэробного и аэробного гликолиза заключается в том, что до стадии образования ПВК эти процессы протекают одинаково при участии тех же ферментов.


 СН3 ЛДГ СН3
СН3 ЛДГ СН3






 Глюкоза С=О 2 Н-С-ОН
Глюкоза С=О 2 Н-С-ОН
СООН СООН
ПВК 2 НАДН2 2НАД лактат
Энергетический баланс анаэробного окисления глюкозы: образование 2 АТФ.
Основное физиологическое значение – использование энергии, которая освобождается в этом процессе для синтеза АТФ. Метаболиты гликолиза используются для синтеза новых соединений (фр-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата – структурного компонента нуклеозидов; 3-фосфоглицерат включается в синтез аминокислот: серин, глицин, цистеин).
ЭФФЕКТ ПАСТЕРА. Заключается в угнетении дыханием (О2) анаэробного гликолиза, т.е. происходит переключение с аэробного гликолиза на анаэробное окисление. Если ткани снабжены О2, то 2НАДН2, образовавшийся в процессе центральной реакции оксидоредукции, окислится в дыхательной цепи, поэтому ПВК не превращается в лактат, а в ацетил-КоА, который вовлекается в ЦТК.
2.3. Глюконеогенез и его значение.
Это процесс синтеза глюкозы из веществ неуглеводной природы. Процесс протекает в печени и менее интенсивно в корковом веществе почек, а также в слизистой кишечника. Эти ткани могут обеспечивать синтез 80-100 г глюкозы в сутки.
Первичные субстраты – лактат, аминокислоты, глицерол. Их включение в глюконеогенез зависит от физиологического состояния организма:
лактат – постоянно;
глицерол – высвобождается при гидролизе жиров в период голодания или при длительной физической нагрузке;
аминокислоты – образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
Если гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях. Процесс идет обратно анаэробному гликолизу за исключением 3-х необратимых реакций:
1. Пируваткиназная – образование фосфоенолпирувата из ПВК происходит в ходе 2-х реакций, первая из кот. протекает в митохондриях. ПВК транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалацетата (ЩУК). Фермент-пируваткарбоксилаза, коферментом которым является биотин. Реакция протекает с использование АТФ. Затем оксалацетат (в цитозоле) превращается в фосфоенолпируват входе реакции, катализируемой фосфоенолпируваткарбоксилазой – ГТФ-зависимым ферментом (-СО2, ГТФ → ГДФ).
2. Фосфофруктокиназная: ФР-1,6-дифосфат →Фр-6-фосфат под действием фермента фруктозо-1,6-бифосфатаза.
3. Гексокиназная: Гл-6-фосфат→ Глюкоза под действием фермента Гл-6-фосфатазы.

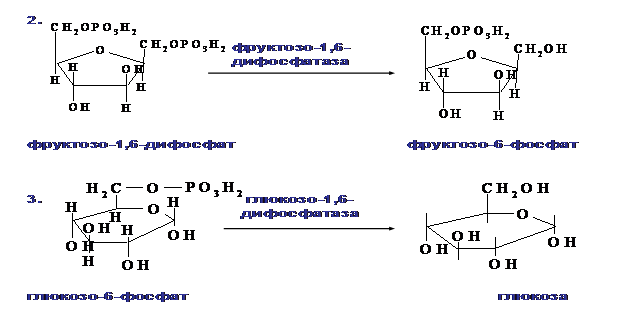
ЗНАЧЕНИЕ – поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок.
РЕГУЛЯЦИЯ: инсулин – тормозит синтез ферментов; глюкокортикоиды – индуцируют синтез ферментов; СТГ – повышает активность ферментов глюконеогенеза.
2.4. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
ЦИКЛ КОРИ.
(взаимосвязь гликолиза в мышцах и глюконеогенеза в печени).
Схема:

ЗНАЧЕНИЕ:
1. Регуляция постоянного уровня глюкозы в крови.
2. Обеспечивает утилизацию лактата.
3. Предотвращает накопление лактата (снижение рН - лактоацидоз).
4. Экономичное использование углеводов организмом.
5. Регуляция обмена углеводов осуществляется на уровне тканей – кровь, печень, мышцы.
3. Лабораторно-практическая работа:
Определение уровня глюкозы в крови с помощью глюкометра One Touch ultra.
3.1. Ознакомление студентов с работой глюкометра «One Touch» ultra.
Измерение содержания сахара в пробе крови с помощью глюкометра происходит посредством электрического сигнала, который возникает при взаимодействии иммобилизованного на тест-полоске фермента (оксидазы глюкозы) с субстратом (глюкозой), находящемся в исследуемой капле крови. Глюкометр позволяет определить уровень глюкозы в крови в диапазоне 1,1-33,3 ммоль/л.
а) Кодирование прибора необходимо выполнять перед первым использованием прибора. Войдите в режим кодирования. Введите тест-полоску (обозначение «Ш») в прибор. На экране появляются все его сегменты, затем появляется номер кода. Сравните номер кода на флаконе тест-полосок. Если номера совпадают, можно приступать к проведению анализа, а если не совпадают, то нажмите кнопку «С», пока номер не совпадет. После этого появляется символ «капля крови». Прибор готов к проведению анализа.
3.2. Определение уровня глюкозы в крови у студентов с помощью глюкометра «One Touch» ultra. Проведение анализа. Подведите каплю крови на пальце руки к зоне теста на верхней части тест-полоски и удерживайте ее в таком положении до полного заполнения капилляра. На экране появляется отчет в течение 5 секунд, после чего обозначается величина уровня глюкозы в ммоль/л. После удаления тест-полоски изображение на экране прибора гаснет и он готов к следующему проведению анализа.
Ход работы: Вымойте руки теплой водой с мылом и тщательно высушите. Обработайте палец руки ватой, смоченной в этиловом спирте и подсушите его. Стерильным скарификатором проколите кожу пальца и выдавите из него капельку крови, которую введите в капилляр тест-полоски. Затем обработайте место прокола ватой, смоченной в этиловом спирте.
Вывод: полученное показание сравнить с нормой глюкозы в крови. Норма - 3,3-5,5 ммоль/л. Если уровень глюкозы выше 5,5 ммоль/л – гипергликемия, если ниже 3,3 ммоль/л – гипогликемия
Занятие №3.
Учебные и воспитательные цели:
1. Общая цель занятия:
- знать биохимические аспекты гликогенозов, сахарного диабета.
2. Частные цели:
- уметь определять уровень глюкозы в крови натощак и после сахарной нагрузки.
1. Входной контроль знаний:
1.1. Тесты.
1.2. Устный опрос.
1.3. Реферативные сообщения.
2. Основные вопросы темы:
2.1. Пентозофосфатный путь превращений глюкозы. Окислительные реакции (до стадии рибулозо-5-фосфата).
Распространение и физиологическое значение.
2.2. Влияние этилового алкоголя на обмен углеводов
2.3. Гликоген – свойства, биосинтез и мобилизация гликогена. Регуляция процессов.
2.4. Гликогенозы.
2.5. Содержание глюкозы в крови. Гипо-, гипергликемия, глюкозурия и причины их возникновения.
2.6. Сахарный диабет, биохимическая характеристика патогенеза. Механизм действия инсулина.
3. Лабораторно-практическая работа:
3.1. Определение глюкозы в крови с помощью глюкометра One Touch ultra натощак и после сахарной нагрузки.
Выходной контроль
4.1. Ситуационные задачи.
5. Литература:
5.1. Материал лекций.
5.2. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. М.: «Медицина», 2004г., с. 335-338, 353-357,
359-361.
Основные вопросы темы
2.1.Пентозофосфатный путь превращений глюкозы. Окислительные реакции (до стадии рибулозо-5-фосфата).
Распространение и физиологическое значение.
Пентозофосфатный путь является альтернативным путем окисления глюкозы. Это путь окисления глюкозы путем укорочения углеродной цепочки на один углеродный атом. Пентозофосфатный путь не приводит к синтезу АТФ.
В пентозофосфатном пути различают два этапа:
Окислительный путь включает две реакции дегидрирования с участием кофермента НАДФ и реакцию декарбоксилирования. В результате образуется НАДФН2 и пентозы (рибозро-5-фосфат).
Неокислительный путь служит для синтеза пентоз. Реакции этого пути обратимы, поэтому из пентоз могут образовываться гексозы. Промежуточные продукты (фруктозо-6-фосфат, глицеро-альдегид-3-фосфат) могут включаться в пути аэробного и анаэробного окисления. Знать химизм окислительного этапа.
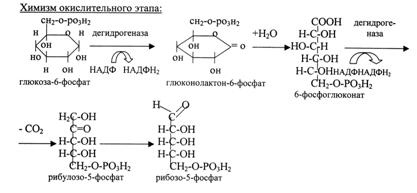
Таким образом, в результате пентозофосфатного пути окисления глюкозы образуются пентозы, необходимые для синтеза нуклеиновых кислот (ДНК, РНК), коферментов (НАД, НАДФ, ФМН, ФАД), а также восстановленная форма НАДФ, водороды которого необходимы для восстановительных синтезов (синтез высших жирных кислот, холестерола, гормонов коры надпочечников, половых гормонов, провитаминов группы Д, желчных кислот), участвует в обезвреживании лекарственных веществ и ядов в печени. Этот путь окисления функционирует в печени, в жировой ткани, молочной железе, коре надпочечников, а также в быстро растущих, регенерирующихся тканях.
2.2. Влияние этилового спирта на углеводный обмен.
Катаболизм этанола осуществляется главным образом в печени (75-98%). Основную роль в метаболизме этанола играет цинксодержащий фермент НАД+- зависимый фермент – алкогольдегидрогеназа, локализующийся в цитозоле и митохондриях печени (95%). В ходе реакции происходит дегидрирование этанола, образуются ацетальдегид и восстановленный НАДН. Алкогольдегидрогеназа катализирует обратимую реакцию, направление которой зависит от концентрации ацетальдегида и соотношения НАДН/НАД+ в клетке.
дегидрогеназа дегидрогеназа
С2Н5ОН → Н3С-СОН → СН3СООН → Н3СОSKoA → ЦТК
НАД → НАДН2 НАД → НАДН2
этанол ацетальдегид уксусная кислота ацетил КоА
При употреблении большого количества спирта количество НАД уменьшается, а НАДН2 увеличивается. Это приводит к уменьшению ПВК – основной предшественник образования глюкозы → гипогликемия, особенно когда запасы гликогена в печени и мышцах невелики (употребление алкоголя натощак, после физической нагрузки, у хронических алкоголиков); блокируется синтез глюкозы из лактата и аминокислот (глюконеогенез). Гипогликемия сказывается на функции мозга и может быть причиной потери сознания при алкогольном отравлении. Алкоголь не содержит витаминов. Алкоголики получают основную массу калорий со спиртом, в котором нет витамина В1. Характерная для них недостаточность тиамина проявляется в синдроме Вернике - Корсакова, сопровождается расстройствами функций нервной системы, психозами, потерей памяти (причина – сочетание недостатка тиамина и снижение активности тиаминзависимого фермента транскетолазы).
2.3. Гликоген – свойства, биосинтез и мобилизация гликогена.
Гликоген – животный крахмал, главный резервный гомополисахарид. Значительная часть глюкозы, поступающей в кровь, превращается в гликоген – запасный полисахарид, используемый в интервалах между приемами пищи в качестве источника глюкозы. Наибольшая концентрация гликогена обнаруживается в печени 2 – 6%, а в мышцах содержится 0,5 – 2%. В клетке гликоген находится не в растворенном состоянии, а в виде гранул. Гликоген имеет высокую молекулярную массу (1∙106 - 2∙108) и содержит до 1 млн. остатков глюкозы, соединенных 1,4 и 1,6 - гликозидными связями. Гликоген с йодом дает красно – бурое окрашивание.
Синтез гликогена.
Происходит тогда, когда после использования глюкозы остается её часть и она запасается в организме в виде
гликогена.

Фермент гликогенсинтаза участвует в образовании α-1,4-гликозидных связей, ветвящий фермент в образовании α-1,6-гликозидных связей. Образовавшиеся молекулы гликогена обладают низкой растворимостью и, следовательно, низким влиянием на осмотическое давление в клетке по сравнению с глюкозой, это объясняет то, что в клетке депонируется гликоген, а не глюкоза.
Распад гликогена.
Распад гликогена с образованием глюкозы происходит в период между приемами пищи, физической работе, при стрессе.
Пути мобилизации гликогена:
1. фосфоролитический.
2. амилолитический путь распада гликогена происходит при участии фермента амилазы.
Фосфоролитический путь – основной путь распада гликогена с образованием глюкозы:
 В мышечной ткани нет фермента глюкозо-6-фосфатазы, поэтому гликоген мышц не распадается с
В мышечной ткани нет фермента глюкозо-6-фосфатазы, поэтому гликоген мышц не распадается с
образованием глюкозы, а окисляется или аэробным или анаэробным путем с освобождением энергии. Через
10-18 часов после приема пищи запасы гликогена в печени значительно истощаются.
Регуляция уровня глюкозы в крови. Роль ЦНС, механизм действия инсулина, адреналина, глюкагона,
СТГ, глюкокортикоидов, тироксина и их влияние на состояние углеводного обмена.
Ведущее значение в регуляции углеводного обмена принадлежит центральной нервной системе. Снижение уровня глюкозы в крови приводит к повышенной секреции адреналина, глюкагона, которые, поступая в орган-мишень для этих гормонов (печень), узнаются рецепторами мембран клеток печени и активируют фермент мембраны аденилатциклазу, запуская механизм, приводящий к распаду гликогена с образованием глюкозы.
Схема механизма взаимодействия адреналина и глюкагона с клеткой:
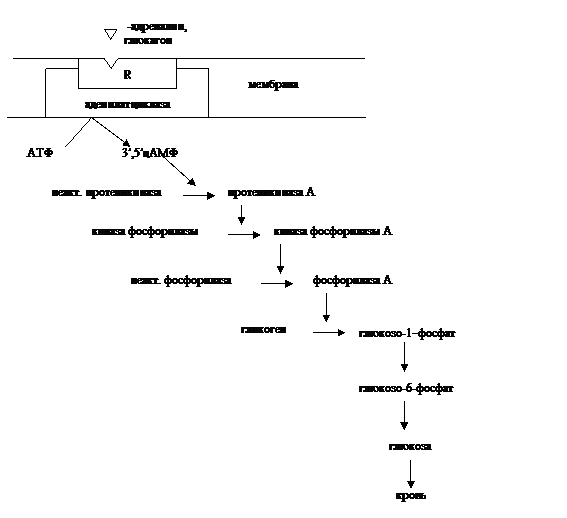

Адреналин – повышает уровень глюкозы за счет активации фермента фосфорилазы (аденилатциклазная система), которая приводит к распаду гликогена с образованием глюкозы, блокирует фермент гликогенсинтазу, т.е. синтез гликогена.
Глюкагон – действует подобно адреналину, но плюс к этому активирует ферменты глюконеогенеза.
Глюкокортикоиды – повышают уровень глюкозы крови, являясь индукторами синтеза ферментов глюконеогенеза.
СТГ актвирует глюконеогенез, тироксин активирует инсулиназу, расщепляющую инсулин, влияет на всасывание глюкозы в кишечнике.
2.4. Гликогенозы
Гликогенозы (болезни накопления гликогена) обусловлены дефектом ферментов, участвующих в распаде гликогена. Например, болезнь Гирке связана с отсутствием фермента глюкозо-6-фосфатазы, при этом наблюдается избыточное накопление гликогена в печени, гипогликемия и ее последствия. Болезнь Мак-Ардла: причина - отсутствие фосфорилазы в мышечной ткани. При этом уровень глюкозы в крови в норме, но наблюдается слабость мышечной ткани и снижена способность выполнять физическую работу. Болезнь Андерсена связана с дефектом, ветвящего фермента, что приводит к накоплению гликогена в печени с очень длинными наружными и редкими точками ветвления, вследствие этого – желтуха, цирроз печени, печеночная недостаточность, летальный исход (неразветвленный гликоген разрушает гепатоциты).

2,5 Концентрация глюкозы в крови поддерживается в течение суток на постоянном уровне 3,5-6,0 ммоль/л. После приема пищи уровень глюкозы возрастает в течение часа до 8 ммоль/л, а затем возвращается к норме. В организме постоянный уровень глюкозы в крови поддерживается благодаря существованию нейрогуморальных механизмов. Основным показателем состояния углеводного обмена служит содержание глюкозы в крови и моче.
ГИПЕРГЛИКЕМИЯ- состояние, при котором уровень глюкозы выше нормы. Причины:
1. Физиологические - алиментарная, эмоциональная.
2. Патологические – сахарный диабет; стероидный диабет (Иценко-Кушинга) – гиперпродукция глюкокортикоидов коры надпочечников; гиперпродукция адреналина, глюкагона, СТГ тироксина.
ГИПОГЛИКЕМИЯ - состояние, при котором уровень глюкозы ниже нормы. Причины:
1. Сниженный выход глюкозы: заболевания печени, эндокринные заболевания (дефицит гормона роста, кортизола), наследственные метаболические нарушения (дефицит гликогенсинтетазы, галактоземия, непереносимость фруктозы, печеночные формы гликогенозов).
2. Увеличенная утилизации глюкозы: снижение запасов жиров (нарушение питания), нарушение окисления жирных кислот, гиперплазия β-кл. подж. железы, передозировка инсулина, болезнь Аддисона – гипопродукция глюкокортикоидов.
ГЛЮКОЗУРИЯ – появление сахара в моче. Если уровень глюкозы в крови составляет 8-10 ммоль/л, то нарушается
почечный порог для глюкозы и она появляется в моче. Причины:
1. физиологические:
- алиментарная глюкозурия
- глюкозурия беременных
- нейрогенная на почве стрессовых состояний
2. патологические:
- сахарный диабет
- острый панкреатит
- острые инфекционные заболевания
2.6. Сахарный диабет, биохимическая характеристика патогенеза.
Это заболевание, возникающее вследствие абсолютного или относительного дефицита инсулина.
Инсулин – единственный гормон, понижающий уровень глюкозы в крови. Механизм:
-повышает проницаемость клеточных мембран для глюкозы в клетках жировой и мышечной ткани, под его влиянием белки-транспортеры ГЛЮТ-4 перемешаются из цитоплазмы в мембрану клетки, где соединяются с глюкозой и транспортируют её во внутрь клетки;
-активирует гексокиназу, фруктокиназу, пируваткиназу (стимулирует гликолиз);
-активирует гликогенсинтетазу (стимулирует синтез гликогена);
-активирует дегидрогеназу пентозо-фосфатного пути;
-по механизму хронической регуляции является индуктором синтеза гексокиназы и репрессором синтеза ферментов глюконеогенеза (блокирует глюконеогенез);
-30% углеводов превращает в липиды;
-стимулирует ЦТК, активируя фермент синтетазу, которая катализирует реакцию взаимодействия ацетил-КоА с ЩУК;
Сахарный диабет (СД) классифицируют с учетом различия генетических факторов и клинического течения на две основные формы: диабет I типа – инсулинзависимый (ИЗСД), и диабет II типа – инсулиннезависимый (ИНСД).
ИЗСД – заболевание, вызванное разрушением β-клеток островков Лангерханса поджелудочной железы, вследствие аутоиммунных реакций, вирусных инфекций (вирус оспы, краснухи, кори, эпидемический паротит, аденовирус). При СД снижено соотношение инсулин/глюкагон. При этом ослабевает стимуляция процессов депонирования гликогена и жиров, и усиливается мобилизация энергоносителей. Печень, мышцы и жировая ткань даже после приема пищи функционируют в режиме постабсорбтивного состояния.
Гипергликемия – повышение конц. глюкозы в крови.
Она обусловлена снижением скорости использования глюкозы тканями вследствие недостатка инсулина или снижения биологического действия инсулина в тканях-мишенях. При дефиците инсулина уменьшается количество белков-переносчиков глюкозы (ГЛЮТ-4) на мембранах инсулинзависимых клеток (жировой ткани мышц). В мышцах и печени глюкоза не депонируется в виде гликогена. В жировой ткани уменьшается скорость синтеза и депонирования жиров. Активируется глюконеогенез из аминокислот, глицерола и лактата.
Глюкозурия – выделение глюкозы с мочой.
В норме проксимальные канальцы почек реабсорбируют всю глюкозу, если ее уровень не превышает 8,9 ммоль/л. Повышение концентрации глюкозы в крови превышает концентрационный почечный порог, что становится причиной появления ее в моче.
Кетонемия – повышение концентрации в крови кетоновых тел.
Жиры не депонируются, а ускоряется их катаболизм. Повышается концентрация неэтерифицированных жирных кислот, которые захватывает печень и окисляет их до ацетил – КоА. Ацетил-КоА превращается в β-гидроксимасляную и ацетоуксусную кислоты. В тканях происходит декарбоксилирование ацетоацетата до ацетона, поэтому от больных исходит его запах. Увеличение концентрации кетоновых тел в крови (выше 20 мг/л) приводит к кетонурии. Накопление кетоновых тел снижает буферную емкость крои и вызывает ацидоз.
Дефицит инсулина приводит к снижению скорости синтеза белков и усилению их распада. Это вызывает повышение концентрации аминокислот в крови, которые дезаминируются в печени. Образующийся при этом аммиак вступает в орнитиновый цикл, что приводит к увеличению концентрации мочевины в крови и моче – азотемия.
Полиурия – повышенное мочеотделение (3-4л в сутки и выше), т.к. глюкоза повышает осмотическое давление.
Полидипсия – постоянная жажда, сухость во рту, вследствие потери воды.
Полифагия – испытывают голод, часто едят, но теряют в массе тела, т.к. глюкоза не является источником энергии - «голод среди изобилия».
ИНСД – возникает в результате относительного дефицита инсулина вследствие:
- нарушения секреции инсулина
- нарушения превращения проинсулина в инсулин
- повышения катаболизма инсулина
-дефекта рецептора инсулина, повреждения внутриклеточных посредников инсулинового сигнала.
Поражает людей старше 40 лет, характеризуется высокой частотой семейных форм. Главная причина поздних осложнений сахарного диабета – гипергликемия, которая приводит к повреждению кровеносных сосудов и нарушению функций различных тканей и органов. Одним из основных механизмов повреждения тканей при сахарном диабете является гликозилирование белков, приводящее к изменению их конформации и функций. Макроангиопатии проявляются в поражении крупных и средних сосудов сердца, мозга, нижних конечностей (гангрена). Микроангиопатия является результатом повреждения капилляров и мелких сосудов и проявляется в форме нефро-, нейро- и ретинопатии. В возникновении микроангиопатий определенную роль играет гликозилирование белков, что приводит к возникновению нефропатии (нарушение функции почек) и ретинопатии (вплоть до потери зрения).
Коллаген составляет основу базальных мембран капилляров. Повышенное содержание гликозилированного коллагена ведет к уменьшению его эластичности, растворимости, к преждевременному старению, развитию контрактур. В почках такие изменения приводят к запустению клубочков и хронической почечной недостаточности.
Гликозилированные липопротеины, накапливаясь в сосудистой стенке, приводят к развитию гиперхолестеринемии и липидной инфильтрации. Они служат основой атером, происходит нарушение сосудистого тонуса, что приводит к атеросклерозу.
2.5. Проба на толерантность к глюкозе.
После приема пищи концентрация глюкозы может достигать 300-500 мг/дл и сохраняется на высоком уровне в постабсорбтивном периоде, т.е. снижается толерантность к глюкозе и наблюдается в случаях скрытой формы сахарного диабета. В этих случаях у людей отсутствуют клинические симптомы, характерные для СД, а концентрация глюкозы натощак соответствует норме.
Для выявления скрытой формы сахарного диабета проводится оральный тест на толерантность к глюкозе. Для этого определяют натощак содержание глюкозы в крови. После этого исследуемый получает нагрузку глюкозой из расчета 1г на кг массы, затем каждые 30 минут в течение 3-х часов определяют уровень глюкозы в крови. Результаты представляют в виде кривой.
 |
3. Лабораторно-практическиая работа:
3.1. Определение глюкозы в крови с помощью глюкометра One Touch ultra.
Определить содержание глюкозы натощак у студента. Проведение анализа. Подведите каплю крови на пальце руки к зоне теста на верхней части тест-полоски и удерживайте ее в таком положении до полного заполнения капилляра. На экране появляется отчет в течение 5 секунд, после чего обозначается величина уровня глюкозы в ммоль/л. После удаления тест-полоски изображение на экране прибора гаснет и он готов к следующему проведению анализа.
Ход работы: Вымойте руки теплой водой с мылом и тщательно высушите. Обработайте палец руки ватой, смоченной в этиловом спирте и подсушите его. Стерильным скарификатором проколите кожу пальца и выдавите из него капельку крови, которую введите в капилляр тест-полоски. Затем обработайте место прокола ватой, смоченной в этиловом спирте.
2. Дать выпить сладкий чай.
3. Определить содержание глюкозы через 30 минут с момента принятия нагрузки.
4. Определить содержание глюкозы через 2,5 часа с момента принятия нагрузки.
Не нашли, что искали? Воспользуйтесь поиском: