
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
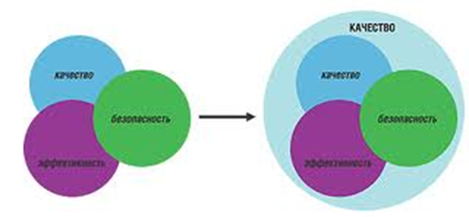
Основные требования к ЛС
Качество + эффективность + безопасность
Качество (фармацевтическое) – соответствие ЛС требованиям утвержденных нормативных документов по контролю качества.
эффективность – характеристика степени положительного влияния ЛС на предупреждение, течение или продолжительность заболевания, предотвращение беременности, восстановление нормальной жизнедеятельности организма человека и компенсацию его функциональных возможностей, нарушенных в результате заболевания.
безопасность – положительная характеристика ЛС, основанная на сравнительном анализе его эффективности и оценке риска причинения вреда жизни и здоровью человека.
Разработка ЛС
• Имеется 10180 возможных биологически активных веществ,
• 1018 вероятных лекарственных препаратов,
• 107 известных соединений,
• 106 коммерчески доступных соединений,
• 106 соединений в базах данных фирм,
• 104 соединений в базах данных по лекарствам,
• 103 коммерческих лекарств
• и 102 коммерчески выгодных лекарств.
Современный путь создания ЛС
• Идентификация мишени (заболевание)
• Потребности клиники, оценка врача
• Терапевтическая мишень
• Физиологическая мишень (система или орган)
• Молекулярная мишень (белок – рецептор, фермент и др.)
• Структура молекулярной мишени
• Оригинальное ЛС - ЛС, которое отличается от всех ранее зарегистрированных ЛС фармакологически активным веществом или комбинацией таких веществ.
Разработка оригинального ЛС

Путь к созданию ЛС
à Только у 1 из ~10.000 исследованных химических соединений удается обнаружить сопоставимые профили эффективности/безопасности.
à Процесс разработки и продвижения препарата на рынок требует затрат 2.000 человеко-часов и продолжается 12-15 лет.
à Если учесть, что патентование лекарства происходит после завершения доклинических испытаний (через 2 года), то на монопольное обращение на фарм. рынке остается 3-5 лет.
à Из 10 зарегистрированных инновационных лекарств только 1 приносит сверхприбыль, 8 – окупают затраты на производство и 1 – является убыточным.
à Затраты на разработку 1 инновационного (оригинального) ЛС составляют от 1 до 10 млрд. долл. США.

Основные этапы создания ЛС
• Этап 1. Поиск молекул-кандидатов:
• Источники:
• 1. Химический синтез (фармакологический скрининг, комбинаторная химия),
• 2. Направленный синтез (молекулярное конструирование),
• 3. Воспроизведение биогенных веществ и/или метаболитов,
• 4. Целенаправленная модификация молекул с уже известной активностью,
• 5. Случайность («серендипи»),
• 6. Изучение и выделение низкомолекулярных БАВ (монокомпоненты или смеси) из растительного, животного сырья, минеральных источников,
• 7. Микробиологический синтез,
• 8. Модификация биомолекул (средства для генной терапии, моноклональные антитела).

Химический синтез
• Метод поиска веществ с определенным типом фармакологической активности среди множества химических соединений, синтезированных химиками по специальному заказу.
• Впервые фармакологический скрининг применил немецкий ученый Домагк, который работал в химическом концерне IG-FI и проводил поиск антимикробных средств среди сульфаниловых красителей. У одного из этих красителей – красного стрептоцида - было обнаружено противомикробное действие. Так были открыты сульфаниламидные средства. Пауль Эрлих, при поиске противосифилитических средств изучил около 1000 органических соединений мышьяка и висмута и только 606-й препарат – сальварсан, оказался достаточно эффективным.
• В настоящее время, для проведения скрининга необходимо синтезировать не менее 10.000 исходных соединений, чтобы с большей долей уверенности полагать, что среди них имеется одно (!) потенциально эффективное лекарственное средство.
Не нашли, что искали? Воспользуйтесь поиском: