
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Наиболее вероятная скорость молекул — это скорость, вблизи которой на единичный интервал скоростей приходится наибольшее число молекул

данная формула вытекает из распределения Максвелла. Наиболее вероятная скорость, как показал он, зависит от температуры газа и массы молекул
Что бы получить из первой формулы скорости молекулы вторую, надо сделать всего две замены, расписать универсальную газовую постоянную, как  , и молярную массу
, и молярную массу  , то у нас получится из этой формулы:
, то у нас получится из этой формулы:

Вот такая вот формула:
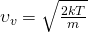
В Формуле мы использовали:
 — Наиболее вероятная скорость молекул
— Наиболее вероятная скорость молекул
 — Постоянная Больцмана
— Постоянная Больцмана
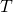 — Температура
— Температура
 — Масса одной молекулы
— Масса одной молекулы
 — Универсальная газовая постоянная
— Универсальная газовая постоянная
 — Молярная масса
— Молярная масса
 — Количество вещества
— Количество вещества
 — Число Авогадро
— Число Авогадро
Средняя скорость молекулы < v > (средняя арифметическая скорость) определяется по формуле
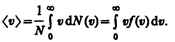
Подставляя сюда f(v) и интегрируя, получаем
 (44.3)
(44.3)
Скорости, характеризующие состояние газа: 1) наиболее вероятная  2) средняя
2) средняя  3) средняя квадратичная
3) средняя квадратичная  (рис. 65). Исходя из распределения молекул по скоростям
(рис. 65). Исходя из распределения молекул по скоростям
 (44.4)
(44.4)
можно найти распределение молекул газа по значениям кинетической энергии e. Для этого перейдем от переменной v к переменной e =m 0 v 2 / 2. Подставив в (44.4) v=  и d v=
и d v=  d e, получим
d e, получим
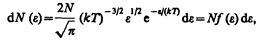
где d N (e) — число молекул, имеющих кинетическую энергию поступательного движения, заключенную в интервале от e до e + d e.
Таким образом, функция распределения молекул по энергиям теплового движения

Средняя кинетическая энергия < e > молекулы идеального газа
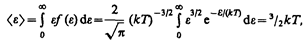
т. е. получили результат, совпадающий с формулой (43.8).
Не нашли, что искали? Воспользуйтесь поиском: