
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Другие физико-химические свойства. Рекомендуемая температура регенерации адсорбента – 250–300 oС.
Рекомендуемая температура регенерации адсорбента – 250–300 oС.
Важная положительная особенность оксида алюминия – его водостойкость. Он может применяться для осушки сред, в которых присутствует капельная влага. Увеличение водостойкости достигается за счет создания бидисперсной пористой структуры, в которой представлены крупные поры размером не менее 50 нм. Мелкопористые сорта оксида алюминия хуже устойчивы к капельной влаге.
При использовании адсорбента в жидких средах амфотерность оксида алюминия приводит к различной ионизации групп ОН- в зависимости от рН раствора. В кислой среде поверхность оксида алюминия будет заряжаться положительно, что приведет к адсорбции ионов противоположного знака. В этом случае оксид алюминия выступает в качестве адсорбента анионов. В щелочной среде оксид алюминия заряжается отрицательно, и в этом случае он адсорбирует катионы.
Ионообменные свойства оксида алюминия находятся в прямой связи с его текстурными характеристиками, а также с химической чистотой, поскольку содержащиеся в нем примеси могут привести к изменению его поверхности и смещению потенциала нулевого заряда.
Получение
Мировое производство оксида алюминия около 30 млн т/год (1980 г.).
γ-Al2O3 получают прокаливанием гиббсита и бемита, а η-А12О3 – прокаливанием байерита.
Сырье для получения оксида алюминия – бокситы, нефелины, алуниты и др. Все технологические схемы производства активного оксида алюминия основаны на получении гидроксида алюминия [1,19,23,24]. При соотношении в рудах А12О3/SiO2 > 6–7 их перерабатывают по способу Байера (основной метод), при Al2O3/SiO2 < 6 (высококремнистое сырье) – спеканием с известью и содой.
По способу Байера измельченный в шаровых мельницах боксит выщелачивают в автоклавах оборотным щелочным раствором алюмината натрия при 225–250 °С. При этом алюминий переходит в раствор в виде алюмината Na. Алюминатные растворы разбавляют водой, отделяют шлам и подвергают разложению в аппаратах с мешалкой или эрлифтом 30–70 ч, при этом выделяется около 1/2 образовавшегося А1(ОН)3, который фактически является гиббситом. Его отфильтровывают и прокаливают во вращающихся печах или в кипящем слое. Щелочной раствор регенерируют, концентрируют и используют для следующего растворения. Процесс ведут таким образом, чтобы получить легко фильтруемый (и прокаливаемый) продукт, поэтому получаемый гидроксид содержит кристаллиты более 20 мкм в диаметре.
По второму способу высококремнистую измельченную руду (нефелин и др.) смешивают с содой и известняком и спекают во вращающихся печах при 1250–1300 оС. Полученную массу выщелачивают водным щелочным раствором, раствор алюмината натрия отделяют от шлама, затем освобождают от SiO2, осаждая его в автоклаве при давлении около 0,6 МПа, а затем известью при атмосферном давлении, и разлагают алюминат газообразным СО2. Полученный А1(ОН)3 отделяют от раствора и прокаливают.
Оксид алюминия и алюмогели получают в результате термического разложения кристаллических модификаций тригидроксида алюминия, Al(OH)3 – гиббсита и байерита и метагидроксида алюминия, AlO(OH) – бемита. Эти процессы могут быть представлены следующей схемой:
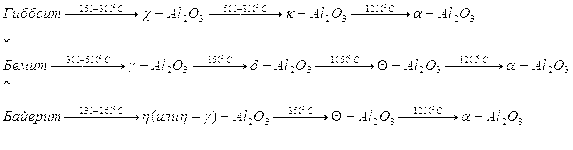 (11)
(11)
В ходе дегидратации происходит ряд последовательных превращений, во всех случаях окончательным продуктом дегидратации является корунд (α-Al2O3). Частичная дегидратация гидроксидов алюминия приводит к соединениям с общей формулой Al2O3. х H2O, где 0< х <1, которые, как правило, плохо окристаллизованы. Существует шесть основных фаз, обозначаемых греческими буквами: χ, κ, η, θ, δ, γ. Именно эти соединения используются в качестве адсорбентов, катализаторов и носителей катализаторов. Природа получаемого при прокаливании продукта зависит от природы исходного гидроксида (гиббсит, бемит и др.) и от условий его прокаливания (давления, среды, скорости нагревания, размера частиц).
1. Быстрое прокаливание. Термическое разложение гиббсита должно протекать по реакции:
2Al(OH)3 → Al2O3 + 3H2O, (12)
которая приводит к очень развитой поверхности, если ее проводят при
250 оС и выше. Однако вследствие крупных размеров кристаллитов промышленного гиббсита, внутри зерен создается высокое парциальное давление воды и существует возможность гидротермального процесса по уравнениям:
Al(OH)3 → AlO(OH) + H2O; (13)
Al2O3 + H2O → 2AlO(OH). (14)
Такое течение процесса приводит к образованию хорошо окристаллизованного бемита с низким значением удельной поверхности.
Прокаливание байерита короткими быстрыми импульсами ведет к развитию чрезвычайно большой поверхности и к получению очень реакционноспособного порошка. Реакции с образованием бемита в этих условиях не протекают.
2. Переосаждение технического гидроксида алюминия. Процесс заключается в растворении технического гидроксида алюминия в кислоте или щелочи с последующим осаждением гидроксида алюминия щелочью или кислотой.
Процесс можно описать следующими уравнениями:
Al(OH)3 + OH- →AlO2−+ 2H2O,
AlO2−+ H2O + H+ → Al(OH)3 . (15)
Гидроксид алюминия может образовывать объемистый гель, что дает возможность получать оксид алюминия с высокоразвитой поверхностью, высокой пористостью и относительно низкой плотностью. Гель-процесс является самым экономичным и дает возможность получать продукт довольно высокой чистоты.
За этой стадией следуют стадии осаждения-кристаллизации, промывания геля и гранулирования. Затем гранулы подвергают сушке и термической обработке.
В ходе прокаливания гидроксида алюминия можно проконтролировать размер агрегатов (путем контроля температуры), объем пустот между частицами остается примерно постоянным.
Адсорбенты с высокой удельной поверхностью и узким распределением пор по размерам получают при образовании и сохранении мелких и монодисперсных кристаллитов. Это достигается регулированием процессов зародышеобразования и кристаллизации и предотвращением нежелательных процессов в результате случайной гидротермальной обработки в ходе сушки.
Размер макропор можно регулировать размером кристаллитов исходного гидроксида, который изменяют в ходе кристаллизации или при помоле. Увеличение объема макропор достигается тремя способами: введением порообразователя, регулированием поверхностного натяжения в ходе сушки или гидротермальной обработкой.
Порообразователь (например, опилки, сажа, меласса и нефтяной кокс) вводится в еще несформованный продукт в количестве, достаточном для создания нужной системы макропор, для необратимого упрочнения структуры твердого тела вокруг порообразователя, а затем порообразователь удаляют путем выжигания. При этом остаются поры соответствующего размера.
Производство адсорбентов и носителей катализаторов нужных размеров, формы, вида и прочности, диктуемых требованиями процессов, где их применяют, осуществляется несколькими методами формования. Это методы дискового гранулирования, экструзии и формования в масле. Из всего объема оксида алюминия, используемого в адсорбционных и каталитических процессах, на долю перечисленных методов приходится соответственно 40, 50 и 10 %.
Метод дискового формования применяют в основном для получения адсорбентов или предшественников носителей катализаторов. Главное достоинство метода заключается в его высокой производительности, а следовательно, в относительно низкой стоимости гранул. Недостатком метода является образование гранул оксида алюминия разных размеров, что требует их последующего рассева. Экструзию применяют для формования алюмогелей, а также получения носителей катализаторов гидроочистки в процессах нефтепереработки. Алюмогели, полученные масляно-капельным методом, используют в качестве адсорбентов, когда процесс ведется под высоким давлением, а также в производстве регенерирующихся катализаторов для процессов, где от катализатора требуется высокая прочность. Преимущество масляно-капельного метода в образовании симметричных шариков одинакового размера. Однако этот метод дороже дискового формования.
Применение
По адсорбентам и катализаторам объем поставок оксида алюминия на мировой рынок составляет около 120 тыс. т/год [20]. Из этого количества 80–90 % оксида алюминия применяется в катализе.
В качестве адсорбента оксид алюминия используется главным образом для осушки газов (например, Н2, Аг, С2Н2) и жидкостей (ароматических углеводородов, керосина и др.), а также в хроматографии. Оксид алюминия обеспечивает глубокую осушку газов до остаточного содержания паров воды минус 60 оС по точке росы и ниже.
Недостатком оксида алюминия как осушителя является то, что он интенсифицирует полимеризацию непредельных углеводородов, образу-ющихся при крекинге в стадии высокотемпературной десорбции. Опыт промышленной эксплуатации оксида алюминия в процессах осушки олефинсодержащих потоков (этан-этиленовой фракции, пирогаза) на отечественных нефтехимических предприятиях показал [25], что в случае использования его в качестве осушителя происходит олигомеризация ценных углеводородов, обладающих высокой реакционной способностью (пропилена, бутиленов, бутадиена). Образование продуктов полиме-ризации в процессе регенерации адсорбента приводит к блокированию его сорбционного объема, вызывая снижение его адсорбционных свойств на 20 % уже в течение первого года использования. Это влечет за собой необходимость ежегодной перезагрузки адсорбента, а также значительные затруднения при выгрузке осушителя вследствие его слипания в монолитную глыбу. Однако возможность многократной регенерации путем выжига коксовых отложений обеспечивает долголетнюю работу адсорбента как осушителя олефинсодержащих потоков [1].
Для осушки применяются мелкопористые марки с удельной поверхностью 350–400 м2/г.
Важная область использования активного оксида алюминия − адсорбционная очистка масел, прежде всего транформаторных. Амфотерный характер Al2O3 делает его эффективным адсорбентом кислот, которые образуются при окислении масел. Накопление таких кислот снижает диэлектрические свойства масел.
С помощью оксида алюминия происходит улавливание паров НF из отходящих газов суперфосфатных и электролизных производств. Алюмогели используются для очистки воды с повышенным содержанием фтора, Al2O3 хемосорбирует F-ион из сточных вод.
В катализе выделяют три области употребления оксида алюминия: как носителя, активного катализатора и сокатализатора. Основная область использования – носитель каталитически активной фазы.
Главным промышленным процессом с его применением в качестве активного катализатора является процесс Клауса. Цель этого процесса – превращение сероводорода, содержащегося в некоторых природных газах или в газах нефтепереработки, в серу. Реакция Клауса протекает очень быстро на оксиде алюминия при 250 оС и лимитируется равновесным выходом серы:
H2S + ½ O2 → H2O + S. (16)
Эту реакцию проводят, употребляя дешевый сорт активированного оксида алюминия с высокой удельной поверхностью (~300 м2/г) и средней чистотой (~ 0,1 % Na), который получают при быстром прокаливании байерита.
Реакции гидролиза СОS и CS2 на Al2O3 протекают медленнее, чем реакция Клауса:
COS + H2O → CO2 + H2S; (17)
CS2 + H2O → CO2 +2 H2S. (18)
Они лимитируются активностью самого алюмооксидного катализатора. Обычно считается, что адсорбция Н2S, SO2, COS и CS2 на этом катализаторе происходит главным образом с участием основных центров (О2- или ОН).
Среди промышленных процессов, в которых применяется оксид алюминия как катализатор, следует также упомянуть дегидратацию спиртов и особенно этанола для получения этилена и других непредельных углеводородов (процесс вытеснен паровым крекингом углеводородов). При использовании Al2O3 как носителя и катализатора очень важна чистота продукта. Присутствие некоторых щелочных примесей в оксиде алюминия (Na, Ca и других) оказывает отрицательное воздействие на процесс.
Не нашли, что искали? Воспользуйтесь поиском: