
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Ядроның зарядын анықтау
 Резерфорд формуласын ядро зарядын өлшеу үшін қолдануға болады. Ол үшін dN және N шамаларын өлшеу керек. Осыдан кейін (1.7)формуладағы басқа қалған шамаларды α-бөлшектердің алтын фольгадан шашырауы белгілі деп санауға болатындықтан Z мәнін табуға болады. Резерфорд шәкірті Чедвиг (1920 ж.) ядро заряды мен элементтің периодтық жүйедегі реттік нөмірі арасындағы байланысты анықтау мақсатында тәжірибе жасады. Чэдвигтің тәжірибесінің схемасы 1.6-суретте келтірілген.
Резерфорд формуласын ядро зарядын өлшеу үшін қолдануға болады. Ол үшін dN және N шамаларын өлшеу керек. Осыдан кейін (1.7)формуладағы басқа қалған шамаларды α-бөлшектердің алтын фольгадан шашырауы белгілі деп санауға болатындықтан Z мәнін табуға болады. Резерфорд шәкірті Чедвиг (1920 ж.) ядро заряды мен элементтің периодтық жүйедегі реттік нөмірі арасындағы байланысты анықтау мақсатында тәжірибе жасады. Чэдвигтің тәжірибесінің схемасы 1.6-суретте келтірілген.
(1.6)Резерфорд формуласының дұрыстығы, оны қорытқанда пайдаланған негізгі ұйғарымдардың дұрыс болғандығын көрсетеді.
1.5. Атомның планетарлық моделінің классикалық физика көріністерімен үйлеспеуі
Ядро айналасында қозғалатын электрондардың центрге тартқыш үдеуі болатындықтан олар үздіксіз электромагниттік толқындар шығаруы тиіс. Сәуле шығарудан энергияның шығынға ұшырап, азаюы нәтижесінде электрондар орбитасының радиусы үдіксіз кішірейе беруге тиіс, ең соңында электрон ядроға құлауға тиіс, яғни классикалық физика тұрғысынан планетарлық модель түріндегі атом жалпы өмір сүре алмайды (1.7-сурет).
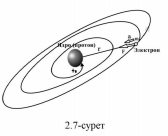 Классикалық физика тұрғысынан атом шығаратын сәуле жиілігі электрондардың айналу жиілігімен дәл келуге тиіс және осы негізгі жиілікке еселі жиіліктерде құрамында болуға тиіс. Сәуле спектрінің осындай сипаты атомдық спектрлерде байқалатын заңдылықтарға толық қарама-қайшы келеді.
Классикалық физика тұрғысынан атом шығаратын сәуле жиілігі электрондардың айналу жиілігімен дәл келуге тиіс және осы негізгі жиілікке еселі жиіліктерде құрамында болуға тиіс. Сәуле спектрінің осындай сипаты атомдық спектрлерде байқалатын заңдылықтарға толық қарама-қайшы келеді.
Сонымен бір жағынан Резерфорд тәжіибелері атомның планетарлық моделін растайды. Екінші жағынан бірқатар тағайындалған эксперименттік деректер мен заңдылықтарды атомның планетарлық моделіне сүйеніп және классикалық физика көріністерін пайдаланып түсіндіру мүмкін болмайды.
2-дәріс. Бордың кванттық теориясы. Бор постулаттары. Франк-Герц тәжірибелері. Сутегі атомының Бор ұсынған моделі. Сутегі атомының энергетикалық күйлері. Сутегі атомының спектрі. Спектрлік сызықтардың изотоптық ығысуы. Бор теориясының кемшіліктері.
Бор постулаттары
Атомның ядорлық (планетарлық) моделі классикалық физика заңдары тұрғысынан орнықсыз. Өйткені классикалық электродинамика заңдарына сәйкес:
1 Үдемелі қозғалатын зарядталған бөлшек (электрон) электромагниттік энергияны (жарық) үздіксіз шығаруға тиіс:
2 Осы жарықтың жиілігі электронның ядроны айналу жиілігіне тең болуы керек.
Демек, осы модельге сәйкес атомның тоық энергиясы үздіксіз кеми беруге, ал айналу жиілігі үздіксіз арта береуге тиіс. Осы жағдайда өте аз уақыт (~10⁻⁸е) ішінде электрон ядроға құлан,атом өзінің өмір сүруін тоқтататындығын есептеп, көз жеткізуге болады. Ал бұл барлық атомдардың өте қысқа уақыт ішінді қиратандығын көрсетеді. Бұған қоса, егер берілген модель дұрыс болса, онда сутегінің оптикалық спектрі (басқа элементтердің спектрі де) үздіксіз,тұтас болу керек. Осы екі қорытынды да тәжірбие деректеріне толығынан қарама-қайшы келеді. Шындығында атом өте орнықты жүйе болып табылады және қозбаған күйде жарық шығармайды, атом сызықтық оптикалық спектір береді. Сонымен, атомның ядорлық (планетарлық) моделі (классикалық механика және электродинамикамен қосылып) атомның орнықтылығын да атомдық спектірдің сызықтық сипатта болатынын да түсіндіре алмады.
Осы тұйыққа тірелуден шығу жолын 1913 ж Дания физигі Нильс Бор (1885-1962) тапты. Ол үшін оған классикалық физика түсініктеріне қайшы келетін жоромалдар енгізуге тура келді. Бор өзінің жорамалдарын екі постулат түрінде ұсынды:
1. Классикалық механика тұрғысынан атомда мүмкін болатын шексіз көп электрон орбиталары ішінен, шындығында mυr nћ (n=1,2,3…) белгілі кванттық шарттарды қанағаттандыратын тек кейбір дискретті орбиталар іске асады. Электрон осы станционарлык орбиталардың күйдегі энергиясының дискретті мәндері (Е1,Е2,Е3,...) болады.
2. Электрон бір стационарлық күйден екінші стационарлық күйге көшкенде ғана жарық энергиясы ћw кванттары түрінде шығарылады немесе жұтылады.
Жарық квантының шамасы араларында электрон кванттык көшу жасайтын стайионарлық күйлер энергияларының айырмасына тең:
ћω = En - Em (2.1)
Осы теңдік Бордың жиіліктер ережесі деп аталады. Сонымен атом стационарлық бір күйден басқа екінші күйге секірмелі түрде ауысады. Бұлар кванттык көшулер деп аталад. Мысалы,егер электрон n= 5 орбитадан (стационарлық күйден) n= 4 орбитаға өткен болса, онда жиілігі ω = (E4– E5) / ћ фотон шығарылады (бұл шығару спектірінің дискреттік сипатын түсіндіреді). Ал егер энергиясы ћω = E4– E5 фотон атоммен соқтығысса, онда-ол жұтылуы мүмкін. Сонда электрон n= 4 орбитадан n= 5 орбитаға көшеді. Жұтылу спектірінің пайда болу механизмі осындай. (2.1) Бордың жиліктер ережесі Ридберг-Ритцтің комбинациялық принципін түсіндіруге мүмкіндіг береді. Осы принципке сәкес спекторскопияяда спектірлік сызықтардың  = 1/λ толқындық сандары T(n) термдер депаталатын оң таңбалы сандар айырмасы түрінде бейнеленеді:
= 1/λ толқындық сандары T(n) термдер депаталатын оң таңбалы сандар айырмасы түрінде бейнеленеді:
 =
=  = T(m) - T(n), n m (2.2)
= T(m) - T(n), n m (2.2)
Спектроскопиялық толқындық сан үшін Бордың (2.1) жиіліктер ережесі мына түрде жазылады:
 (2.3)
(2.3)
(2.3) және (2.2) теңдіктерін салыстырып, терм атомның стационарлық күйдегі энергиясына тура пропорционал екендігін көруге болады:
 (2.4)
(2.4)
Сөйтіп спектірлік термнің физикалық мағынасы түсінікті болды. Атомның стацонарлық күйлердінің Е1, Е2, Е3, … энергия мәндерінің жиынтығы атомның энергетикалық спектірін түзеді. Сонымен терм атомның энергия деңгейлерімен анықталады.
Не нашли, что искали? Воспользуйтесь поиском: