
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Методы синтеза полифениленов с образованием нового бензольного кольца.
Вторым основным направлением синтеза ПФ является метод полициклоконденсации (ПЦК), основанный на образовании нового бензольного кольца в процессе формирования макромолекулярной цепи.
К этому направлению относится получение ПФ по реакции Дильса-Альдера на основе бис -тетрациклонов (бис -тетрафенилциклопентадиенонов) и ароматических диэтинильных соединений (бис -толанов) [46-48, 186, 187], где в результате поликонденсации образуются новые, пента- или гексафенилзамещенные бензольные кольца (схема 13).
Схема 13.
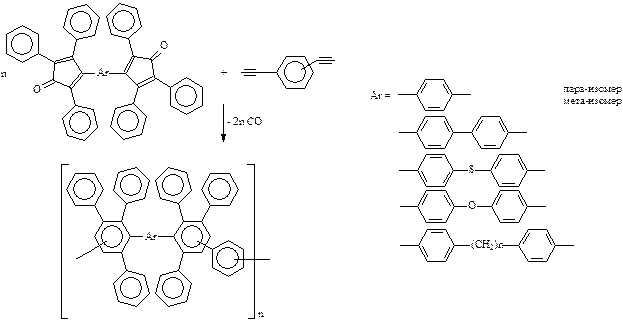
В работе [47] была изучена реакция Дильса-Альдера между 1,4- бис -(2,4,5-трифенилциклопентадиенон-3-ил)бензолом и 1,4-диэтинилбензолом (схема 14). Полимеробразующая реакция была проведена с использованием различных концентраций мономеров и различного времени реакции. Молекулярные массы (Mw) синтезированных разветвленных ПФ находятся в интервале 12000-120000.
Схема 14.

Для планаризации гексафенилзамещённого бензольного кольца полученный полимер (или модельное соединение) подвергался окислительному внутримолекулярному циклодегидрированию c образованием полициклических ароматических углеводородов (схема 15).
Однако такой ПФ сразу терял растворимость. Для придания ему растворимости на периферию планаризованного кольца на стадии синтеза мономеров вводили длинные алифатические заместители.
Схема 15.
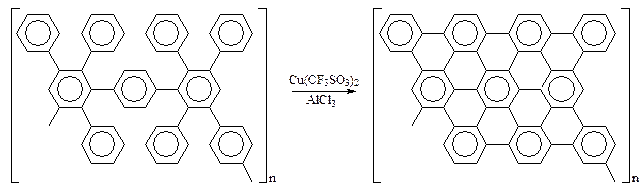
Перспективным методом синтеза ПФ с образованием нового бензольного кольца является метод, предложенный в ИНЭОС РАН В.В. Коршаком, М.М. Тепляковым и В.А. Сергеевым [51-55] и основанный на конденсации ацетилароматических соединений.
В процессе конденсации образуются растворимые полимеры, которые легко перерабатываются, давая при нагревании за счёт конденсации концевых ацетильных групп и дефектных β-метилхалконовых (дипноновых) фрагментов трехмерные тепло- и термостойкие полимеры [53, 55].
Образование ПФ из ацетилароматических соединений представляет собой реакцию тримеризационной полициклоконденсации (ПЦК), общие закономерности которой рассмотрены в литературе [59]. Эта реакция во многом сходна с процессами полициклотримеризации этинильных, нитрильных, цианамидных и других мономеров [56-58]. Рост цепи ПФ в случае циклоконденсации ацетилароматических соединений осуществляется за счет взаимодействия трех ацетильных или кетальных групп с образованием нового бензольного кольца и сопровождается выделением воды и спирта. На определенном этапе реакция заканчивается образованием геля, поэтому условия синтеза варьируют в зависимости от того растворимый или нерастворимый полимер хотят получить.
Таким образом использование ди- и моноацетилароматических соединений в условиях ПЦК позволило разработать в лаборатории высокомолекулярных соединений ИНЭОС РАН новый метод синтеза ПФ [51, 77], в основе которого лежит известная в органической химии реакция циклоконденсации ацетона [60], ацетофенона [61] и других метиларил- или метилалкилкетонов [62, 63] в присутствии кислотных катализаторов. (H2SO4, ZnCl2, AlCl3, сухой HCl и др.).
М.М. Тепляковым и сотрудниками [51, 53, 55] было предложено проводить ПЦК моно- и диацетилариленов в присутствии триэтилортоформиата (ортомуравьиного эфира) при пропускании сухого хлористого водорода в качестве катализатора в растворе бензола при комнатной температуре.
При условии равной реакционной способности функциональных групп и без учета побочных реакций ПЦК с образованием ПФ можно представить схемой 16.
Схема 16.

Протекание побочных реакций связано, главным образом, с неполной циклизацией, а также отсутствием равной реакционной способности двух ацетильных групп мономеров. Реальные полимеры имеют в незначительной степени разветвленную цепь и высокую степень полидисперсности: отношение `Mw/Mn составляет 6,8 – 9,9 [51]. Кроме того, наряду с образованием 1,3,5-замещенных бензольных колец, в цепи полимера образуются дипноновые фрагменты – продукты неполной циклизации ацетильных групп. Физико-химические исследования ПФ показали, что в цепи с n = 7 – 8 содержится около двух дипноновых фрагментов [64, 67].
Так как с ростом молекулярной массы увеличивается вероятность образования нерастворимых продуктов, реакцию ПЦК в растворе заканчивали на стадии форполифениленов с относительно невысокой молекулярной массой и остаточными концевыми ацетильными группами [55]. Такие полимеры с `Mn = 1500 – 4000 и hпр = 0,10 – 0,15 дл/г растворимы в хлороформе, бензоле, диоксане, ДМФА и др. Было использовано эквимолярное или близкое к нему соотношение ди- и монофункциональных исходных мономеров. В случае уменьшения содержания моноацетиларилена быстро образуется нерастворимый полимер. При избытке моноацетиларилена увеличивается степень обрыва растущей цепи и форполимер имеет малое количество концевых групп.
Схема элементарного акта образования ПФ может быть представлена следующим образом (схема 17) [65]:
Схема 17.

На второй стадии полимер за счет дальнейшей конденсации концевых групп при нагревании превращается в конечный трехмерный полимер. Конденсация концевых ацетильных групп полимера происходит при 450оС за 1 час, а при 300оС – за 5 часов. В присутствии 10% п -толуолсульфокислоты или другого кислотного катализатора этот процесс заметно ускоряется и при 300оС в течение 1 часа выход гель-фракции близок к количественному.
Двухстадийное проведение процесса позволяет осуществить на второй стадии переработку полимеров в изделия. Конечные полимеры обладают высокой тепло- и термостойкостью. Так, образцы, отпрессованные при 350оС с последующим прогревом при 450 – 500оС, при испытаниях на плоскостном пластометре деформируются не более чем на 10% при нагревании до 500оС [55]. По данным динамического ТГА в инертной атмосфере, полимер, отвержденный при 350 – 400оС, теряет 30% массы при нагревании до 900о, а на воздухе полимер начинает терять массу при 500оС.
Разновидностью метода синтеза ПФ из ацетилароматических соединений является синтез таких полимеров из их кеталей (схема 18) [51, 65, 66, 68, 69, 70, 72].
Схема 18.
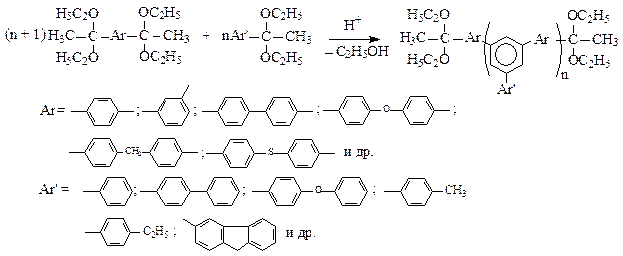
При этом предполагалось, что использование кеталей позволяет проводить процесс ПЦК более специфично и с образованием менее дефектных структур. Для выяснения условий синтеза ПФ было проведено изучение процесса ПЦК на модельных реакциях кеталей ацетилароматических соединений и предложен следующий механизм (схема 19).
Суммируя данные по исследованиям циклоконденсации кеталей метиларилкетонов, в работе [51] делается вывод о том, что оптимальными условиями процесса ПЦК кеталей является проведение реакции, катализируемой HCl, в неполярных ароматических растворителях, при начальной концентрации кетальных групп - 1 г-экв/л и температуре 15 – 20оС.
Если в реакции ПЦК использовали только дифункциональный мономер, например, кеталь п -диацетилбензола [66, 68], то уже на первой стадии начинается ветвление полимера, которое и приводит к быстрому образованию трехмерного полимера. Реакцию ветвления можно замедлить путем блокирования части функциональных групп, вводя монофункциональный мономер, например, кеталь ацетофенона, уже в процессе реакции. В отличие от одновременного введения ди- и монофункциональных мономеров, в данном случае получали более
Схема 19.

разветвленный полимер. При увеличении доли кеталя ацетофенона, уменьшается скорость гелеобразования и выход гель-фракции. Когда соотношение моно- и дифункциональных компонентов составляет 2 моля на 1 моль соответственно, то значительно уменьшается скорость гелеобразования и увеличивается доля растворимой фракции. При дальнейшем увеличении содержания блокирующего агента, образования геля не наблюдается. При этом снижается молекулярная масса полимера и количество концевых ацетильных групп, что нежелательно для последующей стадии отверждения.
Следует отметить зависимость скорости гелеобразования при ПЦК кеталей ди- и моноацетилароматических соединений от количества катализатора HCl. Найдено [51], что с увеличением скорости подачи газообразного HCl уменьшается продолжительность синтеза, т.е. сокращается время достижения точки гелеобразования. Таким образом, дозировкой катализатора можно регулировать процесс синтеза. В работе [51] показано, что практически одинаковый выход полимера может быть достигнут при пропускании определенного количества газообразного HCl через реакционный раствор или при предварительном насыщении реакционного раствора этим же количеством катализатора. Основным недостатком использования газообразного HCl в качестве катализатора является невозможность его точного дозирования и обусловленная этим неоднозначность процесса синтеза.
В работах [71, 73] с целью выяснения характера процесса ПЦК проведено термодинамическое изучение реакции синтеза ПФ на основе кеталя ацетофенона и кеталя п -диацетилбензола. Процессы образования полимера из мономера путем ПЦК в растворе и формирования трехмерного полимера при нагревании полимера термодинамически разрешены и их равновесие сдвинуто практически полностью в сторону образования соответствующего полимера. Так, при 25оС константы равновесия равны 1,5 . 1024 и 1,35 . 105 соответственно, то есть ПЦК кеталей является неравновесным процессом, т.к. константы равновесия превышают 103 [74].
В работах [64, 67, 69] показано, что ПФ, полученные на основе кеталей, содержат меньше дефектных структур, чем получаемые из исходных ацетилсодержащих мономеров в присутствии кетализирующего агента – ортомуравьиного эфира. Однако наличие дефектных b-метилхалконовых (дипноновых) фрагментов, образующихся при неполной циклизации ацетильных групп, не сказывается существенным образом на термических свойствах конечных структур [51].
Следует отметить, что синтез и хранение кеталей ацетильных соединений представляет довольно сложную проблему, поэтому синтез полимеров из ацетилароматических соединений является предпочтительным с технологической точки зрения.
Полимеры, синтезированные как из ацетильных соединений, так и из кеталей, обладают хорошей растворимостью на стадии форполимеров и, как правило, высокой теплостойкостью как на стадии форполимеров, так и на стадии конечных сшитых полимеров, причем термическая устойчивость последних находится на уровне п -ПФ, одного из наиболее термостойких полимеров [76].
Таким образом, имеющиеся в литературе сведения позволяют сделать вывод о том, что дальнейшее развитие реакции ПЦК моно- и диацетилариленов является перспективным, т.к. может приводить как к растворимым, так и нерастворимым ПФ. Последние в свою очередь могут использоваться в качестве матриц для иммобилизации катализатора и проведения гетерогенных каталитических реакций.
2. КАТАЛИЗ РЕАКЦИЙ КРОСС-СОЧЕТАНИЯ С ИСПОЛЬЗОВАНИЕМ N-ГЕТЕРОЦИКЛИЧЕСКИХ КАРБЕНОВЫХ ЛИГАНДОВ.
Палладий-катализируемые реакции образования связей С-С и С-гетероатом находятся в числе наиболее универсальных синтетических методов. Число коммерчески доступных, стабильных и удобных катализаторов кросс-сочетания постоянно увеличивается. Среди них N-гетероциклические карбены пользуются повышенной популярностью как лиганды в Pd-катализируемом кросс-сочетании и сходных реакциях, поскольку их характеристики превосходят классические третичные фосфины. Высокая σ–электронодонорная способность N-гетероциклических карбеновых лигандов является причиной быстрого окислительного присоединения различных субстратов, в то время как стерически объёмные заместители и строение молекулы способствуют быстрому восстановительному элиминированию. Прочность связи Pd-С в комплексах N-гетероциклических карбеновых лигандов приводит к высокой стабильности активных частиц даже при низком соотношении лиганд/Pd и высоких температурах.
В самом обобщённом представлении карбены - неустойчивые органические соединения, содержащие электронейтральный двухвалентный атом углерода (R'R"C:). Карбены являются промежуточными частицами во многих органических реакциях [184]. Так, простейший карбен - метилен (: CH2) образуется при термическом или фотохимическом разложении диазометана или кетена, например:
CH2N2 →: CH2 + N2.
Аналогично могут быть получены и другие карбены. Дигалогенкарбены возникают при термическом разложении щелочных солей тригалогенуксусных кислот:
CCl3COONa →: CCl2 + NaCl + CO2.
Карбены стабилизируются различными путями в зависимости от условий образования и природы взаимодействующих с ними соединений. Например, они могут димеризоваться:: CH2 +: CH2 → CH2 = CH2; внедряться по связи углерод — водород, например в углеводороды R — Н +: СН2 → R — CH3; присоединяться по кратной связи (например, к этилену) с образованием трёхчленного цикла:
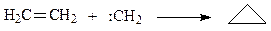
Последнюю реакцию широко применяют для синтеза различных трёхчленных циклических соединений.
N-гетероциклические карбены, впервые полученные независимо Ванзликом (Wanzlick) и Шёнхерром (Schönherr) [78] и Йофеле (Öfele) [79] в 1968 году, не привлекали внимания химиков до 1991 года, когда Ардуенго (Arduengo) с сотр. впервые получили стабильный кристаллический N-гетероциклический карбен (IAd) (табл. 1) [80]. Наряду с ним, были синтезированы менее устойчивые гетероциклические карбены на основе имидазола и 4,5-дигидроимидазола с мезитиленовыми и фенилдиизопропильными группами (табл. 1).
Таблица 1.
N-гетероциклические карбены.
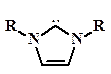
| |
| R 2,4,6-триметилфенил 2,6-диизопропилфенил 4-метилфенил 2,6-диметилфенил циклогексил адамантил | L IMes IPr ITol IXy ICy IAd |

| |
| 2,4,6-триметилфенил 2,6-диизопропилфенил циклогексил | SIMes SIPr SICy |
Потенциал этого класса соединений в качестве лигандов в комплексах переходных металлов был признан только в 1995 году. После появления работы Херрманна (Herrmann) и др. [81], N-гетероциклические карбеновые лиганды начали использовать в катализе. Работы в этой области привели к созданию целого ряда других подходов к синтезу N-гетероциклических карбенов (схема 20) [82] и соответствующих комплексов переходных металлов на их основе.
Схема 20.

Однако, на сегодняшний день широкое применение в гомо- и гетерогенном катализе находят комплексы с лигандами, полученными из имидазола или солей 4,5-дигидроимидазола. Наиболее важным примером перспективности данного класса катализаторов является катализ реакции метатезиса комплексами рутения, разработанный Граббсом (Grubbs) и его коллегами. Данная работа была удостоена Нобелевской премии. В условиях катализа замена одного из двух трициклогексилфосфиновых лигандов в I поколении катализаторов Граббса на объемный карбен SIMes привела к увеличению стабильности и активности субстрата в последующих поколениях [83].
Палладий является одним из переходных металлов, способных катализировать широкий спектр органических реакций [84], в частности, C-C и C-гетероатом кросс-сочетание. Использование объёмных карбенов, в частности IPr и SIPr, в качестве лигандов привело к значительному улучшению каталитических показателей по сравнению с наиболее традиционными фосфиновыми лигандами. С тех пор появилось большое число работ, посвященных исследованию химии N-гетероциклических карбенов, написанных Херманном и Кочером (Köcher) [85, 86], а также Бертраном (Bertrand) и сотр. [87], и многие другие обзоры, касающиеся отдельных аспектов этой области, например, хиральных N-гетероциклических карбенов [88, 89], структуры, образования связей и реакционной способности свободных N-гетероциклических карбенов [90], а также N-гетероциклических карбеновых комплексов переходных металлов [91-96]. Ранние работы в химии комплексов N-гетероциклических карбеновых лигандов, особенно направленные на реакции кросс-сочетания, были обобщены Херрманном в 2003 году [97].
Согласно проведённому анализу экспериментальных данных [97], преимущества использования N-гетероциклических карбенов как лигандов в Pd-катализируемых реакциях состоят в следующем: 1) высокая σ-донорная способность N-гетероциклических карбенов приводит к способности палладиевого центра к окислительному присоединению по связям, традиционно считавшимися стойкими, например, в хлораренах [98] или алкилированных галогенидах [99, 100]; 2) стерически объёмные N-гетероциклические карбены облегчают восстановительное элиминирование, подобно стерически затруднённым фосфинам [101, 102]; 3) прочность связи Pd-лиганд служит гарантом, что металл находится в координациинной сфере лигандов, т.е. в каталитически активном состоянии, даже в случае присоединения одного лиганда. Как следствие особых свойств комплексообразования N-гетероциклических карбенов с Pd, комплексы являются устойчивыми, легко синтезируются, в условиях реакции демонстрируют явные преимущества перед катализаторами, сформированными in situ. Идеально, такие катализаторы должны быть получены из соответствующих солей имидазола, избегая выделения высокочувствительного к влаге и воздуху карбена. На сегодняшний день существует 2 основных принципа использования N-гетероциклических карбенов в качестве лигандов в реакциях кросс-сочетания:
1) в виде готовых комплексов лиганд-Pd0 или лиганд-PdII.
2) в виде солей N-метилимидазола и различных источников палладия (чаще, соли палладия). При этом образование комплекса происходит в общей реакционной массе непосредственно перед началом реакции – in situ.
Не нашли, что искали? Воспользуйтесь поиском: