
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Энтропия , ее статистический смысл.
Макросостояние – это состояние вещества, характеризуемое его термодинамическими параметрами.
Состояние же системы, характеризуемое состоянием каждой входящей в систему молекулы, называют микросостоянием.
Термодинамической вероятностью или статистическим весом макросостояния W - называется число микросостояний, осуществляющих данное макросостояние (или число перестановок одноименных элементов, при которых сохраняется данное макросостояние).
Термодинамическая вероятность W - максимальна, когда система находится в равновесном состоянии.
В состоянии равновесия и термодинамическая вероятность максимальна, и энтропия максимальна. Из этого можно сделать вывод, что между ними существует связь.
Энтропия S – аддитивная величина:  , где
, где 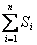 - сумма энтропий тел, входящих в систему.
- сумма энтропий тел, входящих в систему.
Вероятность сложного события, есть произведение вероятностей состояний:
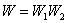 , ,
|
где W 1 – первое состояние; W 2 – второе состояние.
Аддитивной величиной является логарифм термодинамической вероятности:
 . .
|
Поэтому Л. Больцман предложил:
 , ,
| (6.7.1) |
где k – коэффициент Больцмана. С этой точки зрения энтропия выступает, как мера беспорядочности, хаотичности состояния.
Связь между S и W позволяет несколько иначе сформулировать второе начало термодинамики: наиболее вероятным изменением энтропии является ее возрастание.
Энтропия – вероятностная статистическая величина. Утверждение о возрастании энтропии потеряло свою категоричность. Её увеличение вероятно, но не исключаются флуктуации.
На основе этих рассуждений Р. Клаузиус в 1867 г. и выдвинул гипотезу о тепловой смерти Вселенной (о ней сказано ранее).
Л. Больцман один из первых опроверг эту гипотезу и показал, что закон возрастания энтропии – статистический закон, т.е. возможны отклонения.
Энтропия замкнутой системы – максимальна, при достижении системой равновесного состояния.
56. Расчет энтропии идеального газа в изопроцессах:
Энтропия системы является функцией ее состояния, определенная с точностью до произвольной постоянной.
Если система совершает равновесный переход из состояния 1 в состояние 2, то изменение энтропии
 . .
| (6.2.1) |
Таким образом, по формуле (6.2.1) можно определить энтропию лишь с точностью до аддитивной постоянной, т.е. начало энтропии произвольно. Физический смысл имеет лишь разность энтропий.
изменения энтропии в процессах идеального газа.
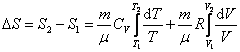 , или , или
|
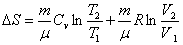 . .
| (6.2.2) |
Таким образом, изменение энтропии ΔS1-2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида перехода 1 - 2.
Каждый из изопроцессов идеального газа характеризуется своим изменением энтропии, а именно:
- изохорический:
 , т.к.
, т.к.  ;
; - изобарический:
 т.к. Р1 = Р2;
т.к. Р1 = Р2; - изотермический:
 т.к.
т.к. 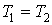 ;
; - адиабатический:
 , т.к.
, т.к. 
Отметим, что в последнем случае адиабатический процесс называют изоэнтропийным процессом, т.к.  .
.
Не нашли, что искали? Воспользуйтесь поиском: