
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Лабораторная работа № 4. Тема: «Выявление ионов железа (II), (III) и алюминия»
Тема: «Выявление ионов железа (II), (III) и алюминия»
Основные теоретические положения:
Одним из важнейших соединений алюминия является гидроксид алюминия Аl(ОН)3, Его получают при взаимодействии раствора щелочи с растворами солей алюминия (раствор щелочи нельзя брать в избытке):

Аl (ОН)3 представляет собой белую желеобразную массу и обладает (как и его оксид) амфотерными свойствами. Обратите внимание - как основа гидроксид алюминия реагирует с кислотами, но со щелочами в водных растворах образует гидроксо - алюминаты:

То есть Аl(ОН)3 обладает амфотерными! свойствами.
По распространенности среди металлов железо занимает второе место после алюминия. Наиболее распространены соединения железа со степенями окисления +2 и +3, С кислородом железо образует два оксида: оксид железа (II) FеO, оксид железа (lll)Fe2 О3. Оксидам железа отвечают соответственно гидроксид железа (II) Fe(ОН)2 и гидроксид железа (III) Fe(OH)3. Эти основания не растворимы в воде, их можно получить при взаимодействии солей железа (II) и солей железа (III) с растворами щелочи. В ионном виде уравнения реакции имеют вид:
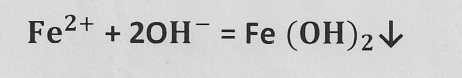
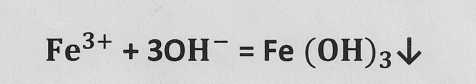
Из солей железа (II) и железа (III) практическое значение и применение имеют две комплексные соли: желтая К4[Fе(СN)6] и красная К3[Fе(СN)6] кровяные соли.
Первая соль - чувствительный реактив на ионе Fe3+ (соли трехвалентного железа); вторая - на иноны Fе2+ (соли двухвалентного железа). При взаимодействии солей трехвалентного железа с желтой кровяной солью образуется комплексная соль, раствор окрашивается в сине - голубой цвет (берлинская лазурь);

При взаимодействии солей железа (II) с красной кровяной солью раствор окрашивается в синий цвет, образуется турбнулева синь.

Указанные в квадратных скобках анионы НЕ диссоциируют на ионы.
Два последних уравнения - напоминание вам о понятии «качественная реакция».
Не нашли, что искали? Воспользуйтесь поиском: