
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Негистоновые белки хроматина 2 страница
Реакции с участием карбонильной группы. Линейная форма в кристаллических препаратах моносахаридов и их растворах присутствует в незначительных количествах, но ее участие в таутомерном равновесии обеспечивает моносахаридам все свойства, присущие альдегидам (в альдозах) или кетонам (в кетозах). Способность альдоз и кетоз присоединять спирты представлена ранее. Рассмотрим некоторые другие их свойства.
Окисление моносахаридов. Обработка альдоз слабыми окислителями приводит к превращению альдегидной группы в положении атома С-1 в карбоксильную группу с образованием так называемых альдоновых кислот. Альдоновой кислотой может быть D-глюконовая кислота, которая образуется при окислении альдегидной группы D-глюкозы. Фосфорилированная форма D-глюконовой кислоты играет важную роль в качестве промежуточного продукта углеводного обмена. Другой пример – D-галактоновая кислота – продукт окисления альдегидной группы D-галактозы.


D-глюконовая к-та D-галактоновая к-та
В альдуроновых, или уроновых, кислотах окислена (с образованием карбоксильной группы) первичная спиртовая группа, а альдегидная группа остается неокисленной. Уроновая кислота, образующаяся из D-глюкозы, носит название D-глюкуроновой кислоты, а образующаяся из D-галактозы – D-галактоуроновой кислоты. Уроновые кислоты весьма важны в биологическом отношении, многие из них являются компонентами полисахаридов.


D-глюкуроновая к-та D-галактоуроновая к-та
Восстановление моносахаридов. Моносахариды легко гидрируются по связи С—О и при этом превращаются в многоатомные спирты (сахароспирты). D-глюкоза, например, образует спирт сорбит, а D-манноза – маннит. Восстановление D-фруктозы приводит к эквимолекулярной смеси эпимеров – D-маннита и D-copбита, так как в результате гидрирования второй атом углерода становится асимметричным. Такого рода восстановление может осуществляться и ферментативным путем.
71. Охарактеризуйте производные моносахаридов: аминосахара, кислоты, гликозиды. Приведите примеры и напишите формулы.
Продуктами реакции замещения полуацетального гидроксила другими группировками в реакциях со спиртами, карбоновыми кислотами,фенолами называются гликозиды.
Соответственно α- и β-изомерам моносахаридов существуют α- и β-глюкозиды. Например, при реакции метилового спирта с глюкозой (допустим, в β-пиранозной форме) в присутствии неорганических кислот образуется продукт алкилирования метил-β-D-глюкопиранозид:
СH3OH H2O

b-D-глюкопираноза Метил-b-D-глюкопиранозид
При действии на β-D-глюкопиранозу уксусной кислотой образуется продукт ацилирования ацетил-β-D-глюкопиранозид (по той же схеме).
Важным классом гликозидов являются N-гликозиды, в которых гликозидная связь осуществляется через азот, а не через кислород *. N-гликозиды рассматривают как производные моносахаридов, у которых гликозидная часть молекулы связана через атом азота с радикалом органического соединения R, не являющегося углеводом. Как и О-гликозиды, N-гликозиды могут быть построены как пиранозиды или как фуранозиды и иметь α- и β-форму:


N-гликозид (a-форма) N-гликозид b-форма
Обработка альдоз слабыми окислителями приводит к превращению альдегидной группы в положении атома С-1 в карбоксильную группу с образованием так называемых альдоновых кислот.


D-глюконовая к-та D-галактоновая к-та


D-глюкуроновая к-та D-галактоуроновая к-та
Аминосахара. Это производные моносахаридов, гидроксильная группа которых —ОН замещена аминогруппой —NH2. В зависимости от положения аминогруппы (при атомах углерода) в молекуле аминосахара различают 2-амино-, 3-амино- и 4-аминосахара и т.д. По числу аминогрупп выделяют моноаминосахара и диаминосахара. Аминосахара обладают всеми свойствами аминов, обычных моносахаров, а также специфическими свойствами, обусловленными пространственной близостью гидроксильных и аминных групп. В организме человека и животных наиболее важными аминосахарами являются D-глюкозамин и D-галактозамин:
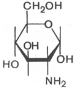

D-глюкозамин D-галактозамин
Аминосахара входят в состав мукополисахаридов животного, растительного и бактериального происхождения, являются углеводными компонентами различных гликопротеинов и гликолипидов. В составе этих высокомолекулярных соединений аминогруппа аминосахара чаще всего ацилирована, а иногда сульфирована.
72. Структура, свойства и биологическая роль аминосахаров и их ацильных производых. Напишите структурную формулу N-ацетилнейраминовой кислоты.
Это производные моносахаридов, гидроксильная группа которых —ОН замещена аминогруппой —NH2. В зависимости от положения аминогруппы (при атомах углерода) в молекуле аминосахара различают 2-амино-, 3-амино- и 4-аминосахара и т.д. По числу аминогрупп выделяют моноаминосахара и диаминосахара. Аминосахара обладают всеми свойствами аминов, обычных моносахаров, а также специфическими свойствами, обусловленными пространственной близостью гидроксильных и аминных групп. В организме человека и животных наиболее важными аминосахарами являются D-глюкозамин и D-галактозамин:


D-глюкозамин D-галактозамин
Аминосахара входят в состав мукополисахаридов животного, растительного и бактериального происхождения, являются углеводными компонентами различных гликопротеинов и гликолипидов. В составе этих высокомолекулярных соединений аминогруппа аминосахара чаще всего ацилирована, а иногда сульфирована.
Формула N-ацетилнейраминовой кислоты (спава)

73. В состав гликозаминогликанов входят аминосахара: глюкозамин и галактозамин в виде N-ацетилированных производных. Напишите 2-1М-ацетил-а-В-глюкозамин и 2-Ы-ацетил-р-В-галактозамин в пиранозной форме.
???
74. Что такое гликозиды? Как определить принадлежность гликозидов к L- и D-ряду? Напишите формулы следующих веществ:
а) метил-Р-Б-фруктопиранозида; б) метил- a-D-глюкопиранозида.
Продуктами реакции замещения полуацетального гидроксила другими группировками в реакциях со спиртами, карбоновыми кислотами,фенолами называются гликозиды.
Соответственно α- и β-изомерам моносахаридов существуют α- и β-глюкозиды. Например, при реакции метилового спирта с глюкозой (допустим, в β-пиранозной форме) в присутствии неорганических кислот образуется продукт алкилирования метил-β-D-глюкопиранозид. При действии на β-D-глюкопиранозу уксусной кислотой образуется продукт ацилирования ацетил-β-D-глюкопиранозид.
А) метил-b-D-фруктопиранозид 
Б) 
Метил-b-D-гликопиранозид (у a-D-формы OCH3 вниз)
75. Редуцирующие сахара. Химические свойства лактозы (напишите формулу). Способна ли она к мутаротации? Может ли она восстанавливать Си2+ до Си1+? Ответ подтвердить уравнениями химических реакций.
Лактоза (от лат. lactis — молоко) C12H22O11 — углевод группы дисахаридов, содержится в молоке и молочных продуктах. Молекула лактозы состоит из остатков молекул глюкозы и галактозы. Лактоза относится классу активных (восстанавливающих, редуцирующих углеводов).
Химические свойства:
- При кипячении с разбавленной кислотой происходит гидролиз лактозы.
- При взаимодействии с раствором щёлочи лактоза окисляется до сахариновых кислот.


Полуацетальный гидроксил глюкозы в молекуле лактозы, в отличие от молекулы сахарозы, остается свободным, поэтому лактоза является мутаротирующим и восстанавливающим сахаром.
Способна восстанавливать Си2+ до Си1+ :
C12H22O11 + 2Сu(ОН)2 —— > С12Н22О12 + Cu2Ov + 2Н2О.
76. Сахароза и лактоза, их строение и химические свойства. Какой из дисахаридов будет восстанавливать Си2+ в щелочной среде. Напишите уравнение реакции.
Сахароза.

Свойства
Сахароза - тростниковый или свекловичный сахар представляет собой белое кристаллическое вещество, растворимое в 0,5 частей воды и в 60 частях спирта, не растворимое в эфире и хлороформе.
Плавится при температуре 184-185°С, при дальнейшем нагревании темнеет и превращается в бурую, горькую на вкус массу (карамель).
Поскольку гликозидную связь в молекуле сахара образуют полуацетальные гидроксилы глюкозы и фруктозы, она является не восстанавливающим и не мутаротирующим сахаром.
Лактоза. (будет восстанавливать медь)

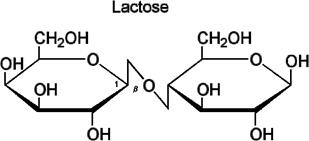
Свойства.
Уже название этого сахара говорит о том, что он встречается в молоке млекопитающих; женское молоко содержит 5—8% лактозы, коровье - 4-6%.В промышленном масштабе лактозу получают в качестве побочного продукта при производстве сыра.
Полученное вещество представляет собой белые кристаллы или белый кристаллический порошок, без запаха, слабого сладкого вкуса.
Полуацетальный гидроксил глюкозы в молекуле лактозы, в отличие от молекулы сахарозы, остается свободным, поэтому лактоза является мутаротирующим и восстанавливающим сахаром.
C12H22O11 + 2Сu(ОН)2 —— > С12Н22О12 + Cu2Ov + 2Н2О.
77. Какой вывод можно сделать о химических свойствах сахарозы на основании ее строения? Способна ли она к мутаротации? Может ли она восстанавливать аммиачный раствор серебра, реактив Фелинга?
Ответ подтвердить уравнениями химических реакций.

Это дисахарид из группы олигосахаридов, состоящий из двух моносахаридов — α-глюкозы и β-фруктозы. Не проявляет восстанавливающих свойств — не реагирует с реактивом Толленса и реактивом Фелинга. Не образует открытую форму, поэтому не проявляет свойств альдегидов и кетонов. Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов. Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди. Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором оксида серебра (I) она не дает «серебряного зеркала» (в отличие от формалина: H-CHO + 2 Ag2O ---> CO2 + H2O + 4 Ag (осадок - "зеркало")), при нагревании с гидроксидом меди (II) не образует красного оксида меди (I). Не способна к мутаротации,. поскольку гликозидную связь в молекуле сахара образуют полуацетальные гидроксилы глюкозы и фруктозы.
78. Строение сахарозы (напишите структурную формулу), её свойства. Инверсия сахарозы. Как называется и чем характеризуется подобный тип олигосахаридов?


Свойства
Сахароза - тростниковый или свекловичный сахар представляет собой белое кристаллическое вещество, растворимое в 0,5 частей воды и в 60 частях спирта, не растворимое в эфире и хлороформе.
Плавится при температуре 184-185°С, при дальнейшем нагревании темнеет и превращается в бурую, горькую на вкус массу (карамель).
Поскольку гликозидную связь в молекуле сахара образуют полуацетальные гидроксилы глюкозы и фруктозы, она является не восстанавливающим и не мутаротирующим сахаром.
Благодаря наличию в молекуле свободного полуацетального гидроксила (в остатке глюкозы) лактоза относится к числу редуцирующих дисахаридов.
Гидролиз сахарозы приводит к образованию смеси, которую называют инвертированным сахаром. В этой смеси преобладает сильно левовращающая фруктоза, которая инвертирует (меняет на обратный) знак вращения правовращающего раствора исходной сахарозы.
Относится к дисахаридам - сложные сахара, каждая молекула которых при гидролизе распадается на две молекулы моносахаридов. Дисахариды наряду с полисахаридами являются одними из основных источников углеводов в пище человека и животных. По строению дисахариды – это гликозиды, в которых 2 молекулы моносахаридов соединены гликозидной связью. Молекула сахарозы состоит из одного остатка D-глюкозы и одного остатка D-фруктозы. Следовательно, это α-глюкопиранозил-(1–>2)-β-фруктофуранозид.
79. Гомогликаны, их строение и функции. Напишите структурную формулу фрагмента гликогена с точкой ветвления и целлюлозы.
Полисахариды, построенные из моносахаридных звеньев одного типа, называются гомогликаны.
Гомогликаны делятся на:
- гексозаны (C6H10O5. Полисахариды, молекулы которых построены из большого числа гексозных остатков, соединённых α- или β-гликозидными связями. К Г. относятся крахмал, гликоген, целлюлоза, декстраны, галактаны, маннаны, фруктозаны, лишайниковый крахмал — лихенин, глюкоманнаны, арабогалактаны и др.);
- пентазаны (так называются сахароколлоиды (полисахариды), дающие при гидролизе пентозы. К последним они стоят в таком же точно отношении, как гексозаны (крахмал, клетчатка, инулин и др.) к гексозам (декстрозе, фруктозе и др.), и представляют, следовательно, их ангидриды (ср. Клетчатка), состав которых выражается формулами (C5H8O4)n или (C 10H18O9)n, а происхождение из пентоз уравнением nC 5H10O5 - nH2O = (C5H8O4)n и т. п. Гидролиз П. совершается весьма легко при кипячении с разбавленными кислотами (серной или соляной), вследствие чего их надо отнести, согласно обозначению Э. Шульце, к числу так называемых полуклетчаток, или гемицеллюлоз. В настоящее время известно лишь два П. - ксилан и арабан, которые соответствуют пентозам - ксилозе и арабинозе и чрезвычайно сильно распространены в растениях, где они являются обыкновенно существенной частью в составе различных их тканей.).
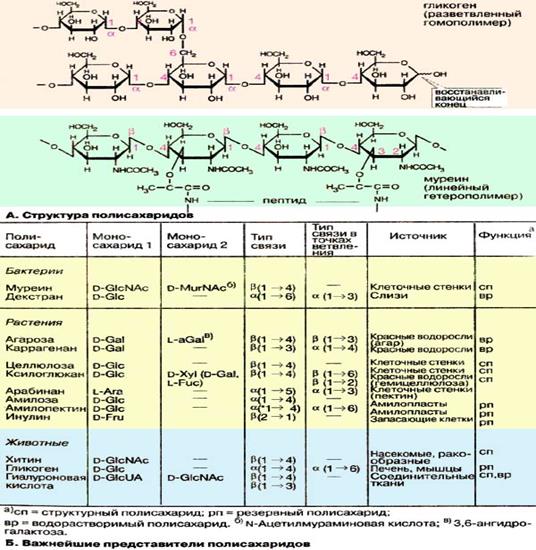
Целлюлоза

80. Охарактеризуйте физико-химические свойства и укажите структурные особенности крахмала, гликогена и целлюлозы. Укажите черты сходства и различия в строении и свойствах указанных гомогликанов.
Крахмал, как отмечалось, является основным резервным материалом растительных организмов. В небольших количествах он содержится в листьях, но главным образом накапливается в семенах (зерна злаков, например пшеницы, риса, кукурузы, содержат до 70% крахмала), а также в луковицах, клубнях и сердцевине стебля растений, где содержание его доходит до 30%. Крахмал представляет собой смесь 2 гомополисахаридов: линейного – амилозы и разветвленного – амилопектина, общая формула которых (С6Н10О5)n. Как правило, содержание амилозы в крахмале составляет 10–30%, амилопектина – 70–90%. Полисахариды крахмала построены из остатков D-глюкозы, соединенных в амилозе и линейных цепях амилопектина α-1–>4-связями, а в точках ветвления амилопектина – межцепочечными α-1–>6-связями.
Итак, единственным моносахаридом, входящим в состав крахмала, является D-глюкоза. В молекуле амилозы линейно связано в среднем около 1000 остатков глюкозы; отдельные участки молекулы амилопектина состоят из 20–30 таких единиц. В настоящее время общепринятой является ветвистая структура отдельных цепочек с α-1–>4-связями в молекуле амилопектина.
Известно, что в воде амилоза не дает истинного раствора. Цепочка амилозы в воде образует гидратированные мицеллы. В растворе при добавлении йода амилоза окрашивается в синий цвет. Амилопектин также дает мицеллярный раствор, но форма мицелл несколько иная. Полисахарид амилопектин окрашивается йодом в красно-фиолетовый цвет. Крахмал имеет молекулярную массу 105–107 Да. При частичном кислотном гидролизе крахмала образуются полисахариды меньшей степени полимеризации – декстрины *, при полном гидролизе – глюкоза. Для человека крахмал является важным пищевым углеводом; содержание его в муке составляет 75–80%, в картофеле – 25%.
Гликоген – главный резервный полисахарид высших животных и человека, построенный из остатков D-глюкозы. Эмпирическая формула гликогена, как и крахмала, (С6Н10О5)n. Гликоген содержится практически во всех органах и тканях животных и человека; наибольшее количество
обнаружено в печени и мышцах. Молекулярная масса гликогена 105–108 Да и более. Его молекула построена из ветвящихся полиглюкозидных цепей, в которых остатки глюкозы соединены α-1–>4-гликозидными связями. В точках ветвления имеются α-1–>6-гликозидные связи. По строению гликоген близок к амилопектину. В молекуле гликогена различают внутренние ветви – участки от периферической точки ветвления до нередуцирующего конца цепи. Гликоген характеризуется более разветвленной структурой, чем амилопектин; линейные отрезки в молекуле гликогена включают 11–18 остатков α-D-глюкопиранозы. При гидролизе гликоген, подобно крахмалу, расщепляется с образованием сначала декстринов, затем мальтозы и, наконец, глюкозы. Инулин – полисахарид, содержащийся в клубнях и корнях георгинов, артишоков и одуванчиков. При его гидролизе образуется фруктоза, следовательно, он представляет собой фруктазан. Метилирование инулина свидетельствует, что остатки D-фруктозы связаны между собой 2–>1-связями и находятся в фуранозной форме. Степень полимеризации инулина равна примерно 35 моносахарным остаткам. Этот полисахарид в отличие от картофельного крахмала легко растворяется в теплой воде. Инулин используют в физиологических исследованиях для определения скорости клубочковой фильтрации в почках.
Целлюлоза (клетчатка) – наиболее широко распространенный структурный полисахарид растительного мира. Он состоит из α-глюкозных остатков в их β-пиранозной форме, т.е. в молекуле целлюлозы β-глюкопиранозные мономерные единицы линейно соединены между собойβ-(1–>4)-связями. При частичном гидролизе целлюлозы образуется дисахарид целлобиоза, а при полном гидролизе – D-глюкоза. Молекулярная масса целлюлозы 1000–2000 кДа. Клетчатка не переваривается ферментами пищеварительного тракта, так как набор этих ферментов у человека не содержит гидролаз, расщепляющих β-связи. В связи с этим целлюлозу можно рассматривать как значительный неиспользуемый пищевой резерв. Вместе с тем известно, что присутствие оптимальных количеств клетчатки в пище способствует формированию кала. При полном исключении клетчатки из пищи нарушается формирование каловых масс. В кишечнике жвачных и других травоядных животных имеются микроорганизмы, способные к ферментативному расщеплению β-связей (β-глюкозидных связей), и для этих животных целлюлоза является важным источником пищевых калорий. Наконец, целлюлоза и ее производные имеют колоссальное практическое значение. Основная масса целлюлозы используется для изготовления хлопчатобумажных тканей и бумаги. Кроме того, на основе целлюлозы производятся искусственные волокна, пластмассы и т.д. Характерной особенностью целлюлозы, определяющей в значительной степени ее механические, физико-химические и химические свойства, является линейная конформация молекул, закрепленная внутримолекулярными водородными связями.
81. Амилоза, амилопектин, целлюлоза, гликоген и декстраны построены из остатков D-глюкозы. Какие виды связей между D-глюкопиранозными остатками в указанных гомогликанах? Чем отличаются эти полимеры? Напишите структурную формулу дисахаридного фрагмента этих гомогликанов.
Участок молекулы амилозы

Участок молеклы амилопектина

Участок молекулы целлюлозы
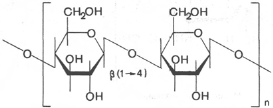
Участок молекулы гликогена

Инулин (декстран)

Хитин (декстран)

82. Гетерогликаны, их строение и функции. Приведите примеры. Напишите структурную формулу фрагмента какого-либо гетерогликана.
Полисахариды, в структуре которых характерно наличие двух или более типов мономерных звеньев, носят название гетерополисахаридов. Принято считать, что, поскольку гетерополисахариды чаще состоят только из двух различных мономеров, расположенных повторяющимся образом, они не являются информационными молекулами. Важнейшие представители гетерополисахаридов в органах и тканях животных и человека – гликозаминогликаны (мукополисахариды). Они состоят из цепей сложных углеводов, содержащих аминосахара и уроновые кислоты. Различают шесть основных классов гликозаминогликанов. Каждый из гликозаминогликанов содержит характерную для него повторяющуюся дисахаридную единицу; во всех случаях (кроме кератансульфатов) эта единица содержит либо глюкуроновую, либо идуроновую кислоту. Все гликозаминогликаны, за исключением гиалуроновой кислоты, содержат остатки моносахаридов с О- или N-сульфатной группой. Гликозаминогликаны значительно различаются по размерам, их молекулярные массы в пределах от 104 Да для гепарина до 107 Да для гиалуроновой кислоты. Выделенные индивидуальные гликозаминогликаны могут содержать смесь цепей различной длины (рис. 5.5). Гликозаминогликаны как основное скрепляющее вещество связаны со структурными компонентами костей и соединительной ткани. Их функция состоит также в удержании большой массы воды и в заполнении межклеточного пространства. Иными словами, гликозаминогликаны – основной компонент внеклеточного вещества – желатинообразного вещества, заполняющего межклеточное пространство тканей. Они также содержатся в больших количествах в синовиальной жидкости – это вязкий материал, окружающий суставы, который служит смазкой и амортизатором. Поскольку водные растворы гликозаминогликанов гелеобразны, их называют мукополисахаридами. Наконец, если цепи гликозаминогликана присоединены к белковой молекуле, соответствующее соединение называют протеогликаном. Протеогликаны образуют основное вещество внеклеточного матрикса. В отличие от простых гликопротеинов, которые содержат только несколько процентов углеводов (по массе), протеогликаны могут содержать до 95% (и более) углеводов.
Гепарин

Сульфатированный Сульфатированная
Гликозаминн идуроновая к-та
83. Классификация и физико-химические свойства липидов.
Липиды представляют собой обширную группу соединений, существенно различающихся по своей химической структуре и функциям. Поэтому трудно дать единое определение, которое подошло бы для всех соединений, относящихся к этому классу. Можно сказать, что липиды представляют собой группу веществ, которые характеризуются следующими признаками: нерастворимостью в воде; растворимостью в неполярных растворителях, таких, как эфир, хлороформ или бензол; содержанием высших алкильных радикалов; распространенностью в живых организмах. Под это определение попадает большое количество веществ, в том числе такие, которые обычно причисляют к другим классам соединений: например, жирорастворимые витамины и их производные, каротиноиды, высшие углеводороды и спирты. Включение всех этих веществ в число липидов в известной степени оправдано, потому что в живых организмах они находятся вместе с липидами и вместе с ними экстрагируются неполярными растворителями. С другой стороны, имеются представители липидов, которые довольно хорошо растворяются в воде (например, лизолецитины). Термин липиды является более общим, чем термин липоиды, который объединяет группу жироподобных веществ, таких, как фосфолипиды, стерины, сфинголипиды и др.
Классификация:
Существует несколько классификаций липидов. Наибольшее распространение получила классификация, основанная на структурных особенностях липидов. По этой классификации различают следующие основные классы липидов.
A. Простые липиды: сложные эфиры жирных кислот с различными спиртами.
1. Глицериды (ацилглицерины, или ацилглицеролы – по международной номенклатуре) представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот.
2. Воска: сложные эфиры высших жирных кислот и одноатомных или двухатомных спиртов.
Б. Сложные липиды: сложные эфиры жирных кислот со спиртами, дополнительно содержащие и другие группы.
1. Фосфолипиды: липиды, содержащие, помимо жирных кислот и спирта, остаток фосфорной кислоты. В их состав часто входят азотистые основания и другие компоненты:
а) глицерофосфолипиды (в роли спирта выступает глицерол);
б) сфинголипиды (в роли спирта – сфингозин).
2. Гликолипиды (гликосфинголипиды).
3. Стероиды.
4. Другие сложные липиды: сульфолипиды, аминолипиды. К этому классу можно отнести и липопротеины.
B. Предшественники и производные липидов: жирные кислоты, глицерол, стеролы и прочие спирты (помимо глицерола и стеролов), альдегиды жирных кислот, углеводороды, жирорастворимые витамины и гормоны.
84. Строение, физико-химические свойства жирных кислот. Приведите примеры. Напишите структурную формулу линоленовой кислоты.
Жирные кислоты – алифатические карбоновые кислоты – в организме могут находиться в свободном состоянии (следовые количества в клетках и тканях) либо выполнять роль строительных блоков для большинства классов липидов. В природе обнаружено свыше 200 жирных кислот, однако в тканях человека и животных в составе простых и сложных липидов найдено около 70 жирных кислот, причем более половины из них в следовых количествах. Практически значительное распространение имеют немногим более 20 жирных кислот. Все они содержат четное число углеродных атомов, главным образом от 12 до 24. Среди них преобладают кислоты, имеющие С16 и С18 (пальмитиновая, стеариновая, олеиновая и линолевая). Нумерацию углеродных атомов в жирно-кислотной цепи начинают с атома углерода карбоксильной группы. Примерно 3/4 всех жирных кислот являются непредельными (ненасыщенными), т.е. содержат двойные связи. Ненасыщенные жирные кислоты человека и животных, участвующие в построении липидов, обычно содержат двойную связь между (9-м и 10-м атомами углеводородов); дополнительные двойные связи чаще бывают на участке между 11-м атомом углерода и метильным концом цепи. Своеобразие двойных связей природных ненасыщенных жирных кислот заключается в том, что они всегда отделены двумя простыми связями, т.е. между ними всегда имеется хотя бы одна метиленовая группа (—СН=СН——СН2—СН=СН—). Подобные двойные связи обозначают как ≪изолированные≫. Систематическое название жирной кислоты чаще всего образуется путем добавления к названию углеводорода окончания -овая. Насыщенные кислоты при этом имеют окончание -ановая (например, октановая кислота –систематическое название, каприловая кислота – тривиальное название), а ненасыщенные кислоты – -еновая (например, октадеценовая кислота – систематическое название, олеиновая кислота – тривиальное название).
В специальной литературе жирные кислоты часто изображают в виде зигзагообразной вытянутой линии, отражающей жесткость валентного угла атомов углерода в 111° для насыщенной и в 123° – для двойной связи. Однако такая конформация является условной и справедлива только для случая, когда жирная кислота находится в кристаллическом состоянии. В растворах жирно-кислотная цепь может образовывать бесчисленное количество конформаций вплоть до клубка, в котором имеются и линейные участки различной длины в зависимости от числа двойных связей. Клубки могут слипаться между собой, образуя так называемые мицеллы. В последних отрицательно заряженные карбоксильные группы жирных кислот обращены к водной фазе, а неполярные углеводородные цепи спрятаны внутри мицеллярной структуры. Такие мицеллы имеют суммарный отрицательный заряд и в растворе остаются суспендированными благодаря
Не нашли, что искали? Воспользуйтесь поиском: