
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Негистоновые белки хроматина 3 страница
взаимному отталкиванию. Известно также, что при наличии двойной связи в жирнокислотной цепи вращение углеродных атомов относительно друг друга ограничено. Это обеспечивает существование ненасыщенных жирных кислот в виде геометрических изомеров, причем природные ненасыщенные жирные кислоты имеют цис- конфигурацию и крайне редко транс -конфигурации. Считают, что жирной кислоте с несколькими двойными связями цис- конфигурация придает углеводородной цепи изогнутый и укороченный вид. По этой причине молекулы этих кислот занимают больший объем, а при образовании кристаллов упаковываются не так плотно, как транс- изомеры. Вследствие этого цис- изомеры имеют более низкую температуру плавления (олеиновая кислота, например, при комнатной температуре находится в жидком состоянии, тогда как элаидиновая – в кристаллическом). Цис- конфигурация делает ненасыщенную кислоту менее стабильной и более подверженной катаболизму.
Структурная формула олеиновой кислоты

85. Характеристика высших жирных кислот, входящих в состав жира. Что называется кислотным числом, числом омыления, йодным числом.
Глицериды (ацилглицерины, или ацилглицеролы *) представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот. Если жирными кислотами этерифицированы все три гидроксильные группы глицерина (ацильные радикалы R1, R2 и R3 могут быть одинаковы или различны), то такое соединение называют триглицеридом (триацилглицерол), если две – диглицеридом (диацилглицерол) и, наконец, если этерифицирована одна группа – моноглицеридом (моноацилглицерол). Наиболее распространенными являются триглицериды, часто называемые нейтральными жирами или просто жирами. Нейтральные жиры находятся в организме либо в форме протоплазматического жира, являющегося структурным компонентом клеток, либо в форме запасного, резервного, жира. Роль этих двух форм жира в организме неодинакова. Протоплазматический жир имеет постоянный химический состав и содержится в тканях в определенном количестве, не изменяющемся даже при патологическом ожирении, в то время как количество резервного жира подвергается большим колебаниям. Как отмечалось, основную массу природных нейтральных жиров составляют триглицериды. Жирные кислоты в триглицеридах могут быть насыщенными и ненасыщенными. Из жирных кислот чаще встречаются пальмитиновая, стеариновая и олеиновые кислоты. Если все три кислотных радикала принадлежат одной и той же жирной кислоте, то такие триглицериды называют простыми (например, трипальмитин, тристеарин, триолеин и т.д.), если разным жирным кислотам, то смешанными. Названия смешанных триглицеридов образуются в зависимости от входящих в их состав жирных кислот, при этом цифры 1, 2 и 3 указывают на связь остатка жирной кислоты с соответствующей спиртовой группой в молекуле глицерина (например, 1-олео-2-пальмитостеарин). Необходимо отметить, что положение крайних атомов в молекуле глицерина на первый взгляд равнозначно, тем не менее их обозначают сверху вниз – 1 и 3. Это объясняется прежде всего тем, что в структуре триглицерида при пространственном ее рассмотрении крайние ≪глицериновые≫ атомы углерода становятся уже не равнозначными, если гидроксилы 1 и 3 ацилированы разными жирными кислотами. При необходимости применяют также систему стереохимической нумерации (обозначают sn –stereochemical numbering): например, 1,2-дистеарил-3-пальмитил-sn-глицерол.
По этой системе, если в проекции Фишера гидроксильная группа при 2-м углеродном атоме глицерина располагается слева, атому углерода, находящемуся над ним, присваивается номер 1, а расположенному под ним – номер 3. Действительно, углероды 1 и 3 глицерола, учитывая их пространственное расположение, неидентичны. Особенно четко это видно на примере молекулы триглицерида. Ферменты это различают и всегда специфичны только к одному из трех углеродов глицерина. Так, глицеролкиназа фосфорилирует глицерин в положении sn-3, в результате чего образуется глицерол-3-фосфат, но не глицерол-1-фосфат. Жирные кислоты, входящие в состав триглицеридов, практически определяют их физико-химические свойства. Так, температура плавления триглицеридов повышается с увеличением числа и длины остатков насыщенных жирных кислот. Напротив, чем выше содержание ненасыщенных жирных кислот, или кислот с короткой цепью, тем ниже точка плавления. Животные жиры (сало) обычно содержат значительное количество насыщенных жирных кислот (пальмитиновой, стеариновой и др.). благодаря чему при комнатной температуре они твердые. Жиры, в состав которых входит много ненасыщенных кислот, при обычной температуре жидкие и называются маслами. Так, в конопляном масле 95% всех жирных кислот приходится на долю олеиновой, линолевой и линоленовой кислот и только 5% – на долю стеариновой и пальмитиновой кислот. В жире человека, плавящемся при температуре 15°С (при температуре тела он жидкий), содержится 70% олеиновой кислоты. Глицериды способны вступать во все химические реакции, свойственные сложным эфирам. Наибольшее значение имеет реакция омыления, в результате которой из триглицеридов образуются глицерол и жирные кислоты. Омыление жира * может происходить как при ферментативном гидролизе, так и при действии кислот или щелочей.
Кислотное число — количество миллиграмм гидроксида калия (KOH), необходимое для нейтрализации всех кислых компонентов, содержащихся в 1 г исследуемого вещества.
Число омыления — количество миллиграммов гидроксида калия (KOH), необходимое для нейтрализации свободных кислот и омыления сложных эфиров, содержащихся в 1 грамме исследуемого вещества.
Иодное число — масса иода (в г), присоединяющегося к 100 г органического вещества.
86. Моно- и полиеновые жирные кислоты, структура, свойства распространение. Напишите формулы следующих жирных кислот и назовите их:
18:1;9 олеиновая
18:2;9,12 линоленовая
20:4;5,8,11,14 арахидоновая 
Жирные кислоты, содержащие двойные связи, называют ненасыщенными. Ненасыщенные жирные кислоты представлены моноеновыми (с одной двойной связью) и полиеновыми (с двумя и большим числом двойных связей). Если в составе жирной кислоты содержатся две и более двойных связей, то они располагаются через СН2-группу.
Структурная формула моноеновой (пример,олеиновая)

Стр.ф-ла палеиновой (линолевая)

Св-ва,распространение.
НЖК с одной или несколькими двойными связями являются структурными элементами фосфолипидов мембран и имеются в организме человека в значительных количествах (незаменимые жирные кислоты — линолевая, линоленовая, арахидоновая — поступают в организм с пищей). Самой распространенной из ненасыщенных жирных кислот является олеиновая. В фосфолипидах животных тканей очень мало содержится линолевой кислоты (0,05-0,4%), так как она превращается в линоленовую и арахидоновую. Линоленовая НЖК содержится в значительных количествах — 4-24%, содержание арахидоновой кислоты в фосфолипидах тканей составляет 0,2-22% (табл. 1). Биологическое значение ненасыщенных жирных кислот в метаболизме окончательно не выяснено, механизмы катаболизма НЖК в клетках животных также досконально не изучены. В молекулах НЖК две двойные связи, расположенные следующим образом: -СН=СН-СН=СН–, называются сопряженными (конъюгированными) (Л. Уайт и соавт., 1981).
Двойные связи определяют существование двух разных жирных кислот с 18-20 углеродными атомами, имеющими различное положение в пространстве: трансизомер имеет прямую форму, а углеродная цепь цисизомера всегда изогнута в месте двойной связи. Ненасыщенные жирные кислоты являются только цисизомерами, т.е. они все изогнуты. Жирные кислоты в свободном состоянии редко встречаются в составе мембран. Они являются важным фактором регулирования проницаемости мембран (влияют на поверхностные свойства фосфолипидов, белок-липидные и липид-липидные взаимодействия), функционирования мембранно-связанных ферментов (П. Г. Богач и соавт., 1981). В мембранах располагаются ферменты, активность которых зависит от липидного окружения. В этом окружении ферменты имеют определенную конформацию. Изменение липидного окружения (делипидирование, использование липолитических ферментов, липидообменивающих белков) ведет к изменению конформации белков (ферментов), изменению их каталитической активности (Н. Е. Кучеренко, А. Н. Васильев, 1985). Активность ферментов в мембранах связана с вязкостью липидной фазы мембран, составом липидов (П. Г. Богач и соавт., 1981; Н. Е. Кучеренко, А. Н. Васильев, 1985). Метаболическая активность липидзависимых ферментов определяется изменениями в липидном микроокружении и в первую очередь это касается фосфолипидов: от их состава и метаболизма зависят ферментативные процессы. Это подтверждено для микросомальной монооксигеназной системы. Липидные молекулы являются матриксом, оптимальным для функционирования мембранно-связанных ферментов. НЖК в мембранах придают им такое качество, как жидкостность (текучесть). Увеличение в мембранах содержания холестерина, насыщенность жирнокислотных радикалов в фосфолипидах снижают жидкостность мембран. Подвижность липидов изменяет конформацию полярных головок. Регулирующее влияние на мембранно-связанные ферменты оказывают гликофосфолипиды (стабилизируя мембраны). При модификации липидного состава теряется чувствительность к гормонам, фосфолипиды влияют на функционирование рецепторов, могут регулировать их число (Н. Е. Кучеренко, А. В. Васильев, 1985), взаимодействовать с токсинами. Интенсивность обновления фосфолипидов зависит от скорости синтеза ДНК в клетке. Имеется связь синтеза ДНК с составом липидов, перераспределением фракций фосфолипидов, степенью ненасыщенности жирнокислотных радикалов (насыщенные жирные кислоты тормозят синтез ДНК). Такие фракции фосфолипидов, как фосфатидилэтаноламины, кардиолипины дестабилизируют молекулы ДНК путем усиления активности ДНК-полимеразы. Фосфолипиды влияют на прочность ДНК (стабилизацию структуры). Все эти данные (Н. Е. Кучеренко, А. Н. Васильев, 1985) свидетельствуют о важной регуляторной роли фосфолипидов мембран, составной частью которых являются ненасыщенные жирные кислоты.
87. Арахидоновая кислота и ее производные, их роль в обмене веществ.

рахидоновая кислота - (эйкозатетраеновая кислота;5,8,11,14-эйкозатетpаеновая) - полиненасыщенная жирная кислота, входит в состав мембранных фосфолипидов тромбоцитов и эндотелиальных клеток. Высвобождается из фосфолипидов под действием фосфолипазы А2 и фосфолипазы С (рис. 2.3 allerg), активируемых коллагеном, тромбином, АДФ и другими биологически активными веществами. Арахидоновая кислота является предшественником в синтезе оксилипинов см. рис. 1-1 и рис. 1-2. Свободная арахидоновая кислота быстро метаболизируется, превращаясь в высокоактивные соединения - простагландины и тромбоксаны.
В составе липидов арахидоновая кислота присутствует в мозге, печени и молочном жире млекопитающих. В фосфолипидах надпочечников арахидоновая кислота составляет около 20 % от суммы жирных кислот. При гидрировании арахидоновая кислота образует арахиновую кислоту, встречающуюся в маслах бобовых растений, в частности — арахиса.[1] Метаболиты АК являются эндогенными лигандами каннабиноидных рецепторов (1992 - 95 гг.). Наиболее важными среди них являются продукт неокислительного метаболизма арахидоновой кислоты - арахидонилэтаноламид (анандамид) и 2- арахидонилглицерин, 2-АГ Оба соединения выполняют функции нейромодулятора и нейромедиатора и служат "эндогенными каннабиоидами".
88. Охарактеризуйте простые липиды: ацилглицерины, воски. Напишите структурную формулу триацилглицерина, дайте его полное название (с указанием жирнокислотных остатков).
Глицериды (ацилглицерины, или ацилглицеролы *) представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот. Если жирными кислотами этерифицированы все три гидроксильные группы глицерина (ацильные радикалы R1, R2 и R3 могут быть одинаковы или различны), то такое соединение называют триглицеридом (триацилглицерол), если две – диглицеридом (диацилглицерол) и, наконец, если этерифицирована одна группа – моноглицеридом (моноацилглицерол).

Триацилглицерол
Наиболее распространенными являются триглицериды, часто называемые нейтральными жирами или просто жирами. Нейтральные жиры находятся в организме либо в форме протоплазматического жира, являющегося структурным компонентом клеток, либо в форме запасного, резервного, жира. Роль этих двух форм жира в организме неодинакова. Протоплазматический жир имеет постоянный химический состав и содержится в тканях в определенном количестве, не изменяющемся даже при патологическом ожирении, в то время как количество резервного жира подвергается большим колебаниям. Как отмечалось, основную массу природных нейтральных жиров составляют триглицериды. Жирные кислоты в триглицеридах могут быть насыщенными и ненасыщенными. Из жирных кислот чаще встречаются пальмитиновая, стеариновая и олеиновые кислоты. Если все три кислотных радикала принадлежат одной и той же жирной кислоте, то такие триглицериды называют простыми (например, трипальмитин, тристеарин, триолеин и т.д.), если разным жирным кислотам, то смешанными. Названия смешанных триглицеридов образуются в зависимости от входящих в их состав жирных кислот, при этом цифры 1, 2 и 3 указывают на связь остатка жирной кислоты с соответствующей спиртовой группой в молекуле глицерина (например, 1-олео-2-пальмитостеарин). Необходимо отметить, что положение крайних атомов в молекуле глицерина на первый взгляд равнозначно, тем не менее их обозначают сверху вниз – 1 и 3. Это объясняется прежде всего тем, что в структуре триглицерида при пространственном ее рассмотрении крайние ≪глицериновые≫ атомы углерода становятся уже не равнозначными, если гидроксилы 1 и 3 ацилированы разными жирными кислотами. При необходимости применяют также систему стереохимической нумерации (обозначают sn –stereochemical numbering): например, 1,2-дистеарил-3-пальмитил-sn-глицерол.
По этой системе, если в проекции Фишера гидроксильная группа при 2-м углеродном атоме глицерина располагается слева, атому углерода, находящемуся над ним, присваивается номер 1, а расположенному под ним – номер 3. Действительно, углероды 1 и 3 глицерола, учитывая их пространственное расположение, неидентичны. Особенно четко это видно на примере молекулы триглицерида. Ферменты это различают и всегда специфичны только к одному из трех углеродов глицерина. Так, глицеролкиназа фосфорилирует глицерин в положении sn-3, в результате чего образуется глицерол-3-фосфат, но не глицерол-1-фосфат. Жирные кислоты, входящие в состав триглицеридов, практически определяют их физико-химические свойства. Так, температура плавления триглицеридов повышается с увеличением числа и длины остатков насыщенных жирных кислот. Напротив, чем выше содержание ненасыщенных жирных кислот, или кислот с короткой цепью, тем ниже точка плавления. Животные жиры (сало) обычно содержат значительное количество насыщенных жирных кислот (пальмитиновой, стеариновой и др.). благодаря чему при комнатной температуре они твердые. Жиры, в состав которых входит много ненасыщенных кислот, при обычной температуре жидкие и называются маслами. Так, в конопляном масле 95% всех жирных кислот приходится на долю олеиновой, линолевой и линоленовой кислот и только 5% – на долю стеариновой и пальмитиновой кислот. В жире человека, плавящемся при температуре 15°С (при температуре тела он жидкий), содержится 70% олеиновой кислоты. Глицериды способны вступать во все химические реакции, свойственные сложным эфирам. Наибольшее значение имеет реакция омыления, в результате которой из триглицеридов образуются глицерол и жирные кислоты. Омыление жира * может происходить как при ферментативном гидролизе, так и при действии кислот или щелочей.
Воска – сложные эфиры высших жирных кислот и высших одноатомных или двухатомных спиртов с числом углеродных атомов от 16 до 22. Общие их формулы можно представить так:
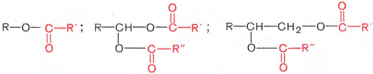
В этих формулах R, R' и R" – возможные радикалы.
Воска могут входить в состав жира, покрывающего кожу, шерсть, перья. У растений 80% от всех липидов, образующих пленку на поверхности листьев и плодов, составляют воска. Известно также, что воска являются нормальными метаболитами некоторых микроорганизмов. Природные воска (например, пчелиный воск, спермацет, ланолин) обычно содержат, кроме указанных сложных эфиров, некоторое количество свободных жирных кислот, спиртов и углеводородов с числом углеродных атомов 21–35.
89. Глицерофосфолипиды, их строение, разнообразие и свойства. Приведите примеры и напишите структурные формулы.
Глицерофосфолипиды являются производными фосфатидной кислоты. В их состав входят глицерин, жирные кислоты, фосфорная кислота и обычно азотсодержащие соединения. Общая формула глицерофосфолипидов выглядит так:


Фосфатидная кислота Глицеролфосфолипид
В этих формулах R1 и R2 – радикалы высших жирных кислот, a R3 – чаще радикал азотистого соединения. Для всех глицерофосфолипидов характерно, что одна часть их молекул (радикалы R1 и R2) обнаруживает резко выраженную гидрофобность, тогда как другая часть гидрофильна благодаря отрицательному заряду фосфорной кислоты и положительному заряду радикала R3.
Из всех липидов глицерофосфолипиды обладают наиболее выраженными полярными свойствами. При помещении глицерофосфолипидов в воду в истинный раствор переходит лишь небольшая их часть, основная же масса липидов находится в виде мицелл. Существует несколько групп (подклассов) глицерофосфолипидов. В зависимости от характера азотистого основания, присоединенного к фосфорной кислоте, Глицерофосфолипиды подразделяют на фосфатидилхолины (лецитины), фосфатидилэтаноламины (кефалины) и фосфатидилсерины. В состав некоторых глицерофосфолипидов вместо азотсодержащих соединений входит не содержащий азота шестиуглеродный циклический спирт инозит, называемый также инозитолом. Эти липиды называются фосфатидилинозитолами.
Фосфатидилхолины (лецитины). В отличие от триглицеридов в молекуле фосфатидилхолина одна из трех гидроксильных групп глицерина связана не с жирной, а с фосфорной кислотой. Кроме того, фосфорная кислота в свою очередь соединена эфирной связью с азотистым основанием – холином [НО—СН2—СН2—N+(CH3)3]. Таким образом, в молекуле фосфатидил-холина соединены глицерин, высшие жирные кислоты, фосфорная кислота и холин:

Фосфатидилхолин
Фосфатидилэтаноламины. Основное различие между фосфатидилхолинами и фосфатидилэтаноламинами – наличие в составе последних азотистого основания этаноламина (HO—CH2—CH2—N+H3):

Фосфатидилэтаноламин
Из глицерофосфолипидов в организме животных и высших растений в наибольшем количестве встречаются фосфатидилхолины и фосфатидилэтаноламины. Эти 2 группы глицерофосфолипидов метаболически связаны друг с другом и являются главными липидными компонентами мембран клеток.
Фосфатидилсерины. В молекуле фосфатидилсерина азотистым соединением служит остаток аминокислоты серина 

Фосфатидилсерин
Фосфатидилсерины распространены гораздо менее широко, чем фосфатидилхолины и фосфоэтаноламины, и их значение определяется в основном тем, что они участвуют в синтезе фосфатидилэтаноламинов.
90. Глицерофосфолипиды являются производными фосфатидной кислоты. Напишите формулу фосфатидной кислоты. Какими кислотами этерифицированы спиртовые группы большинства природных глицерофосфолипидов?

Фосфатидная кислота
Какими кислотами???
91. Напишите формулы: а- и b-фосфатидилхолинов, кардиолипина. Охарактеризуйте эти соединения.

Фосфатидилхолин
В отличие от триглицеридов в молекуле фосфатидилхолина одна из трех гидроксильных групп глицерина связана не с жирной, а с фосфорной кислотой. Кроме того, фосфорная кислота в свою очередь соединена эфирной связью с азотистым основанием – холином [НО—СН2—СН2—N+(CH3)3]. Таким образом, в молекуле фосфатидил-холина соединены глицерин, высшие жирные кислоты, фосфорная кислота и холин

Кардиолипин
Своеобразным представителем глицерофосфолипидов является кардиолипин, впервые выделенный из сердечной мышцы. По своей химической структуре кардиолипин можно рассматривать как соединение, в котором 2 молекулы фосфатидной кислоты связаны с помощью одной молекулы глицерина. В отличие от остальных глицерофосфолипидов кардиолипин является как бы ≪двойным≫ глицерофосфолипидом. Кардиолипин локализован во внутренней мембране митохондрий. Функция его пока неясна, хотя известно, что в отличие от других фосфолипидов кардиолипин обладает иммунными свойствами.
93. Церамиды и сфингомиелины
Церамидами называют?-ацильные производные сфингозинов, в которых аминогруппа основания ацилирована жирной кислотой. Эти соединения широко распространены в тканях растений и животных, но количества их незначительны. Церамиды различаются остатками жирных кислот, входящими в их состав. Жирные кислоты, присоединенные амидными связями к аминогруппе основания в молекуле церамида, содержат различное число атомов углерода (Ci6, Ci8, С22 или С24). Сфингомиелины могут рассматриваться как фосфохолиновые производные церамидов и являются одной из наиболее важных групп фосфолипидов.
О? II
ОН N—CR
СН3(СН2)12—СН=СН—СН—СН—СН2ОН цераммЭ
н?
ОН N—CR О CH3(CH2)12-CH=CH-CH-CH-CH2-0-P-OCH2CH2N=(CH3)3
о-сфмнгомиелмн
Хотя сфингомиелины по химическому строению и отличаются от фосфатидилхолина, эти соединения проявляют определенное сходство, обусловленное типичной для амфифилов структурой, а именно наличием ионной фосфорилхолиновой группировки и двух длинных углеводородных целей.
Впервые сфингомиелины были обнаружены в нервной ткани, однако они входят в состав липидов крови, а также встречаются во многих других тканях. Кроме обычных сфингозинов, рассмотренных выше, сфингомиелин из мозга содержит полиненасыщенные сфингозины, называемые дегидросфингозинами.
95. ЦЕРЕБРОЗИДЫ, сфинголипиды общей ф-лы RCH(OH)CH(NHCOR')CH2OX, где R и R' - алкил, гидроксиалкил, алкенил; X - остаток глюкозы (глюкоцереброзиды), галактозы (галактоцереброзиды) или фукозы (фукоцереброзиды). В глюко- и галакто-цереброзидах присутствует-гликозидная связь, в фуко-цереброзидах-гликозидная связь.
Цереброзиды- твердые в-ва, не раств. в воде, хорошо раств. в орг. р-рителях. При кислотном гидролизе образуют жирные к-ты, сфингозины (сфингозиновые основания) RCH(OH)CH(NH2)CH2OH и углеводы.
Цереброзиды содержатся в тканях человека, животных и высших растений. С их функционированием связана деятельность организма в целом и на клеточном уровне (изолирующие свойства миелиновой оболочки нервных аксонов, межклеточное узнавание, иммунологич. р-ции). Биосинтез цереброзидов протекает по двум путям: гликозилирование церамидов с помощью уридиндифосфатсахаров или гликозилирование сфингозинов с послед. N-ацилированием. Нарушения метаболизма цереброзидов, обусловленные снижением активности или отсутствием ферментов их гидролиза, имеют наследственный характер (т. наз. болезнь Краббе); при этом в органах и тканях, особенно в мозге, накапливаются галактоцереброзиды. Повышение содержания глюкоцереброзидов в мозге, печени свидетельствует о нарушениях обмена ганглиозидов (болезнь Гоше).
Осуществлен полный хим. синтез и полусинтез цереброзидов, их аналогов и меченых производных, используемых в качестве диагностич. и исследовательских биопрепаратов. Осн. путь синтеза - гликозилирование бензоилцерамидов RCH(OCOC,H5)CH(NHCOR')CH2OH по Кёнигса-Кнорра реакции. Наиб. стереоселективно с образованием-аномера гликозилирование происходит в присут. цианида ртути. Другой подход - ацилирование психозина (сфингозил--галактозида), полученного при избират. гидролизе прир. цереброзидов.
Типичными представителями цереброзидов головного мозга являются галактоцереброзиды на основе 4-сфингенина CH3(CH2)12CH = CHCH(OH)CH(NH2)CH2OH: френозин [в общей ф-ле R' = C22H25CH(OH)], т. пл. 195 °С; церазин (R' = С23H47), т. пл. 182 °С; нервон [R' = СН3(СН2)6СН = = СН(СН2)13].
96. При гидролизе распадаются на сфингозин, галактозу или глюкозу, а также остаток жирной кислоты. Цереброзиды содержатся в больших количествах в составе мозга, особенно в белом веществе мозга и мякотных нервных волокнах.
Избыточное накопление цереброзидов в организме и появление их в больших количествах в печени, селезенке, костном мозге и лимфатических узлах связано с некоторыми заболеваниями нервной системы — так называемой нейролипоидозами.
Среди этих жирных кислот чаще всего встречается лигноцериновая, нервоновая и цереброновая кислоты, т.е. жирные кислоты, имеющие 24 углеродных атома. Структура цереброзидов может быть представлена следующей схемой:
Сфингозин - СН2-О— гексоза (чаще галактоза)
0 = С — остаток жирной кислоты
97) ГАНГЛИОЗИДЫ (сиалогликосфинголипиды), гликосфин-голипиды общей ф-лы, где Х - углеводная цепь, содержащая остатки сиаловых к-т, связанных с остатком галактозы или гексозамина (см., напр., ф-лу I в ст. Гликосфинголипиды; Y - остаток N-ацетил- или N-гликолилнейраминовой к-ты, к-рые наз. сиаловыми к-тами - см. ф-лу).
В названиях ганглиозидов используют сочетание из двух букв - G (указывает принадлежность соед. к ганглиозидам) и М, D, Т или Q (показывают число сиаловых к-т в молекуле - соотв. 1, 2, 3 или 4) и цифры (иногда с буквами) в ниж. индексе, обозначающие конкретное в-во. Соед. I (ф-ла в ст. Гликосфинголипиды, Y-остаток N-ацетилнейраминовой к-ты) по этой номенклатуре обозначается GM1. В соответствии с правилами ИЮПАК это соед. обозначается II3AcNeuGgOse4Cer, где римская цифра показывает положение остатка моносахарида (считая от церамида; в общей ф-ле Х-Н), с к-рым связан остаток сиаловой к-ты, цифра в верх. индексе-номер углеродного атома в цикле, с к-рым связана эта к-та, AcNeuGgOse4-oлигocaxapиднaя цепь (AcNeu-остаток N-ацетилнейраминовой к-ты, GgOse4- остаток ганглиотет-раозы), Сеr-остаток церамида.
Ганглиозиды широко распространены в тканях животных, особенно в мозге. В растениях и микроорганизмах не встречаются. Локализованы в осн. на пов-сти плазматич. мембраны клетки. Как и др. Гликосфинголипиды участвуют в процессах регуляции роста и адгезии клеток, межклеточных взаимодействиях, иммунология, процессах. Могут входить в состав рецепторов токсинов (напр., GMj входит в состав рецептора токсина холеры), пептидных гормонов, нек-рых вирусов и интерферона.
В клетке ганглиозиды синтезируются в аппарате Гольджи путем переноса остатков моносахаридов и сиаловых к-т от уридиндифосфатсахаров и цитидинмонофосфатсиаловых к-т в присут. специфич. гликозилтрансфераз и сиалилтрансфераз к церамиду. При нарушении метаболизма ганглиозидов возникают болезни (ганглиозидозы). Изменение биосинтеза ганглиозидов происходит и при злокачественной трансформации клеток. В препаративных кол-вах ганглиозиды получают из прир. источников, в осн. из мозга.
98. Стерины
Стеролы, циклические спирты, относящиеся к классу стероидов (См. Стероиды), широко распространены в живой природе. Большинство С. — оптически-активные кристаллические вещества, растворимые в органических растворителях и нерастворимые в воде. Общим предшественником С. у микроорганизмов, растений и животных служит углеводород Сквален, превращающийся в циклический ланостерин (С30Н50О) или в его изомер циклоартенол, из которых затем образуются различные С., содержащие 27—29 атомов углерода. Важнейший С. животных — Холестерин, самый распространённый С. грибов, в том числе дрожжей,— Эргостерин, а из обширной группы С. растений (фитостеринов (См. Фитостерины)) наиболее распространены β-ситостерин и стигмастерин.
У высших животных С. содержатся в нервной ткани, печени, клетках спермы и т.д.: образуя с высшими жирными кислотами сложные эфиры, они служат их переносчиками в организме. В растениях С. находятся в свободном состоянии или в соединении с жирными кислотами (т. н. стериды), углеводами (т. н. фитостеролины) или с теми и другими вместе. С., поступающие с пищей, используются для синтеза гормонов насекомыми. которые не обладают ферментами, необходимыми для первых стадий биосинтеза С. К С. относят гормоны линьки насекомых (см. Экдизон (См. Экдизоны)) и антеридиол, индуцирующий половое размножение некоторых низших грибов. Близки к С. витанолиды (ненасыщенные Лактоны) и кукурбитацины (ненасыщенные горькие вещества из тыквенных растений), а также сапогенины морских беспозвоночных и входящие в состав Ланолина и восков ланостерин и др. тритерпены со стерановым углеродным скелетом (см. Стероиды). Наиболее изученные биохимич. функции С. — превращение холестерина в стероидные гормоны и эргостерина в витамины группы D под действием ультрафиолетового света. С. входят в состав биологических мембран (См. Биологические мембраны) как их структурные компоненты. Доступные С. (холестерин, эргостерин, (β-ситостерин) используются как сырьё для промышленного получения стероидных гормонов и витаминов группы D.
Не нашли, что искали? Воспользуйтесь поиском: