
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Будова атомних ядер
Факт існування атомних ядер вперше був доведений у досліді Резерфорда по бомбардуванню золотої фольги a -частками високої енергії. Математична обробка статистичних результатів досліду дозволила визначити і приблизні розміри ядра. Виявилось, що ядро має діаметр 10 - 14¸10 - 15 м, тобто на 4 – 5 порядків менше, ніж діаметр атома, який складає близько 10 - 10 м.
До складу ядра входить 2 типи елементарних часток: протони і нейтрони. Вони мають спільну назву – нуклони.
Протон – це позитивно заряджена частка, заряд якої по модулю дорівнює заряду електрона (елементарному заряду): е = 1,6 ×10 - 19 Кл.
Маса протона: тр = 1,6726 ×10 - 27 кг» 1836 те,
де те – маса електрона.
Нейтрон – це частка, яка не має електричного заряду, маса якої:
тп = 1,6749 ×10 - 27 кг» 1838,5 те
Загальний електричний заряд ядра визначається кількістю протонів у ядрі Z і дорівнює + Zе. Число Z називається атомним номером і визначає порядковий номер хімічного елемента в періодичній таблиці Менделєєва.
Загальна кількість нуклонів у ядрі позначається А і називається масовим числом ядра.
Для умовного позначення ядер користуються символами відповідних хімічних елементів з двома індексами, верхнім і нижнім, які записуються зліва:  , де Х - символ елемента, А - масове число, Z - атомний номер (число протонів у ядрі). Наприклад, ядро атома вуглецю позначається так:
, де Х - символ елемента, А - масове число, Z - атомний номер (число протонів у ядрі). Наприклад, ядро атома вуглецю позначається так:  .
.
Кількість нейтронів у ядрі, у відповідності до вищесказаного:
N = A - Z (5.7.1) Більшість хімічних елементів мають по кілька різновидів атомних ядер, які мають один і той же заряд (однакове число протонів), але відрізняються масовими числами (тобто мають різну кількість нейтронів). Такі атоми (або їх ядра) називаються ізотопами.
Ізотопи – це атомні ядра, що мають однаковий атомний номер, але різні масові числа.
Наприклад, водень має три ізотопи: звичайний водень (протій)  , важкий водень (дейтерій)
, важкий водень (дейтерій)  і надважкий водень (тритій)
і надважкий водень (тритій) 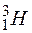 . Дейтерій міститься у звичайному водні у вигляді малої домішки. Тритій – це нестабільний ізотоп, тобто його ядро існує лише обмежений час, після чого розпадається. Період піврозпаду тритію 12,5 років. Ядра протію, дейтерію і тритію називаються, відповідно, протон, дейтрон і тритон. Внаслідок великого практичного значення ізотопів дейтерію і тритію, вони, на відміну від інших, отримали власні символічні позначення, відповідно D і Т.
. Дейтерій міститься у звичайному водні у вигляді малої домішки. Тритій – це нестабільний ізотоп, тобто його ядро існує лише обмежений час, після чого розпадається. Період піврозпаду тритію 12,5 років. Ядра протію, дейтерію і тритію називаються, відповідно, протон, дейтрон і тритон. Внаслідок великого практичного значення ізотопів дейтерію і тритію, вони, на відміну від інших, отримали власні символічні позначення, відповідно D і Т.
Можна навести багато прикладів наявності ізотопів у різних хімічних елементів. Наприклад, кисень має три стабільних ізотопи:  ,
,  ,
,  ; олово має 10 стабільних ізотопів і т.д.
; олово має 10 стабільних ізотопів і т.д.
Внаслідок наявності ізотопів трапляються такі випадки, коли ядра різних хімічних елементів (ядра з різними Z) мають однакове масове число. Такі ядра називаються ізобарами.
Ізобари – це атомні ядра, що мають однакові масові числа, але різні атомні номери.
Прикладом ізобар є ядра  ,
,  ,
,  .
.
В природі зустрічаються хімічні елементи з атомними номерами Z від 1 (водень) до 92 (уран). Інші представлені в періодичній таблиці хімічні елементи (на даний час – до Z = 107) отримані штучно за допомогою ядерних реакцій. Всього відомо понад 1500 різних атомних ядер, що відрізняються або Z, або А, або і тим, і другим. З них приблизно 20% є стабільними, а решта – радіоактивні.
Радіус атомного ядра можна приблизно визначити за формулою:
 , (5.7.2)
, (5.7.2)
де R 0» 1,5 × 10 - 15 м. Оскільки об'єм ядра пропорційний кубу його радіусу, то, згідно з цією формулою, об'єм ядра пропорційний кількості нуклонів у ядрі. Отже, густина речовини у всіх ядрах приблизно однакова. Неважко підрахувати, що вона складає близько 10 17 кг/м3, тобто на багато порядків вище, ніж густина звичайної речовини (10 3 ¸10 4 кг/м3).
2. Дефект маси і енергія зв’язку
Ядра атомів – це досить стабільні утворення, здатні до тривалого існування (за винятком радіоактивних ізотопів). Це свідчить про те, що між нуклонами у ядрі є певна взаємодія, яка утримує їх разом. Енергію цієї взаємодії (енергію зв'язку ядра) можна визначити за допомогою формули Ейнштейна з теорії відносності (див. (1.178)), яка визначає зв'язок маси і енергії:
Е = тс 2, (5.7.3)
де с – швидкість світла. Точні вимірювання мас протонів, нейтронів і атомних ядер свідчать про те, що маса атомного ядра тЯ завжди менша, ніж сума мас протонів і нейтронів, які входять до складу ядра. Ця різниця називається дефектом маси ядра:
 (5.7.4)
(5.7.4)
Згідно з раніше прийнятими позначеннями,
 , (5.4.5)
, (5.4.5)
 (5.4.6)
(5.4.6)
Тому  (5.4.7)
(5.4.7)
Дефект маси обумовлений тим, що при об’єднанні окремих нуклонів у єдине ядро загальна енергія цієї системи часток зменшилась на певну величину, яка і називається енергією зв'язку. Якби такого зменшення не відбувалось, об’єднання нуклонів було б енергетично невигідним, і ядро не могло б існувати як стабільна квантова система. Згідно з формулою Ейнштейна (5.7.3), зменшення енергії системи обов'язково супроводжується відповідним зменшенням її маси. Звідси енергія зв'язку ядра:
 (5.4.8)
(5.4.8)
Але знання енергії зв'язку ще не дає відповіді на питання, наскільки міцно зв'язані один з одним нуклони всередині ядра. Для цього необхідно знати питому енергію зв'язку  , що визначає, яка енергія зв'язку припадає на один нуклон. Для визначення питомої енергії зв'язку необхідно загальну енергію зв'язку ядра поділити на кількість нуклонів, тобто на масове число:
, що визначає, яка енергія зв'язку припадає на один нуклон. Для визначення питомої енергії зв'язку необхідно загальну енергію зв'язку ядра поділити на кількість нуклонів, тобто на масове число:
 (5.4.9)
(5.4.9)
Ця величина характеризує стійкість атомних ядер, їх здатність зберігати цілісність у випадку дії зовнішніх чинників, які намагаються їх зруйнувати.
Як показують обчислення, питома енергія зв'язку залежить від масового числа А. Графік залежності  (А) (Рис. 5.4.1) свідчить про те, що найбільш стійкими є ядра з масовими числами А = 50 ¸ 60 (тобто для ділянки періодичної таблиці хімічних елементів від Cr до Zn). Питома енергія зв'язку для цих елементів досягає 8,7 МеВ/нуклон. При подальшому зростанні масового числа
(А) (Рис. 5.4.1) свідчить про те, що найбільш стійкими є ядра з масовими числами А = 50 ¸ 60 (тобто для ділянки періодичної таблиці хімічних елементів від Cr до Zn). Питома енергія зв'язку для цих елементів досягає 8,7 МеВ/нуклон. При подальшому зростанні масового числа  поступово зменшується, і для найважчого природного елементу (урану) складає близько 7,5 МеВ/нуклон.
поступово зменшується, і для найважчого природного елементу (урану) складає близько 7,5 МеВ/нуклон.
Таким чином, енергетично вигідними є такі процеси: 1) поділ важких ядер на більш легкі (для А > 60), 2) злиття легких ядер з утворенням більш важких (для А < 50). Під час процесів такого типу звільняється величезна кількість енергії. Так, наприклад, при поділі одного ядра з масовим числом 240 ( = 7,5 МеВ) на два ядра з масовими числами 120 (
= 7,5 МеВ) на два ядра з масовими числами 120 ( = 8,5 МеВ) звільнилась би загальна енергія 240 МеВ. Злиття двох ядер дейтерію в ядро гелію привело б до звільнення енергії 24 МеВ. Якщо порівняти ці процеси зі звичайними хімічними реакціями, то виявиться, що енергетична ефективність ядерних реакцій у мільйони разів вища. Наприклад, при згорянні вугілля відбувається хімічна реакція окислення вуглецю. При з’єднанні одного атому вуглецю з двома атомами кисню (утворення СО 2) звільняється енергія близько 5 еВ.
= 8,5 МеВ) звільнилась би загальна енергія 240 МеВ. Злиття двох ядер дейтерію в ядро гелію привело б до звільнення енергії 24 МеВ. Якщо порівняти ці процеси зі звичайними хімічними реакціями, то виявиться, що енергетична ефективність ядерних реакцій у мільйони разів вища. Наприклад, при згорянні вугілля відбувається хімічна реакція окислення вуглецю. При з’єднанні одного атому вуглецю з двома атомами кисню (утворення СО 2) звільняється енергія близько 5 еВ.


МеВ
 | |||
 |
Рис. 5.4.1 30 60 90 120 150 А
Більш детально процеси взаємодії атомних ядер (реакції поділу ядер та термоядерні реакції) будуть розглянуті нижче.
3. Ядерні сили
До складу атомних ядер входять позитивно заряджені протони, які взаємно відштовхуються за рахунок кулонівської взаємодії. Той факт, що ядро все ж зберігає свою цілісність, свідчить про те, що, крім електростатичних, між нуклонами всередині ядра діють також інші сили, сили взаємного притягнення, величина яких є значно вищою, порівняно з кулонівською. Це не можуть бути гравітаційні сили, оскільки простий підрахунок показує, що гравітаційна взаємодія занадто слабка, щоб пояснити притягнення нуклонів. Не можна пояснити цю взаємодію і за допомогою магнітного поля. Таким чином, два вже відомих нам силових поля (електромагнітне і гравітаційне) не в змозі пояснити природу сил взаємодії нуклонів всередині атомних ядер.
Отже, можна зробити логічний висновок, що існує ще один тип силового поля, величина якого всередині ядер значно перевищує гравітаційне і електромагнітне. Це силове поле називається полем сильної взаємодії. Внаслідок наявності цього поля, між нуклонами всередині ядра діють ядерні сили. Аналіз властивостей атомних ядер дозволяє визначити такі характерні риси ядерних сил:
1) Ядерні сили є короткодіючими і діють лише на відстанях, що не перевищують 10 -15 м.
2) Ядерні сили є силами притягнення; але на відстанях, суттєво менших від 10 -15 м, притягнення перетворюється на відштовхування, завдяки чому нуклони утримуються один від одного на певних відстанях, близько 10 -15 м.
3) Ядерні сили не залежать від електричного заряду нуклонів. Взаємодія між протоном і протоном, протоном і нейтроном, нейтроном і нейтроном є однаковою.
В 1930-х роках була створена теорія ядерних сил (теорія поля сильної взаємодії), яка пізніше отримала експериментальне підтвердження. Згідно з цією теорією, поле сильної взаємодії обумовлене тим, що нуклони всередині ядра здійснюють взаємообмін віртуальними (уявними) частками, які називаються p -мезонами. Маса цих часток була спочатку визначена теоретично на основі відомої величини радіусу дії ядерних сил. Самі ж ці частки, p -мезони, були виявлені експериментально значно пізніше, у 1947 р., в складі космічних променів.
Точна теорія атомного ядра на даний час ще не створена. Перепоною на шляху її створення є те, що до складу ядра входить велика кількість часток, які взаємодіють між собою, а тому кожна частка перебуває одночасно під впливом багатьох сил, що змінюються в залежності від руху часток. Задача такого типу (задача багатьох тіл) поки що не має точного розв’язку. Крім того, недостатньо розроблена теорія сил взаємодії між нуклонами.
В той же час, розроблено ряд моделей атомного ядра, які мають наближений характер, але дозволяють виконувати деякі розрахунки процесів у ядрах. Найбільш відомими серед них є такі:
1) Краплева модель ядра основана на аналогії між поведінкою нуклонів у ядрі і молекул у краплі рідини. При цьому сила взаємодії нуклонів аналогічна поверхневому натягу рідини і також є короткодіючою. Ще однією спільною рисою є те, що густина часток в обох випадках практично не залежить від зовнішніх умов (нестисливість рідини). На основі краплевої моделі були пояснені характерні особливості деяких процесів, що відбуваються в атомних ядрах, наприклад, процесів поділу важких ядер.
2) Оболонкова модель ядра розглядає ядро як квантову систему, всередині якої нуклони знаходяться у певних енергетичних станах (оболонках), які заповнюються згідно з принципом Паулі. Оболонкова модель є більш досконалою, порівняно з краплевою. На основі цієї моделі можна розрахувати спіни та магнітні моменти ядер, їх стійкість, енергетичний стан та інші характеристики.
| <== предыдущая лекция | | | следующая лекция ==> |
| Рух вільної частинки | | | I. Методика как учебная дисциплина |
Не нашли, что искали? Воспользуйтесь поиском: