
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
ФІЗИКА АТОМНОГО ЯДРА
Основні формули
1. Число протонів в ядрі (також порядковий номер елементу) прийнято позначати через Z, число нейтронів – через N. Їх сума A = Z + N називається масовим числом ядра. Атоми з однаковим Z (тобто атоми одного і того ж елементу), але з різними N називаються ізотопами, з однаковими A, але з різними Z – ізобарами.
2. Основна відмінність між протоном і нейтроном полягає в тому, що протон – заряджена частинка, заряд якої e = 1,602×10−19 Кл. Це елементарний заряд, чисельно рівний заряду електрона. Нейтрон же, як і показує його назва, електрично нейтральний. Спіни протона і нейтрона однакові і рівні спіну електрона, тобто 1/2 (в одиницях ћ зведеної сталої Планка). Маси протона і нейтрона майже рівні: 1836,15 і 1838,68 мас електрона, відповідно.
3. Протон і нейтрон не є елементарними частинками. Вони складаються з двох типів кварків – d -кварка із зарядом -1/3 і u -кварка із зарядом +2/3 від елементарного заряду е. Протон складається з двох u -кварків і одного d -кварка (сумарний заряд +1), а нейтрон з одного u -кварка і двох d -кварків (сумарний заряд – 0). Вільний нейтрон – частинка нестабільна. Він розпадається через 15 хвилин після свого виникнення на протон, електрон і антинейтрино. В ядрі нейтрон знаходиться в глибокій потенціальній ямі, тому його розпад може бути заборонений законами збереження.
4. Позначення ядер  ,
,
де Х – хімічний символ елементу;
А – масове число (число нуклонів у ядрі);
Z – зарядове число (число протонів).
5. Закон радіоактивного розпаду
N = Noe-  t,
t,
де N – число ядер, які не розпалися на момент часу t;
N o – число ядер у початковий момент часу (t = 0);
 – постійна розпаду.
– постійна розпаду.
6. Залежність періоду піврозпаду Т від постійної розпаду
Т 
7. Число ядер, які розпалися за час t
 .
.
У випадку, якщо інтервал часу  t набагато менший періоду піврозпаду Т, то
t набагато менший періоду піврозпаду Т, то
 .
.
8. Середній час життя  радіоактивного ядра
радіоактивного ядра

9. Число атомів (ядер) N, які перебувають у радіоактивному ізотопі довільної маси m
N =  ,
,
де m – маса ізотопу;
 – молярна маса;
– молярна маса;
NA – постійна Авогадро.
10. Активність А радіоактивного ізотопу
А = -  ,
,
де dN – число ядер, що розпалися за інтервал часу dt;
А о – активність ізотопу в початковий момент часу.
У системі СІ одиницею активності радіоактивної речовини є бекерель (Бк),
1Бк = 1розпад/с.
Позасистемною одиницею активності є кюрі (Кі) 1Кі= 3,7.1010 Бк.
Таку активність має 1 г чистого ізотопу радію-226.
11. Дефект маси ядра
 m = Zmp + (А-Z)mn - mя,
m = Zmp + (А-Z)mn - mя,
де mp – маса протона;
mn – маса нейтрона;
mя – маса ядра.
12. Енергія зв'язку нуклонів у ядрі
Езв . =  m.с2,
m.с2,
де 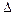 m – дефект маси ядра;
m – дефект маси ядра;
с – швидкість світла у вакуумі.
У позасистемних одиницях енергія зв'язку ядра дорівнює
Езв = 931,4.  m МеВ,
m МеВ,
де  m – дефект маси, виражений в а.о.м.;
m – дефект маси, виражений в а.о.м.;
931,4 – коефіцієнт пропорційності (1 а.о.м. ~ 931,4 Мев).
Не нашли, что искали? Воспользуйтесь поиском: