
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Методичні вказівки. В процесі різних хімічних виробництв для добування того чи іншого продукту використовують речовини (сировину)
В процесі різних хімічних виробництв для добування того чи іншого продукту використовують речовини (сировину), які не завжди бувають чистими речовинами, а можуть містити різні домішки. Ці домішки не будуть утворювати в процесі виробництва потрібні продукти, тому для визначення маси чи об'єму продукту, що добувається, необхідно спочатку розрахувати масу чи об'єм чистої речовини, яка вступає в реакцію і міститься в вихідній суміші, а вже потім розв'язувати основну (базову) задачу за рівнянням реакції.
Вміст домішок виражають в процентах або в частках одиниці. Ця величина показує масову частку чистої речовини або масову частку домішок в зразку. Для обчислення маси чистої речовини чи домішок, що містяться в суміші, використовують формулу:
w(чист. р-ни) = 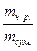
m(ч.р.) = m(сум) × w(ч.р.)
Масу чистої речовини (як і об'єм) можна обчислювати також іншим способом; визначити спочатку масу домішок, а потім відняти її від маси суміші:
m(домішок) = m (cуміші) × w(домішок)
m(ч.р.) = m(суміші) – m(домішок)
Задача 1. На завод доставлено 50т фосфориту, що містить 35% пустої породи. Обчисліть масу чистого фосфату кальція.
Розв'язування:
Чистого фосфату кальція в руді було 65% (100 - 35%), інакше w(пустої породи) = 0,35; а w (Са3(РО4)2) = 0,65.
m (Са3(РО4)2) = 50т × 0,65 = 32,5т
Або m (cуміші) = 50т × 0,35 = 17,5
Тоді m (Са(РО4)2) = 50т - 17,5т = 32,5т
Відповідь: m Са3(РО4)2 = 32,5т.
Задача 2. При взаємодії 10,8г кальцинованої соди (безводний карбонат натрія) з надлишком хлоридної кислоти одержали 2,24л (при н.у.) оксиду карбона (IV). Обчисліть вміст домішок в соді.
 Розв’язування:
Розв’язування:
m (соди) = 10,8 г Для обчислення вмісту домішок в соді, потрібно
V(СО2) = 2,24 л розрахувати масу соди. Для цього визначають масу
М(Na2CO3) = 106 г/моль карбонату натрія, що прореагував, за рівнянням.
Vm = 22,4 л/моль Na2CO3 + 2HCI = 2NaCI + H2O + CO2
 За рівнянням:
За рівнянням:
w (домішок) -? m (Na2CO3) = 1моль × 106 г/моль = 106г
V(CO2) = 1моль × 22,4л/моль = 22,4л
Далі розв'язування буде таким:
1-й спосіб (спосіб порівняння)
2,24 л < 22,4 л в 10 раз, тобто, і карбонату натрію знаходиться в 10 раз менше, тобто m (Na2CO3) = 10,6 г. Соди ж було взято 10,8 г, звідси:
m(домішок) = 10,8 – 10,6 = 0,2 г
w (домішок) = 0,2: 10,8 = 0,018 або 1,8%
Відповідь: вміст домішок в соді 1,8%.
І1-й спосіб
По формулі: n = 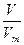 знаходимо u(СО2):
знаходимо u(СО2):
n(СО2) = 2,24: 22,4 = 0,1моль
Згідно з рівнянням реакції для добування 0,1моль СО2 потрібно 0,1моль Na2CO3.
m(Na2CO3) = 106г/моль × 0,1моль = 10,6г.
w(Na2CO3) = 10,6: 10,8 = 0,982
w (домішок) = 1 - 0,982 = 0,018 або 1,8%
Відповідь: вміст домішок в соді 1,8%.
Завдання для самостійної роботи
1. Обчисліть масу фосфора який потрібно взяти для добування 200 кг ортофосфатної кислоти, якщо масова частка виходу кислоти складає 0,9.
2. Який об'єм при нормальних умовах сірчистого газу утворюється при прожарюванні цинкової обманки, що містить 80% сульфіду цинка.
3. Визначити об'єм оксиду карбону (ІV) (н.у.), який можна добути з вапняка масою 0,5т (масова частка СаСО3 у вапняку складае 95%).
4. До суміші газоподібних оксиду карбону (ІІ) і оксиду карбону (ІV) додали надлишок кисню. Суміш спалили. Об'єм газової суміші зменшився на 10 мл. Обчисліть об'ємну частку оксиду карбону (ІV) в вихідній газовій суміші. Всі об'єми приведені до нормальних умов.
Не нашли, что искали? Воспользуйтесь поиском: