
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Властивості кристалічних речовин
Кристалічні речовини мають характерні властивості, які зумовлені внутрішньою будовою кристалів. До таких властивостей відносять: однорідність, анізотропність, здатність до самообмеження, певні фізичні константи, пов'язані з руйнуванням кристалічних ґраток (наприклад, температура плавлення).
Однорідність. Ця властивість проявляється в тому, що два однакових елементарних обсяги кристалічної речовини, однаково орієнтовані в просторі, але вирізані в різних місцях цієї речовини, абсолютно однакові за всіма своїми властивостями і мають однаковий колір, питому вагу, твердість, теплопровідність, електропровідність та ін.
Необхідно мати на увазі, що реальні кристалічні речовини дуже часто містять постійні домішки й включення, що спотворюють їхні кристалічні ґратки, тому абсолютної однорідності в реальних кристалах часто не буває.
Анізотропність. При вивченні кристалічних ґраток можна переконатися, що відстань між складовими її частками в паралельних і непаралельних рядах різні; фізичні властивості кристалів (міцність, крихкість, твердість, величина теплового розширення, швидкість проходження різних хвиль, теплопровідність, електропровідність і ін.) проявляються залежно від напрямку рядів ґраток: для горизонтальних рядів вони можуть мати одне значення, для вертикальних - інше. Це явище називається анізотропністю, або нерівно-притаманністю, на противагу ізотропності (рівно-притаманності). У речовин, що характеризуються ізотропністю, фізичні властивості в усіх напрямках проявляються однаково.
Дискретність внутрішньої будови означає, що властивості кристала не можуть бути однаковими там, де частка є, і там, де частки немає, або в місцях, у яких розташовані частки різних сортів. Однак для опису багатьох властивостей кристала досить обмежитися розглядом обсягів значно більших, ніж власний обсяг частки, і значно менших, ніж обсяг кристала в цілому. Саме в такому розумінні розглядають кристал як середовище суцільне й однорідне.
Здатність до самообмеження - властивість кристалів утворювати грані при їхньому вільному росту. Так, якщо виточену з будь-якої кристалічної речовини кульку, наприклад повареної солі, помістити в її перенасичений розчин, то через якийсь час ця кулька набуде форми куба. На противагу цьому скляна кулька не змінить своєї форми, тому що аморфна речовина не може самообмежуватися.
Здатність до самообмеження, тобто набувати багатогранної форми в результаті вільного росту у відповідному середовищі, характерна тільки для кристалічних речовин.
Постійна точка плавлення. Якщо нагрівати кристалічне тіло, то температура його буде підвищуватися до певної межі; при подальшому нагріванні речовина почне плавитися, а температура на якийсь час залишиться постійною, тому що все тепло піде на руйнування кристалічних ґраток. Температура, при якій починається плавлення, називається температурою плавлення.
Якщо підвищення температури аморфних і кристалічних речовин зобразити графічно, то для аморфних тіл крива нагрівання буде мати плавний характер; для кристалічних тіл крива нагрівання буде мати ламаний характер, де горизонтальна ділянка відповідає температурі плавлення (рисунок 1.6).
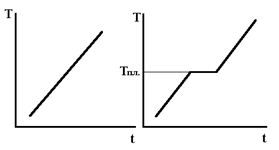
|
Аморфні тіла
Рентгеноструктурні дослідження дозволили встановити, що існують і такі тверді тіла, у яких частинки розташовані зовсім безладно, подібно до того, як це спостерігається в рідинах або газах. Такі тіла називаються аморфними, тобто безформними, оскільки на відміну від кристалічних вони не утворюють багатогранників. До аморфних належать мінеральні тіла, фізичні властивості яких у всіх напрямках однакові. Аморфність твердих мінералів чітко проявляється в процесі їхнього росту - вони ростуть в усі сторони з однаковою швидкістю, у результаті чого в остаточному підсумку (в ідеальних умовах) утворюють шароподібне тіло. Такі елементи структури, як грані, ребра й вершини, у них відсутні.
У них взаємне розташування структурних одиниць характеризується наявністю порядку тільки у взаємному розташуванні найближчих сусідів - так званий ближній порядок, у той час як тверді тіла - кристали - мають, крім того, також дальній порядок, тобто строгу періодичність в розташуванні частинок, що складають кристал. Цікаво, що ті самі речовини в багатьох випадках можуть бути й кристалічними, й аморфними. Так, наприклад, із цукрового розплаву може утворитися кристалічний цукор, якщо розплав буде застигати повільно, і цукор-льодяник, якщо той самий розплав буде застигати швидко.
Отже, головна відмінність кристалічної речовини від аморфної полягає в тому, що її атоми, іони або молекули розташовуються в просторі закономірно в певному порядку, а в аморфної - безладно.
Не нашли, что искали? Воспользуйтесь поиском: