
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Орґанічні ліґанди: аміни
C2H7NO, H2N‑CH2‑CH2‑OH, 2‑аміноетанол
| H+ lg K H = { | 9,498, 9,62 [ I = 0,5] | |||
| Ag+ lg b1 ={ | 3,2 3,13 [ I = 0,5] | lg b2 ={ | 6,76 6,68 [ I = 0,5] | |
Cd2+ lg b1 = 2,77 lg b2 = 4,09 lg b3 = 5,6 [ I = 0,1]
Cu2+ lg b1 = 5,7 lg b2 = 9,8 lg b3 = 13,0 lg b4 = 15,2 [ I = 0,1]
| Hg2+ lg b1 = { | 8,56 8,52 [ I = 0,5] | lg b2 = { | 17,33 17,32 [ I = 0,5] |
| Ni2+ lg b1 = { | 2,98 [ I = 0,1] 3,06 [ I = 0,4] | lg b2 = { | 5,33 [ I = 0,1] 5,52 [ I = 0,4] |
| lg b3 = { | 7,33 [ I = 0,1] 6,95 [ I = 0,4] |
C2H7NO, H2N‑CH2‑CH2‑OH, 2‑аміноетанол (продовження)
Pb2+ lg b1 = 7,56 [ I = 0,1]
Zn2+ lg b1 = 3,7 lg b2 = 6,1 lg b3 = 9,4 [ I = 0,1]
C2H8N2, H2N‑CH2‑CH2‑NH2, En, етилендіамін
| H+ lg K H1 = { | 9,928 10,18 | lg K H2 = { | 6,848, 7,45 |
Ag+ lg b1 = 4,70 lg b2 = 7,70
lg K (AgEn+ + H+ Û AgHEn2+) = 7,68
lg K (AgEn+ + Ag+ Û Ag2En2+) = 1,8
lg K (2 AgEn+ Û Ag2En22+) = 3,8 [20 oC, I = 0,1]
| Cd2+ lg b1 = { | 5,41 5,62 | lg b2 = { | 9,91 10,21 | |
| lg b3 = { | 11,74 [ I = 0,1] 12,30 | |||
Cu+ lg b1 = 11,2 [ I = 0,3], lg b2 = 4,09, lg b3 = 5,6 [ I = 0,1]
| Cu2+ lg b1 = { | 10,48 10,82 | lg b2 = { | 19,55 20,2 |
lg K (CuEn2+ + OH‑ Û CuEnOH+) = 0,73 [ I = 0,5]
Hg2+ lg b1 = 14,3, lg b2 = 23,24 [ I = 0,1]
lg K (HgEn2+ + OH‑ Û HgEnOH+) = 9,5
lg K (HgEn22+ + H+ Û HgHEn23+) = 5,2
lg K (HgHEn23+ + H+ Û HgH2En24+) = 3,6 [ I = 0,1]
lg K (HgCl2 + En Û HgCl2En) = 5,54 [ I = 0]
| Ni2+ lg b1 = { | 7,35 [ I = 0,1] 7,58 | lg b2 = { | 13,50 14,02 |
| lg b3 = { | 17,61 18,44 |
Pb2+ lg b1 = 7,0 [ I = 0,1] lg b2 = 8,45 [ I = 0,1]
| Zn2+ lg b1 = { | 5,66 5,92 [ I = 1,4] | lg b2 = { | 10,64 11,07 [ I = 1,4] |
| lg b3 = { | 13,89 12,93 [ I = 1,4] |
C6H18N4, H2N‑(CH2)2‑NH‑(CH2)2‑ NH‑(CH2)2‑NH2, Trien,
триетилентетрамін
| H+ lg K H1 = { | 9,74 [ I = 0,1] 10,02 | lg K H2 = { | 9,08 [ I = 0,1] 9,39 |
| lg K H3 = { | 6,56 [ I = 0,1] 7,00 | lg K H4 ={ | 3,25 [ I = 0,1] 4,00 |
Ag+ lg b1 = 4,70 lg K (AgTrien+ + H+ Û AgHTrien2+) = 8,0
lg K (AgHTrien2+ + H+ Û AgH2Trien3+) = 6,2
lg K (Ag+ + AgTrien+ Û Ag2Trien2+) = 2,4[20 oC, I = 0,1]
| Cd2+ lg b1 = { | 10,63 [ I = 0,1] 11,04 |
lg K (CdTrien2+ + H+ Û CdHTrien3+) = 6,2 [20 oC, I = 0,1]
| Cu2+ lg b1 = { | 20,1 [ I = 0,1] 20,9 |
lg K (CuTrien 2+ + H+ Û CuHTrien3+) = 3,5 [20 oC, I = 0,1]
lg K (CuTrienOH+ + H+ Û CuTrien2+ + H2O) = 10,8 [ I = 0,1]
| Hg2+ lg b1 = { | 25,1 [ I = 0,1] 25,3 [20 oC, I = 0,1] |
lg K (HgTrien2+ + H+ Û HgHTrien3+) = 5,5 [20 oC, I = 0,1]
| Ni2+ lg b1 = { | 13,8 [ I = 0,1] 14,5 | lg b2 = 18,6, lg b32 = 36,9 [ I = 0,5] |
lg K (NiTrien2+ + H+ Û NiHTrien3+) = 4,8 [ I = 0,1]
Pb2+ lg b1 = 10,4 [ I = 0,1]
| Zn2+ lg b1 = { | 12,03 [ I = 0,1] 12,05 |
lg K (ZnTrien2+ + H+ Û ZnHTrien3+) = 5,1 [ I = 0,1]
| C9H7CNO | HOxin, 8-гідроксихінолін; ліґанд C9NH6‑O‑, Oxin‑, 8-гідроксихінолінат-іон (оксинат-іон) | 
|
lg K D(HOxin Û HOxin(CHCl3)) = lg K D(HOxin Û  ) = 2,66
) = 2,66
[ I =0,1]
(реаґенти з надкресленими формулами - у розчиннику CHCl3)
| H+ lg K H1 = { | 9,81 9,58 | lg K H2 = { | 4,91 5,17 |
Ag+ lg b1 = 5,20 [20oC, I =0,1] lg b2 = 9,56 [20 oC, I =0,1]
lg K ex(Ag+ +  Û
Û  + H+) = ‑4,51 [20 oC, I =0,1]
+ H+) = ‑4,51 [20 oC, I =0,1]
Al3+ lg K s = -28,99
lg K ex(Al3+ + 3  Û
Û  + 3 H+) = ‑5,22 [20 oC, I =0,1]
+ 3 H+) = ‑5,22 [20 oC, I =0,1]
Ba2+ lg b1 = 2,07 lg Ks = ‑7,7 [ I = 0,1]
lg K D(Ba2+ + 4  Û
Û  + 2 H+) = ‑20,9 [ I =0,1]
+ 2 H+) = ‑20,9 [ I =0,1]
Bi3+ lg K ex(Bi3+ + 3  Û
Û  + 3 H+) = ‑1,2 [20 oC, I =0,1]
+ 3 H+) = ‑1,2 [20 oC, I =0,1]
Ca2+ lg b1 = 3,27 lg Ks = ‑10,4 [ I = 0,1]
lg K ex(Ca2+ + 3  Û
Û  + 2 H+) = ‑17,89
+ 2 H+) = ‑17,89
[ I =0,1]
Cd2+ lg b1 = 7,78 [20 oC]
lg K ex(Cd2+ + 2  Û
Û  + 2 H+) = 5,29
+ 2 H+) = 5,29
[20 oC, I =0,1]
Co2+ lg b1 = 8,65 lg Ks = ‑24,2 [ I = 0,1]
lg K ex(Co2+ + 3  Û
Û  + 2 H+) = ‑3,7
+ 2 H+) = ‑3,7
[20 oC, I =0,1]
lg K ex(Co2+ + 4  Û
Û  + 2 H+) = ‑2,16
+ 2 H+) = ‑2,16
[20 oC, I =0,1]
Oxin‑, оксинат-іон (продовження)
Cu2+ lg b1 = 8,65 lg Ks = ‑29,1 [ I = 0,1]
lg K ex(Cu2+ + 2  Û
Û 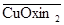 + 2 H+) = 1,77 [20 oC, I =0,1]
+ 2 H+) = 1,77 [20 oC, I =0,1]
| Fe3+ lg b1 = { | 14,52 13,0 [ I = 0,5] | lg b2 = 25,3 [ I = 0,5] |
lg b3 = 36,9 [ I = 0,5] lg Ks = ‑43,5 [ I = 0,1]
lg K ex(Fe3+ + 3  Û
Û  + 3 H+) = 4,11 [ I =0,1]
+ 3 H+) = 4,11 [ I =0,1]
| Mg2+ lg b1 = 4,74 | lg Ks = { | ‑15,4 ‑14,8 [ I = 0,1] |
lg K ex(Mg2+ + 2  Û
Û 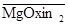 + 2 H+) = ‑15,13 [ I =0,1]
+ 2 H+) = ‑15,13 [ I =0,1]
Mn2+ lg b1 = 6,24 [ I =0,1] lg Ks = ‑21,7
lg K ex(Mn2+ + 2  Û
Û  + 2 H+) = ‑9,32 [20 oC, I =0,1]
+ 2 H+) = ‑9,32 [20 oC, I =0,1]
Ni2+ lg b1 = 9,27 lg Ks = ‑25,5 [ I = 0,1]
lg K ex(Ni2+ + 2  Û
Û  + 2 H+) = ‑2,18
+ 2 H+) = ‑2,18
[20 oC, I =0,1]
lg K ex(Ni2+ + 3  Û
Û  + 2 H+) = ‑0,1
+ 2 H+) = ‑0,1
[20 oC, I =0,1]
Pb2+ lg b1 = 9,02
lg K ex(Pb2+ + 2  Û
Û  + 2 H+) = ‑8,04
+ 2 H+) = ‑8,04
[20 oC, I =0,1]
Sr2+ lg b1 = 2,56 lg Ks = ‑8,7 [ I = 0,1]
lg K ex(Sr2+ + 4  Û
Û 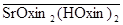 + 2 H+) =
+ 2 H+) =
= ‑19,71 [20 oC, I =0,1]
Zn2+ lg b1 = 8,52 [20oC, I=0,1] lg b2 = 15,8 lg Ks = ‑23,7 [ I = 0,1]
lg K ex(Zn2+ + 3  Û
Û  + 2 H+) = ‑7,8
+ 2 H+) = ‑7,8
[30 oC, I =0,1]
lg K ex(Zn2+ + 4  Û
Û 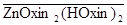 + 2 H+) = ‑2,16
+ 2 H+) = ‑2,16
[30 oC, I =0,1]
| C10H8N2 | Bipy, біпіридил | 
| ||
| H+ lg K H1 = { | 4,35 4,67 | lg K H2 = 1,5 [ I =0,1] | ||
Cd2+ lg b1 = 4,18 [ I =0,1], lg b2 = 7,7 [ I =0,1], lg b3 = 10,3 [ I =0,1]
Cu+ lg b1 = 12,95 [20 oC, I =0,1]
Cu2+ lg b1 = 6,33 [ I =0,1]
lg K (CuOHBipy+ + H+ Û CuBipy2+ + H2O) = 7,9 [ I =0,1]
lg K (Cu(OH)2Bipy + 2 H+ Û CuBipy2+ + 2 H2O) = 17,67 [ I =0,1]
lg K (2 CuBipy2+ + 2 H2O Û Cu2(OH)2Bipy22+ + 2 H+) = 10,81 [ I =0,1]
| Fe2+ lg b1 = { | 4,36 4,65 [20oC] | lg b2 = 7,90 [ I =0,1] |
| lg b3 = { | 17,2 [ I =0,1] 17,49 |
Fe3+ lg K (2 Fe3+ + 4 Bipy + 2 H2O Û
Û Fe2(OH)2Bipy 44+ + 2H+) = 16,29 [20 oC, I =0,1]
Hg2+ lg b1 = 9,64, lg b2 = 16,7, lg b3 = 19,5 [20 oC, I =0,1]
| Mn2+ lg b1 = { | 2,62 [ I = 0,1] 2,61 | lg b2 = { | 4,62 [ I = 0,1] 4,47 |
| lg b3 = { | 5,6 [ I = 0,1] 6,0 | ||
| Ni2+ lg b1 = { | 7,04 [ I = 0,1] 7,06 | lg b2 = { | 13,85 [ I = 0,1] 14,01 |
| lg b3 = { | 20,16 [ I = 0,1] 20,47 |
Pb2+ lg b1 = 2,9 [ I =0,1]
| Zn2+ lg b1 = { | 5,13 [ I = 0,1] 5,34 | lg b2 = { | 9,5 [ I = 0,1] 9,96 |
| lg b3 = { | 13,2 [ I = 0,1] 13,97 |
| C12H8N2 | Phen, о-фенантролін | 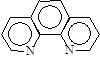
| |||
| H+ lg K H1 = { | 4,86 5,12 | lg K H2 = 1,9 [ I =0,1] | |||
Cd2+ lg b1 = 5,8 [ I =0,1], lg b2 = 10,6 [ I =0,1], lg b3 = 14,6 [ I =0,1]
Cu2+ lg b1 = 7,4 [ I =0,1]
lg K (CuPhen2+ + 2 H2O Û Cu(OH)2Phen + 2 H+) = 17,3 [ I =0,1]
lg K (2 CuPhen+ + 2 H2O Û Cu2(OH)2Phen22+ + 2 H+) = 10,69 [ I =0,1]
Fe2+ lg b1 = 5,85, lg b2 = 11,15, lg b3 = 21,0 [ I =0,1]
Fe3+ lg b1 = 6,5 lg b2 = 11,4 [20oC, I =0,1] lg b3 = 13,8
lg K (Fe2OHPhen45+ + H+ Û Fe2Phen46+ + H2O) = 6,5 [ I =0,1]
lg K (Fe2(OH)2Phen44+ + H+ Û Fe2(OH)Phen45+ + H2O) = 4,4 [ I =0,1]
Hg2+ lg b2 = 19,65 [20oC, I =0,1] lg b3 = 23,25 [20 oC, I =0,1]
Mn2+ lg b1 = 4,0 [ I =0,1] lg b2 = 7,3 [20 oC, I =0,1]
lg b3 = 10,3 [ I =0,1]
Ni2+ lg b1 = 8,6 [ I =0,1] lg b2 = 16,7 [20 oC, I =0,1]
lg b3 = 17,08 [ I =0,1]
Pb2+ lg b1 = 4,65 [ I =0,1]
Zn2+ lg b1 = 6,2 lg b2 = 12,1 lg b3 = 17,3
Не нашли, что искали? Воспользуйтесь поиском: