
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Де Dх і Dр – невизначеності у величинах відповідно координати й імпульсу.
Приклад 1. Оцініть швидкість електрона в атомі.
Розв’язання. Приймемо в співвідношенні невизначеностей D х рівною порядку розміру атома: D х»1 Å= =10-10 м. Знаходимо невизначеність імпульсу для такого стану електрона:
D р  h /2p × D х = 6,63×10-34 /2 ×3,14 × 10-10 = 1,06 × 10-24 Дж×с/м.
h /2p × D х = 6,63×10-34 /2 ×3,14 × 10-10 = 1,06 × 10-24 Дж×с/м.
Далі, враховуючи значення маси електрона (кг), знаходимо невизначеність його швидкості:
D v = D р / m ē = 1,06× 10-24/ 9,1× 10-31 = 1,16× 106 м/с.
Швидкість не може бути меншою своєї невизначеності. Отже вона більша за 1,16×106 м/с, і це значення можна оціночно прийняти за швидкість електрона в атомі. Зверніть увагу, що вона більш ніж на два порядки менша максимальної швидкості у природі – швидкості світла (с = 3×108м/с). Поясніть, чому при розгляді електронної структури атомів зневажають хвильовими властивостями ядра. Довжина хвилі якої мікрочастинки визначає розмір атома? Що таке атомна орбіталь електрона і як це поняття співвідноситься з класичним поняттям орбіти?
Стан мікрочастинки, а також системи частинок, цілком визначається хвильовою функцією Ψ (читається: "псі"). У звичайному, так званому координатному, представленні Ψ – функція, що залежить від координат і часу: Ψ = Ψ(x, y, z, t). У загальному випадку Ψ – комплексна функція, зокрема, вона може приймати позитивні і негативні дійсні значення. Фізичний зміст має квадрат модуля хвильової функції |Ψ|2 – це густина ймовірності виявлення частинки у точці з координатами x, y, z. Це означає, що ймовірність знайти частинку у деякому малому об’ємі dV дорівнює |Ψ|2× dV Хвильову функцію знаходять із розв’язання рівняння Шредингера – основного рівняння квантової механіки.
Так, для частинки масою m, що рухається у потенційному полі (наприклад, електрон у полі електричного притягання ядра атома водню), рівняння Шредингера має вигляд

 ,
,
де U – потенційна, а E – повна енергія частинки.
Як диференційне рівняння в частинних похідних, рівняння Шредингера при E < 0 (тобто якщо електрон не відірваний від атома) має не безперервний, а дискретний набір рішень: Ψ1, Ψ2, Ψ3, …. Цьому відповідає дискретний ряд (квантованість) можливих значень енергії електрона, моменту його орбітального імпульсу (кількості руху), проекції цього моменту на деякий виділений напрямок.
Квантованість станів электрона в атомі відображають квантові числа, які можна розглядати як набір номерів рішень рівняння Шредингера. Особливу увагу варто приділити фізичному змісту і можливим значенням квантових чисел (див. табл.1). Зверніть увагу на прийняті буквені позначення підрівнів.
Таблиця 1
Основні властивості квантових чисел електрона в атомі
| Квантове число | Можливе значення | Число можливих значень | Физичний зміст (що визначає квантове число) |
| Головне n | 1, 2, 3, 4… K,L,M,N... | ∞ | Енергію електрона на даному рівні. Середню відстань електрона від атомного ядра (розмір електронної хмари). Порядковий номер енерге-тичного рівня (електронної оболонки, шару). |
| Орбіталь-не (побі-чне) l | 0,1,2,...(n -1) s,р,d, f... | N | Орбітальний момент імпуль-су і магнітний момент електрона. Енергію електро-на на підрівні даного рівня багатоелектронного атома. Форму орбіталі. Енергетич-ний підрівень. |
| Магнітне ml | - l … 0 … + l | (2 l +1) | Проекцію орбітального моменту на виділений напрямок. Просторову орієн-тацію орбіталі (електронної хмари). |
| Спінове ms | +½ і -½ 
| Власний момент імпульсу і магнітний момент електрона (один із двох можливих способів “обертання” електрона). |
Проаналізувавши вміст таблиці, спробуйте відповісти на такі питання: які квантові числа та чи у однаковій мірі визначають енергію електрона в атомі? Які енергетичні рівні не мають: а) p -, б) d -, в) f - підрівнів? Чи можлива відсутність на рівнях s -підрівня? Скільки різних орієнтацій можуть мати орбіталі d- підрівня?
Кожен дозволений стан електрона в атомі характеризується конкретним набором усіх чотирьох квантових чисел. Припустимий набір перших двох квантових чисел (n і l) визначає конкретний підрівень, тобто підрівень розглянутого енергетичного рівня. При цьому використовуються буквені позначення для орбітального квантового числа (табл.1): 2 s (n =2, l =0), 2 p (n =2, l =1), 3 d (n =3, l =2).
Допустимий набір перших трьох квантових чисел однозначно визначає атомну орбіталь (АО) електрона: 

Вказуючи атомну орбіталь, до позначення підрівня додають підрядковий індекс, що показує її орієнтацію щодо осей координат і відповідає визначеному значенню ml. Якщо орієнтація спеціально не вказується, індекс опускають, наприклад, 3 d - або d -орбіталі. На графічних схемах АО позначають умовно "квантовими комірками" 1, а електрони – стрілками, що дає можливість розрізняти орієнтацію їх спінів:
 (ms = +½) та
(ms = +½) та  (ms = -½).
(ms = -½).
Приклад 2. Складіть графічну схему орбіталей 4-го енергетичного рівня.
Розв’язання. При n = 4 можливі наступні значення l = 0, 1, 2, 3. Відповідно цьому, 4-й рівень включає s-, p-, d- і f – підрівні (табл.1). Комірки, що зображують орбіталі одного підрівня, розташовуємо поруч по горизонталі, тому що енергія електронів на них однакова. Число орбіталей-комірок на підрівні дорівнює числу можливих значень ml, тобто (2 l +1) або одна на s -, три на p -, п'ять на d - і сім на f -підрівнях. Значення ml записуємо під кожною з комірок. Розв’язок виглядає в такий спосіб:
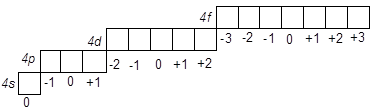
Порядок заповнення орбіталей у багатоелектронних атомах визначається двома основними принципами: принципом найменшої енергії і принципом Паулі. По першому з них, електрони в незбуджених атомах займають ті АО, на яких їх енергія найменша.
За принципом Паулі (в атомі не може бути двох електронів з однаковим набором усіх чотирьох квантових чисел) на одній орбіталі не може бути більше двох електронів. Допускаються лише такі чотири варіанти заповнення кожної окремої АО:




(вільна АО) (пара з протилежними спінами)
Звідси можна послідовно визначити електронну ємність (максимально можливе число електронів) рівнів і підрівнів (табл.2).
Таблиця 2.
Не нашли, что искали? Воспользуйтесь поиском: