
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Тема 1.6. Химические реакции
Химическая реакция – это процесс, в результате которого из одних веществ образуются другие, отличающиеся от них по составу и строению. Химические реакции можно классифицировать по следующим признакам.
1) По составу вещества:
а) реакции, идущие с изменением состава вещества (реакции соединения, разложения, замещения, обмена),
б) реакции, протекающие без изменения состава вещества.
Пример: С (графит) «С (алмаз),
3О2 (кислород) «2О3 (озон).
2) По изменению степени окисления химических элементов:
а) реакции, идущие без изменения степени окисления.
Пример:  ,
,
б) реакции, идущие с изменением степени окисления – окислительно-восстановительные (ОВР).
Пример: 2  .
.
3) По агрегатному состоянию:
а) гетерогенные – реакции, в которых реагирующие вещества и продукты реакции находятся в разных агрегатных состояниях.
Пример: СаО (тв) + СО2(г) «СаСО3(тв),
б) гомогенные – реакции, в которых все вещества находятся в одном агрегатном состоянии.
Пример: N2(г) + 3H2(г) «2NH3(г).
4) По участию катализатора:
а) некаталитические реакции, идущие без участия катализатора.
Пример:  ,
,
б) каталитические - реакции, которые идут с только участием катализатора.
5) По направлению:
а) необратимые реакции протекают только в одном направлении до полного расходования одного из исходных веществ (¯,, Н2О),
б) обратимые реакции протекают как в прямом, так и в обратном направлении.
6) По тепловому эффекту:
а) экзотермические - реакции, которые протекают с выделением теплоты Q (+Q),
б) эндотермические - реакции, которые протекают с поглощением теплоты Q (- Q).
Тепловой эффект химической реакции – количество выделенной или поглощенной в результате химической реакции теплоты.
Реакция разложения – химическая реакция, при которой из одного вещества образуется 2 или несколько новых веществ.
Реакция соединения – химические реакции, при которых из двух или нескольких веществ получается одно сложное вещество.
Реакции замещения – химические реакции, при которых атомы, составляющие простое вещество, замещают атомы одного из элементов сложного вещества.
Реакция обмена – химические реакции, при которых молекулы двух сложных веществ обмениваются атомами или атомными группами.
Скорость химических реакций (V) определяется изменением концентрации прореагировавшего или образующегося вещества в единицу времени и соответствует формуле: 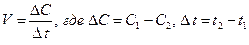 .
.

На скорость химических реакций влияют различные факторы:
1) Природа реагирующих веществ.
2) Для вещества в растворенном состоянии и газов скорость химических реакций зависит от концентрации реагирующих веществ.
3) Для веществ, находящихся в твердом состоянии, скорость реакции прямо пропорциональна поверхности реагирующих веществ.
Закон действующих масс (1867г., Гульдберг, Вааге) для гомогенных систем звучит так: при постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ.
Зависимость выражают формулой:  , где а,b – коэффициенты уравнения реакции, k – константа скорости, С – концентрации реагирующих веществ.
, где а,b – коэффициенты уравнения реакции, k – константа скорости, С – концентрации реагирующих веществ.
4) При повышении температуры на каждые 10°С скорость большинства реакций увеличивается в 2-4 раза (правило Вант – Гоффа). Зависимость выражают формулой:  , где g - температурный коэффициент скорости, т.е. число, характеризующее ускорение реакции при нагревании на 10°С.
, где g - температурный коэффициент скорости, т.е. число, характеризующее ускорение реакции при нагревании на 10°С.
5) Присутствие некоторых веществ (ингибиторы и катализаторы).
Вещества, которые ускоряют химические реакции, но сами при этом не расходуются, называют катализаторами.
Химическое равновесие – состояние системы, при котором скорость прямой реакции равна скорости обратной реакции. Зависимость отражается формулой: 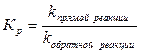 , где Кр – константа равновесия, k – константа скорости химической реакции.
, где Кр – константа равновесия, k – константа скорости химической реакции.
Если Кр = 1,  - устанавливается химическое равновесие системы.
- устанавливается химическое равновесие системы.
Если Кр > 1,  - продуктов реакции больше, чем реагентов.
- продуктов реакции больше, чем реагентов.
Если Кр < 1,  - продуктов реакции меньше, чем исходных веществ.
- продуктов реакции меньше, чем исходных веществ.
Правило смещения химического равновесия под влиянием внешних условий Ле Шателье (1884 г) звучит так:
Если на систему, находящуюся в равновесии, оказывается внешнее воздействия (изменение С, р, t), то химическое равновесие смещается в ту сторону, которая ослабляет данное воздействие.
Следствия принципа смещения химического равновесия Ле Шателье:
1) при повышении концентрации (С) реагирующего вещества равновесие смещается в сторону образования продуктов реакции;
2) при повышении давления химическое равновесие смещается в сторону той реакции, при которой объем образующихся газов уменьшается;
3) при повышении температуры химическое равновесие смещается в сторону эндотермической реакции;
4) при понижении температуры химическое равновесие смещается в сторону экзотермического процесса.
Пример 1. Определим, как сместится химическое равновесие в реакции N2+O2  2NO-Q при повышении температуры.
2NO-Q при повышении температуры. 
Согласно принципу Ле Шателье при повышении температуры химическое равновесие смещается в сторону эндотермической реакции, т.е. в данном случае - в сторону прямой реакции.
Пример 2. Определим, как сместится химическое равновесие в реакции N2+O2  2NO-Q при понижении давления.
2NO-Q при понижении давления. 
При понижении температуры химическое равновесие смещается в сторону той реакции, при которой объем образующихся газов увеличивается.
Из уравнения видно, что объёмы газов в левой и правой части уравнения одинаковые, поэтому равновесие не смещается.
Катализ – изменение скорости реакций под действием катализатора.
Гомогенный катализ – катализатор находится в таком же агрегатном состоянии, как и реагирующие вещества.
Гетерогенный катализ – агрегатные состояния катализатора и реагента различаются.
Окислительно – восстановительными реакциями (ОВР) называют реакции, которые протекают с изменением степени окисления элементов.
Восстановитель – атом или ион, который отдает электроны и окисляется. Окислитель - атом или ион, который принимает электроны и восстанавливается.
Восстановление – процесс принятия электронов. Окисление – процесс отдачи электронов.
По распределению функций окислителя и восстановителя выделяют следующие типы ОВР:
1. Межмолекулярная ОВР – реакция, в которой функции окислителя и восстановителя выполняют разные реагирующие вещества.
2. Внутримолекулярная ОВР – реакция, в которой изменение степени окисления атомов происходит в одной и той же молекуле.
3. Реакция диспропорционирования – реакция, при которой окислительные и восстановительные функции выполняют атомы одного элемента в одной и той же степени окисления.
4. Реакция конмутации – реакция, в результате которой химический элемент, окисляясь и восстанавливаясь, приобретает одинаковую степень окисления.
1. Алгоритм расчета количества теплоты по термохимическим уравнениям реакции:
1) Записать условие задачи.
2) Записать термохимическое уравнение.
3) Подписать формулы веществ известных исходных данных.
4) Над подчеркнутой формулой указать исходные данные, под формулой числовые значения.
5) Рассчитать исходное количество теплоты в кДж.
6) Записать ответ.
Пример: Вычислить, какое количество теплоты выделится при сгорании 6,2 г фосфора.
Термохимическое уравнение реакции: 4Р(тв) +5О2(газ)® 2Р2О5 (тв)+ 3010 кДж.
Дано: Решение:

 m (Р)=6,2 г 6,2г Q
m (Р)=6,2 г 6,2г Q
Найти: 4Р + 5O2 ® 2Р2O5 + 3010кДж
Q-? 4×31г\моль

Ответ: при сгорании 6,2 граммов фосфора выделяется 150,5 к Дж.
2. Алгоритм вычисления массы (m) продуктов реакции по заданному количеству исходного вещества:
1) Записать условие задачи.
2) Составить уравнение реакции.
3) Подчеркнуть формулы веществ, о которых идет речь.
4) Записать исходные данные.
5) Рассчитать количество вещества.
6) Найти М определяемого вещества, зная что [M]=Mr.
7) Используем формулу  и вычисляем массу вещества
и вычисляем массу вещества  .
.
8) Записываем ответ.
Пример: Рассчитать массу H2O, образовавшейся в результате взаимодействия 0,5 моль оксида алюминия с серной кислотой при нагревании.
 |
Дано: Решение:
 n(Al2O3)=0,5 моль 0,5моль n моль
n(Al2O3)=0,5 моль 0,5моль n моль
Найти: Al2O3 + 3H2SO4 ® Al2(SO4)3 + 3H2O
M(H2O)-? 1 моль 3 моль


Ответ: при взаимодействии оксида алюминия с серной кислотой образуется 27 граммов воды.
Задания для самоконтроля:
Задание № 1. Химической реакции в растворе отвечает уравнение: А+В=С. Как изменится скорость реакции если:
а) концентрацию А увеличить в 2 раза, оставив концентрацию В прежней,
б) концентрацию одного из веществ увеличить в 2 раза, а другого – в 2 раза уменьшить.
Задание № 2. При повышении температуры на 10ºС скорость химической реакции возрастает в 2 раза. При 20ºС она равна 0,04  . Какова будет скорость этой реакции при: а) 40ºС, б) 10ºС, в) 0ºС, г) 20ºС?
. Какова будет скорость этой реакции при: а) 40ºС, б) 10ºС, в) 0ºС, г) 20ºС?
Задание № 3. В какую сторону сместится равновесие химической системы (влево или вправо), соответствующей реакции:
2SO2+O2  2SO3+Q
2SO3+Q
а) при повышении температуры, б) при повышении давления.
Задание № 4. Вычислите, какое количество теплоты поглощается при окислении 14г азота. Термохимическое уравнение реакции окисления азота:
N2+O2=2NO-180, 8 кДж.
Задание № 5. Напишите электронные уравнения, расставьте коэффициенты и укажите восстановитель и окислитель в следующих реакциях:
а) Mg+H2SO4=MgSO4+H2, б) Zn+CuCl2=ZnCl2+Cu,
в) H2+J2=HJ, г) O2+Na2SO3=Na2SO4.
Задание № 6. Методом электронного баланса подберите коэффициенты в схемах ОВР:
а) FeCl3+KJ=FeCl2+J2+KCl,
б) S+KOH=K2S+K2SO3+H2O,
в) MnS+НNО3=MnSO4+NO2+H2O.
Не нашли, что искали? Воспользуйтесь поиском: