
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Аналогично решается задача 2б.
Задача 3а.
Приведём объём сероводорода к данной температуре с помощью уравнения Менделеева – Клапейрона: n = PV/RT = 101 325 Па * 0.258 *10-3 м3 / 8.31 Дж/моль*К/293 К = 0.011 моль. Концентрация сероводорода в насыщенном растворе тогда составит:
[H2S] = 0.011 моль / 0.1 л = 0.11 моль/л.
(5 баллов, расчёт [H2S] без приведения к заданной температуре – 1 балл)
Запишем равновесие между осадком и раствором:
FeS(т) D Fe2+ + S2-; ПР = [Fe2+] [S2-]. Условие выпадения осадка: C(Fe2+) * C(S2-) = ПР.
Отсюда [S2-] = ПР/[Fe2+] (1). (2.5 баллов)
Концентрация сульфид – ионов определяется протолизом сероводорода:
H2S + H2O D HS- + H3O+; Kк1 = [HS-] [H3O+] / [H2S] (2) (2.5 баллов) и
HS- + H2O D S2- + H3O+; Kк2 = [HS-] [H3O+] / [H2S] (3) (2.5 баллов).
Решая систему уравнений (2) и (3) относительно [S2-], получаем
[S2-] = Kк1 * Kк2 * [H2S] / [H3O+]2 или [S2-] = Kк1 * Kк2 * [H2S] / 10-2pH (4). (2.5 баллов)
Приравнивая (1) и (4), получаем
[H3O+] = (Kк1 * Kк2 * [H2S] * [Fe2+] / ПР)1/2 (5)
и pH = -1/2 lg (Kк1 * Kк2 * [H2S] * [Fe2+] / ПР) ~ 2.5
(5 баллов)
За предложенный графический способ решения – дополнительно 5 баллов.
Аналогично решается задача 3б относительно [Co2+].
Задача 4а.
Из описания опыта (цвет газов и жидкостей) следует, что речь идёт о разложении какого-либо нитрата металла. Так как выделяется смесь газов (один из которых NO2), возможны два варианта:
1. M(NO3)x = M + xNO2 + 2xO2.
Молярная масса нитрата равна Mr(нитр) = (Ar(M) + 52*x)
Из уравнения реакции имеем
Ar(M) * 18.75 = 7.95 * (Ar(M) + 52*x).
Отсюда 10.8* Ar(M) = 492,9x и Ar(M) = 45.6х. Перебор целочисленных значений х подходящих вариантов не даёт.
2. M(NO3)x = MOx/2 + xNO2 + (x – y)O2.
Молярная масса нитрата равна Mr(нитр) = (Ar(M) + 62*x), оксида – Mr(MOy) = Ar(M) + 8x.
Из уравнения реакции имеем (Ar(M) + 8x) * 18.75 = 7.95 * (Ar(M) + 62*x).
Отсюда 10.8* Ar(M) = 263.4x и Ar(M) = 31.75х. При x = 2 получаем Ar(M) = 63.5 – Cu.
(9 баллов)
Таким образом, вещество А – Cu(NO3)2 (нитрат меди (II)). (0.5+0.5 = 1 балл)
Следовательно, протекают следующие реакции:
2Cu(NO3)2 = 2CuO + 4NO2 + O2, (1 балл)
2NO2 D N2O4(ж), (1 балл)
2N2O4(ж) + H2O = N2O3(ж) + 2HNO3, (1 балл)
3N2O3(ж) + H2O = 2HNO3 + 4NO. (1 балл)
Б – NO2 (диоксид азота или оксид азота (IV)), (0.5+0.5 = 1 балл)
В - O2 (дикислород), (0.5+0.5 = 1 балл)
Г - N2O4 (тетраоксид диазота), (0.5+0.5 = 1 балл)
Д - N2O3 (триоксид диазота или оксид азота (III)), (0.5+0.5 = 1 балл)
Е - HNO3 (азотная кислота), (0.5+0.5 = 1 балл)
Ж – NO (монооксид азота или оксид азота(I)) (0.5+0.5 = 1 балл)
З – CuO (оксид меди(II)). (0.5+0.5 = 1 балл)
Строение молекул (4х1 = 4 балла)
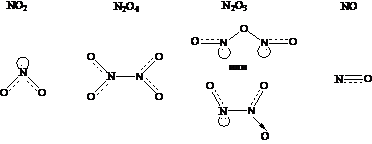
Расчёт рН.
Суммируя все уравнения реакций, получаем, что из 1 моль нитрата по двум последним реакциям образуется 1 + 1/3 = 1.33 моль азотной кислоты. Тогда из 18.75 г нитрата образуется n(HNO3) = 18.75 г / 187.5г/моль * 1.33 = 0.133 моль. Концентрация кислоты в растворе, следовательно, равна С = 0.133 моль / 0.1 л = 1.33 моль/л. Так как азотная кислота – сильная, pH = -lg (C(HNO3)) = -0.12. (5 баллов)
Аналогично задача 4б, но там разлагается нитрат серебра (I) и вещество З – Ag. Соотношение нитрата к HNO3 – 1:7/12. n(HNO3) = 0.58*17/170 = 0.058 моль.
С(HNO3) = 0.058 моль / 0.2 л = 0.29 моль/л. pH = 0.54.
Задача 5а (она же 5б)
1. Строение (2 балла)

2. Насыщенными называют растворы, находящиеся в термодинамическом равновесии с осадком растворённого вещества (1 балл).
Уравнения равновесных реакций и константы равновесий:
AgN3 (тв.) D Ag+ (р-р) + N3– (р-р); ПР = [Ag+] [N3–] = 10–8,54; (1 +1 = 2 балла)
AgIO3 (тв.) D Ag+ (р-р) + IO3- (р-р); ПР = [Ag+] [IO3-] = 10–7,52. (1 +1 = 2 балла)
Протолиз анионов:
N3– + H2O D HN3 + OH–; Kо = [HN3][OH–]/[N3–] = 10–14/Кк(HN3) = 10–4,72 = 5,25·10–10,
(1 +1 + 1= 3 балла)
IO3- + H2O D HIO3 + OH–; Kо = [HIO3][OH–]/[IO3–] = 10–14/Кк(HIO3) 10–14/10–0,79 = 6,17·10–14
(1 +1 + 1 = 3 балла)
3. Оба аниона, проявляя оснóвные свойства, подвергаются в воде протолизу (см. п. 2). Уменьшение рН раствора (т.е. подкисление) приведет к увеличению степени протолиза (т.е. к смещению равновесия вправо по принципу Ле Шателье – Брауна) и к увеличению растворимости осадков. (2 балла)
4. Запишем ещё раз уравнения равновесных процессов и константы равновесий:
AgX(т) D Ag+ + X-; ПР = [Ag+][X-].
X-+ H2O D HX + OH–; Kо = [HX][OH–]/[X–]
Без учета протолиза растворимость s = [Ag+] = [X–]. С учетом протолиза:
s = [Ag+] = [X–] + [НX].
Выразим [НX] из выражения для Ko (или Kк):
[HX] = [X-] [H+]/Kк. Тогда:
s = [X–] + [НX] = [X–] + [X-] [H+]/Kк = [X–]*(1+[H+]/Kк) = ПР/s *(1+[H+]/Kк)
(так как [X–] = ПР/[Ag+] = ПР/s).
s2 = ПР *(1+[H+]/Kк).
Отсюда ПРAgN3 *(1+[H+]/KкHN3) = ПРAgIO3 *(1+[H+]/Kк HIO3)
Решая это уравнение относительно [H+], получим:
[H+] = {К1К2*(ПР1-ПР2) / (К1*ПР2 – K2*ПР1)}
Подставив значения констант из условия, найдём:
[H+] = 1,81·10–4, рН = 3,74 (5 баллов)
Растворимость при этом значении рН составит s1 = s2 = 1,74·10–4 моль/л. (2 балла)
5. СТРОГОЕ РЕШЕНИЕ. Без учета протолиза рН = 7 и растворимость равна
s = (ПР)1/2 = 5.37*10-5.
Протолиз увеличивает растворимость соли и повышает рН насыщенного раствора. Запишем ещё раз уравнения равновесных процессов и константы равновесий:
AgX(т) D Ag+ + X-; ПР = [Ag+][X-].
X-+ H2O D HX + OH–; Kо = [HX][OH–]/[X–] = [HX]2/[X–].
С учетом протолиза s = [Ag+] = [X–] + [НX]. Из выражения для Ko получим
[HX] = (Ko*[X–])1/2. Следовательно [Ag+] = [X–] + [НX] = [X–] + (Ko*[X–])1/2.
С учетом этого выражение для ПР запишем так:
ПР = {[X–] + (Ko*[X–])1/2}* [X–] = [X–]2 + Ko1/2*[X–]3/2,
что равносильно уравнению:
[X–]4 – Ko*[X–]2 – 2ПР*[X–]2 + ПР2 = 0. (4 балла)
Подстановка Kо = 5,25·10–10 и ПР = 2,88·10–9 и решение уравнения методом последовательных приближений (в качестве первого приближения взято [N3-] = ПР1/2) даст
[N3-] = 5.42*10-5, (0.5 балла)
[НN3] = (Ко*[N3-])1/2 = 1.69*10-7, (0.5 балла)
s = [Ag+] = [N3–] + [НN3] = 5,44·10–5 моль/л, (0.5 балла)
[OH–] = [НN3] = 1,69·10–7 моль/л (0.5 балла).
[H+] = 5,92·10–8 моль/л (0.5 балла)
рН = 7,23 моль/л (0.5 балла)
ПРИБЛИЖЕННОЕ РЕШЕНИЕ. (7 баллов при тех же результатах)
Kо = [HN3][OH–]/[N3–] = [ОН]2/[N3–]. Отсюда [ОН]2 = Ко*[N3–].
Предположим, что ввиду малой константы протолиза концентрация азид-ионов изменилась не сильно. Тогда [N3–]~(ПР)1/2 и [ОН]2 = Ко*(ПР)1/2
После подстановки констант ответы практически совпадают.
И, наконец, самое приблизительное решение.
Примем, что протолиз практически не изменяет величину рН раствора, а именно рН = 7. Тогда, используя формулу, связывающую растворимость и рН, выведенную в пункте 4, получим:
s = {ПР *(1+[H+]/Kк)}1/2 = 5,38·10–5 моль/л. (3 балла)
6. По правилу Полинга HIO3 – одноосновная кислота с двуия концевыми атомами кислорода (HO)IO2 – сильная кислота. Оценочное значение pKa ≈ -3. Экспериментальное значение
pKa = -lg(10-0,79) = 0,79. Это значение можно объяснить, предполагая, что в водном растворе происходит дополнительная гидратация кислоты (образование ортоформы):
HIO3 + H2O D H3IO4
В этой форме кислота является трехосновной кислотой с одним концевым атомом кислорода (HO)3IO – кислотой средней силы pKa ≈ 2. Возможны процессы конденсации орто-формы:
n H3IO4 D (HIO3)n + n H2O.
И в этом случае каждый атом иода связан только с одним концевым атомом кислорода (остальные – мостиковые). Равновесие между такими формами может давать промежуточное
значение pKa (2 > pKa > –3). (3 балла)
Задача 6а.
1. Cl2+6КОН (гор.) = KClO3 + 5KCl + 3H2O
(за каждую ОВР - 2 балла с полуреакциями, 1 – без, за неОВР – 2 балла)
2. 3KClO3 + 3H2SO4(к) = 2ClO2(г) + HClO4 + 3KHSO4 + H2O
3. 2ClO2 + H2O = HClO3 + HClO2
4. HClO3 + KOH = KClO3 + H2O
5. HClO2 KOH = KClO2 + H2O
6. 2KClO2 + Cl2 = 2ClO2(г) + 2NaCl
7. 4 HClO4 = 4ClO2(г) + 3O2 + 2H2O (при нагревании)
8. 8HClO4 + P4O10 = 4Cl2O7 + (HPO3)4 +2H2O
9. 2Cl2O7 = 4ClO2(г) + 3O2 (при нагревании).
(за каждую ОВР - 2 балла с полуреакциями, 1 – без, за неОВР – 2 балла; итого максимум 18 баллов)
А - ClO2 (диоксид хлора или оксид хлора (IV))
Б - HClO4 (хлорная кислота)
В – HСlO3 (хлорноватая кислота)
Г – HСlO2 (хлористая кислота)
Д - КСlO2 (хлорит калия)
Е - Cl2O7 (гептаоксид дихлора или оксид хлора (VII))
(по 1 баллу за формулу и по 1 за название, итого максимум 12 баллов)
Задача 6б.
1. N2 + 3H2 = 2NH3 (на катализаторе при нагревании)
2. 2NH3 + NaClO = N2H4 + NaCl + H2O (в кислой среде, в желатине)
3. N2H4 + H[SnCl3] + 5HCl = 2NH4Cl + H2[SnCl6]
4. 2NH4Cl (т)+ Ca(OH)2 (т) = 2NH3 + CaCl2 + 2H2O
5. 5N2H4 -4e = N2 + 4N2H5+
(окислитель – любой, кроме нитритов, например, перманганат калия)
6. N2H4 + NaNO2 + H3O+ = HN3 + Na+ + 3H2O
7. HN3 + 2H+ +2e = N2 + NH3 (восстановитель – любой, например, HJ) или
2HN3 -2e = 3N2 + 2H+ (окислитель – любой)
8. 2HN3 + Pb2+ = Pb(N3)2 (т) + 2H+
9. Pb(N3)2 (т) = Pb + 3N2 (при нагревании или ударе)
10. 3HN3 + Zn = Zn(N3)2 + HN3 (г) + N2 (г)
(за каждую ОВР - 2 балла с полуреакциями, 1 – без, за неОВР – 2 балла; итого максимум 20 баллов)
А - N2 (диазот)
Б - N2H4 (гидразин, допустимо N2H5+ (ион гидразиния))
В – HN3 (азидоводород)
Г – Pb(N3)2 (азид свинца (II))
Д - NH4Cl (хлорид аммония)
(по 1 баллу за формулу и по 1 за название, итого максимум 10 баллов)
Задача 7а (она же 7б)
1. Шееле выделил кислород. (2балла)
2. Из закона эквивалентов следует:
m(Cs) / Mэ(Cs) = m(A) / Mэ(A), Mэ(Cs) = 133 * 19.39 / 80.61 = 32 г/моль, (2 балла)
m(Н) / Mэ(Н) = m(A) / Mэ(A), Mэ(Cs) = 1 * 94.12 / 80.61 = 16 г/моль. (2 балла)
Эквивалентные массы 32 и 16 г/моль могут, конечно же, отвечать элементу сере например, в соединениях Cs2S2 и H2S. Однако это противоречит указанию на газообразность простого вещества А. Таким образом, вещество А – кислород, который может помимо обычных
8 г/моль иметь и другие эквивалентные массы.
Первое соединение – надпероксид цезия CsO2, второе – пероксид водорода H2O2. (2+2 балла)
3. 2 CsO2 + H2O2 = 2 CsOH + 2O2. (3 балла)
4. Шееле использовал серную кислоту: 2MnO2 + 2H2SO4 = 2MnSO4 + O2 + 2H2O. (3 балла)
5. Оксиды: MnO2, NiO2, TcO2, ReO2и т.д. В оксидах кислород имеет степень окисления -2.
Пероксиды: CaO2, BaO2, MgO2 и т.п. В пероксидах кислород имеет степнь окисления -1.
(2+2 балла)
Не нашли, что искали? Воспользуйтесь поиском: