
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Химические свойства. На воздухе сера горит, образуя сернистый ангидрид — бесцветный газ с резким запахом:
На воздухе сера горит, образуя сернистый ангидрид — бесцветный газ с резким запахом:

С помощью спектрального анализа установлено, что на самом деле процесс окисления серы в двуокись представляет собой цепную реакцию и происходит с образованием ряда промежуточных продуктов: моноокиси серы S2O2, молекулярной серы S2, свободных атомов серы S и свободных радикалов моноокиси серы SO[6].
Восстановительные свойства серы проявляются в реакциях серы и с другими неметаллами, однако при комнатной температуре сера реагирует только со фтором:

Расплав серы реагирует с хлором, при этом возможно образование двух низших хлоридов[7]:

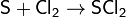
При нагревании сера также реагирует с фосфором, образуя смесь сульфидов фосфора, среди которых — высший сульфид P2S5:

Кроме того, при нагревании сера реагирует с водородом, углеродом, кремнием:
 (сероводород)
(сероводород)
 (сероуглерод)
(сероуглерод)
При нагревании сера взаимодействует со многими металлами, часто — весьма бурно. Иногда смесь металла с серой загорается при поджигании. При этом взаимодействии образуются сульфиды:



 .
.
Растворы сульфидов щелочных металлов реагируют с серой с образованием полисульфидов:
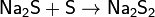
Из сложных веществ следует отметить прежде всего реакцию серы с расплавленной щёлочью, в которой сера диспропорционирует аналогично хлору:
 .
.
Полученный сплав называется серной печенью.
С концентрированными кислотами-окислителями (HNO3, H2SO4) сера реагирует только при длительном нагревании:
 (конц.)
(конц.) 
 (конц.)
(конц.) 
Хлор
Хлор (от греч. χλωρός — «зелёный») — элемент 17-й группы периодической таблицы химических элементов (поустаревшей классификации — элемент главной подгруппы VII группы), третьего периода, с атомным номером17[2]. Обозначается символом Cl (лат. Chlorum). Химически активный неметалл. Входит в группу галогенов(первоначально название «галоген» использовал немецкий химик Швейгер для хлора — дословно «галоген» переводится как солерод — но оно не прижилось и впоследствии стало общим для 17-й (VIIA) группы элементов, в которую входит и хлор[3]).
Простое вещество хлор (CAS-номер: 7782-50-5) при нормальных условиях — ядовитый газ желтовато-зелёногоцвета тяжелее воздуха, с резким запахом. Молекула хлора двухатомная (формула Cl2).
Не нашли, что искали? Воспользуйтесь поиском: