
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Теория метода и описание установки. 2.2.1 Приборы и материалы: баллон с кранами, манометр, насос.
2.2.1 Приборы и материалы: баллон с кранами, манометр, насос.
Для определения отношения теплоемкостей в данной работе используется метод, предложенный Клеманом и Дезормом. Величина 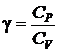 зависит от структуры молекул газа.
зависит от структуры молекул газа.
 Установка для выполнения работы этим методом состоит из стеклянного баллона А (рисунок 2.1) емкостью 15 ¸ 20 литров, соединенного с манометром В и насосом (на рисунке не показан). Через кран С баллон А соединяется с атмосферой. С помощью крана Д баллон сообщается с насосом. При открытом кране С баллон заполнен воздухом при атмосферном давлении P 0 и комнатной температуре T 0 и массой m 0, состояние 1. На диаграмме P – V (рисунок 2.2) представлена последовательность процессов при выполнении работы. Кран С закрывают и насосом накачивают
Установка для выполнения работы этим методом состоит из стеклянного баллона А (рисунок 2.1) емкостью 15 ¸ 20 литров, соединенного с манометром В и насосом (на рисунке не показан). Через кран С баллон А соединяется с атмосферой. С помощью крана Д баллон сообщается с насосом. При открытом кране С баллон заполнен воздухом при атмосферном давлении P 0 и комнатной температуре T 0 и массой m 0, состояние 1. На диаграмме P – V (рисунок 2.2) представлена последовательность процессов при выполнении работы. Кран С закрывают и насосом накачивают
Рисунок 2.1 дополнительную порцию воздуха m.
Давление в баллоне повышается до Р, так как масса газа увеличивается  , состояние 2 (PTV 1) (рисунок 2.2).
, состояние 2 (PTV 1) (рисунок 2.2).
Температура воздуха увеличивается до T потому, что внешние силы совершают работу по сжатию газа массы m0 при накачивании воздуха  . Вследствие теплообмена воздуха с окружающей средой через некоторое время (2 ¸ мин.) температура воздуха, находящегося в баллоне,сравняется с температурой внешней среды T 0. При этом по манометру можно отметить уменьшение давления воздуха. Когда температура воздуха в баллоне будет равна комнатной (показания манометра перестанут меняться), давление в баллоне станет равным
. Вследствие теплообмена воздуха с окружающей средой через некоторое время (2 ¸ мин.) температура воздуха, находящегося в баллоне,сравняется с температурой внешней среды T 0. При этом по манометру можно отметить уменьшение давления воздуха. Когда температура воздуха в баллоне будет равна комнатной (показания манометра перестанут меняться), давление в баллоне станет равным
 , (2.31)
, (2.31)
где r× g × h 1 – избыточное давление воздуха в баллоне,
r – плотность жидкости в манометре,
h 1 – разность уровней жидкости в манометре.
Это состояние 3 с параметрами (P 1 V1T 0), где V 1 – объем массы газа m 0.
Затем кран С открывается на короткое время, при этом часть воздуха выходит из баллона, и давление сравнивается с атмосферным P 0. Оставшаяся часть адиабатически расширяется, совершая работу против атмосферного давления; внутренняя энергия газа уменьшается, и температура понижается до T 1 < T 0, состояние 4 (P 0 V2T 1). Затем кран С быстро закрывают, и воздух в баллоне начинает медленно нагреваться до температуры окружающей среды T 0 – состояние 5 (P 2 V2T 0), давление при этом увеличивается до P 2.
Понятие адиабатического процесса является идеализацией, так как невозможно полностью исключить обмен теплом между газом и окружающей средой. Но процесс теплообмена идет довольно медленно, поэтому быстрое расширение газа можно рассматривать приближенно адиабатическим.
Давление в баллоне станет равным P 2:
 , (2.32)
, (2.32)
где r × g × h 2 – избыточное давление после расширения и установления температуры T 0,
h 2 – разность уровней жидкости в манометре после охлаждения до температуры T 0.
По величине измеренных на опыте давлений P 0, P 1 и P 2 можно определить соотношение теплоемкостей:
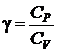 .
.
 Для этого мысленно выделим внутри баллона произвольную массу воздуха m 0, ограниченную замкнутой поверхностью, которая играет роль «оболочки». На рисунке 2.1 «оболочка» изображена пунктирной линией в рассмотренных выше процессах воздух внутри нее будет расширяться и сжиматься, совершая работу против давления окружающего воздуха и обмениваясь с ним теплом.
Для этого мысленно выделим внутри баллона произвольную массу воздуха m 0, ограниченную замкнутой поверхностью, которая играет роль «оболочки». На рисунке 2.1 «оболочка» изображена пунктирной линией в рассмотренных выше процессах воздух внутри нее будет расширяться и сжиматься, совершая работу против давления окружающего воздуха и обмениваясь с ним теплом.
Рисунок 2.2
Запишем параметры для различных состояний воздуха внутри «оболочки».
Первое состояние – после накачки воздуха и выравнивания температур (на диаграмме P – V это точка (3) рисунка 2.2):
I состояние – параметры – P 1, V 1, T 0.
Второе состояние (точка (4)) – после адиабатического расширения:
I I состояние – параметры – P 0, V 2, T 1.
Третье состояние – после закрытия крана и выравнивания температуры до T 0 – (точка (5)):
III состояние– параметры – P 2, V 2, T 0.
Разность давлений P 1– P 0 и P 2– P 1 в сотни и тысячи раз меньше атмосферного P 0, поэтому для упрощения вычислений с этими разностями можно обращаться как с бесконечно малыми величинами. То же относится и к соответствующим изменениям объема выделенной массы газа.
Переход газа из состояния I (3 – P 1 V 1 T 0) в состояние II (4 – P 0 V 2 T 1) происходит адиабатически (2.27):
 . Учитывая, что в условиях опыта изменения объемов и давлений газа малы, уравнение адиабаты (2.27) можно записать:
. Учитывая, что в условиях опыта изменения объемов и давлений газа малы, уравнение адиабаты (2.27) можно записать:
 . (2.33)
. (2.33)
В состояниях I (точка 3) и III (точка 5) на диаграмме P – V воздух имеет одинаковую температуру T 0, поэтому применяем закон Бойля-Мариотта (PV = const), запишем его в дифференциальной форме:

или
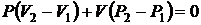 . (2.34)
. (2.34)
Решая совместно (2.33) и (2.34), имеем:
 . (2.35)
. (2.35)
Подставим в это соотношение  и
и  , получим:
, получим:
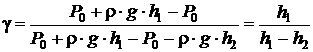 . (2.36)
. (2.36)
Так как в рабочей формуле (2.36) g выражена через отношение избыточных давлений, то измерять его можно в любых единицах. Удобнее всего выразить его в миллиметрах водяного столба по манометру.
Для определения отношения 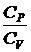 опытным путем необходимо измерить разности уровней h 1 и h 2 и, пользуясь формулой (2.36), произвести вычисления.
опытным путем необходимо измерить разности уровней h 1 и h 2 и, пользуясь формулой (2.36), произвести вычисления.
Не нашли, что искали? Воспользуйтесь поиском: