
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
ВНУТРЕННЯЯ ЭНЕРГИЯ И ТЕПЛОЕМКОСТЬ ГАЗОВ
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
ЗАДАНИЕ № 4
Укажите, в какой из приведенных единиц измерения не может быть выражена постоянная Больцмана.
ВАРИАНТЫ ОТВЕТОВ:
1) Дж/К; 2) кгм2/(с2К); 3) кгм2/(сК); 4) Нм/К; 5) эВ/К.
ЗАДАНИЕ № 5
Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя кинетическая энергия молекул азота (N2) равна...
ВАРИАНТЫ ОТВЕТОВ:
1) kT/ 2; 2) 3 kT/ 2;3)5 kT/ 2; 4) 3 kT;5) 7 kT/ 2.
ЗАДАНИЕ № 6
В классическом описании газа из N двухатомных молекул используются две возможные модели для молекулы:
1 модель 2 модель
О______О O-\/\/\/\/-О
Жесткая гантель Упpугая гантель
Какое из следующих утвеpждений веpно для этого газа?
ВАРИАНТЫ ОТВЕТОВ:
1. Удельная теплоемкость для втоpой модели меньше, чем для пеpвой модели.
2. Модель 1 всегда коppектна.
3. Модель 2 всегда коppектна.
4. Модель 1 имеет теплоемкость CV= (3/2). k.NА (k – постоянная Больцмана).
5. Выбоp модели зависит от темпеpатуpы.
---------------------------
Указания к заданиям № 4 – 6
Средняя кинетическая энергия молекулы идеального газа при температуре Т равна 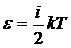 . Здесь i = пп + пвр + 2пк, где пп , пвр и пк – число степеней
. Здесь i = пп + пвр + 2пк, где пп , пвр и пк – число степеней
свободы поступательного, вращательного и колебательного движений молекулы.
Молярная теплоемкость при постоянном объеме Cv и при постоянном давлении Cp: 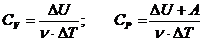 ,
,
где DU – изменение внутренней энергии; A – работа над внешними телами;
n – число молей; DT – изменение температуры.
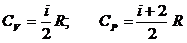 (i – число степеней свободы молекулы).
(i – число степеней свободы молекулы).
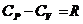 – уравнение Майера. R=kNA (NA – число Авогадро).
– уравнение Майера. R=kNA (NA – число Авогадро).
Для многоатомных молекул число степеней свободы, проявляющихся в теплоемкости газа, зависит от температуры. С повышением температуры, кроме степеней свободы поступательного движения, увеличивается роль степеней свободы вращательного и колебательного движений молекулы.
ЗАДАНИЕ № 7
Состояние идеального газа определяется значениями параметров: T0, p0, V0,
где Т – термодинамическая температура, р – давление, V – объем газа. Определенное количество газа перевели из состояния (р0, V0) в состояние
(2 р0, V o/3). При этом его внутренняя энергия...
ВАРИАНТЫ ОТВЕТОВ:
1) не изменилась; 2) уменьшилась;3) увеличилась.
---------------------------
Указания
Уравнение Клапейрона-Менделеева: 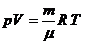 .
.
Изменение внутренней энергии идеального газа: 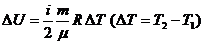 .
.
ЗАДАНИЕ № 8
Если DU – изменение внутренней энергии идеального газа, А – работа газа,
Q – количество теплоты, сообщаемое газу, то для адиабатного расширения газа справедливы соотношения...
ВАРИАНТЫ ОТВЕТОВ:
1) Q> 0; A> 0; DU= 0;
2) Q< 0; A< 0; DU= 0;
3) Q= 0; A< 0; DU> 0;
4) Q= 0; A> 0; DU< 0.
ЗАДАНИЕ № 9
Если DU – изменение внутренней энергии идеального газа, А – работа газа,
Q – количество теплоты, сообщаемое газу, то для изотермического сжатия газа справедливы соотношения...
ВАРИАНТЫ ОТВЕТОВ:
1) Q= 0; A< 0; DU> 0;
2) Q< 0; A> 0; DU= 0;
3) Q> 0; A< 0; DU< 0;
4) Q< 0; A< 0; DU= 0.
ЗАДАНИЕ № 10
Если DU – изменение внутренней энергии идеального газа, А – работа газа,
Q – количество теплоты, сообщаемое газу, то для изобарного расширения газа справедливы соотношения...
ВАРИАНТЫ ОТВЕТОВ:
1) Q= 0; A> 0; DU< 0;
2) Q> 0; A> 0; DU> 0;
3) Q< 0; A< 0; DU> 0;
4) Q> 0; A> 0; DU= 0.
ЗАДАНИЕ № 11
Если DU – изменение внутренней энергии идеального газа, А – работа газа,
Q – количество теплоты, сообщаемое газу, то для изохорного нагревания газа справедливы соотношения...
ВАРИАНТЫ ОТВЕТОВ:
1) Q= 0; A< 0; DU> 0;
2) Q< 0; A= 0; DU> 0;
3) Q> 0; A= 0; DU> 0;
4) Q > 0; A> 0; DU> 0.
---------------------------
Указания к заданиям № 8 - 11
Уравнение адиабатного (Q= 0) процесса в координатах (V, T): 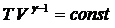 .
.
Работа при адиабатном процессе: 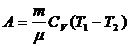 .
.
Уравнение изотермического (T=const) процесса: 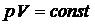 .
.
Работа при изотермическом процессе: 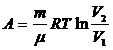 .
.
Уравнение изобарного (p=const) процесса: 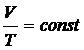 .
.
Работа при изобарном процессе: 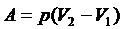 .
.
Уравнение изохорного (V=const) процесса:  .
.
Работа при изохорном процессе: 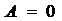 .
.
Изменение внутренней энергии: 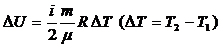 .
.
Первое начало термодинамики: 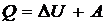 .
.
Не нашли, что искали? Воспользуйтесь поиском: