
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Изохорный процесс- это процесс, протекающий при постоянном объёме .
 (1)
(1)
 Рис.1 Диаграмма
Рис.1 Диаграмма  . Изохорный процесс
. Изохорный процесс
Работа изменения объёма газа в изохорном процессе равна нулю: 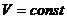 ,
,  ,
, 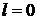 . (2)
. (2)
Так как  , то в соответствии с первым законом термодинамики
, то в соответствии с первым законом термодинамики
 (3)
(3)  (4)
(4)
Отсюда, в изохорном процессе теплота, подводимая (отводимая) к рабочему телу, идёт на изменение внутренней энергии.
Таким образом, можем записать для изменения внутренней энергии
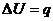
 (5)
(5)
Изобарный процесс это процесс, протекающий при постоянном давлении  . Из уравнения состояния идеального газа
. Из уравнения состояния идеального газа  следует, что
следует, что  т. е. при изобарном процессе объём газа прямо пропорционален его абсолютной температуре -закон Гей-Люссака
т. е. при изобарном процессе объём газа прямо пропорционален его абсолютной температуре -закон Гей-Люссака 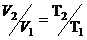 (1)
(1)
 Рис. 2
Рис. 2 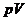 - диаграмма. Изобарный процесс
- диаграмма. Изобарный процесс
Работа изменения объёма газа в изобарном процессе будет
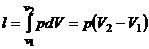 (2) или
(2) или  . (3)
. (3)
L = M p(V2 –V1) (4) L = M R(T2 –T1) (5)
количество теплоты, подведённое к рабочему телу в процессе Qp = M cp (T2 –T1) (6)
В соответствии с уравнением первого закона термодинамики 
в изобарном процессе часть теплоты, подведённой к рабочему телу, расходуется на изменение внутренней энергии, а оставшаяся часть идёт на совершение внешней работы.
Изменение внутренней энергии в процессе можно найти из соотношения  (7)
(7)
При изотермическом процессе температура рабочего тела постоянна  и, следовательно,
и, следовательно,  или
или 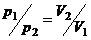 то есть давление и объём при изотермическом процессе обратно пропорциональны друг другу. Закон Бойля – Мариотта. Графиком изотермического процесса на
то есть давление и объём при изотермическом процессе обратно пропорциональны друг другу. Закон Бойля – Мариотта. Графиком изотермического процесса на 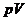 - диаграмме является равнобокая гипербола, для которой координатные оси диаграммы служат асимптотами.рис.3
- диаграмме является равнобокая гипербола, для которой координатные оси диаграммы служат асимптотами.рис.3
 Рис. 3.
Рис. 3. 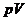 - диаграмма изотермического процесса
- диаграмма изотермического процесса
Работа при изотермическом процессе выражается формулой
 (2)
(2)
Так как температура не меняется, то внутренняя энергия идеального газа в данном процессе остаётся постоянной  ,
,  и из уравнения первого закона термодинамики
и из уравнения первого закона термодинамики
 следует, что
следует, что 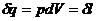 (3)
(3)  . (4)
. (4)
То есть при изотермическом процессе вся подводимая к газу теплота полностью переходит в работу расширения, а при изотермическом сжатии от газа отводится теплота в количестве, равном затраченной на сжатие работе.
Адиабатный процесс – это процесс, происходящий без теплообмена с окружающей средой, ( то есть  ).
).  (1)
(1)
Показатель адиабаты 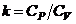 (2).
(2).
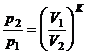 (3)
(3)  (4).
(4).  (5)
(5)
Из уравнения первого закона термодинамики 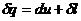 следует, так как теплообмен отсутствует, то есть
следует, так как теплообмен отсутствует, то есть  , то
, то  или для конечного изменения имеем
или для конечного изменения имеем  . (6)
. (6)
Таким образом, работа в адиабатном процессе совершается за счёт убыли внутренней энергии.
 (7)
(7)  (8)
(8)  (9)
(9)
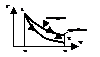
Рис. 4. Взаимное расположение адиабаты и изотермы расширения в 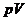 - диаграмме
- диаграмме
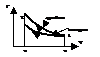
Рис. 5. Взаимное расположение адиабаты и изотермы сжатия в 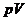 - диаграмме
- диаграмме
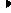
Политропный процесс  , (1)
, (1)
Показатель политропы 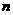 может принимать любое численное значение от 1 до
может принимать любое численное значение от 1 до  , но для данного процесса он является величиной постоянной.
, но для данного процесса он является величиной постоянной.  (2),
(2),  (3),
(3),  (4)
(4)
 (5)
(5) 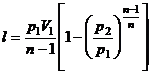 (6)
(6)  , (7)
, (7)  (8)
(8) 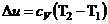 (9)
(9)  (10)
(10)
 (11) представляет собой теплоёмкость идеального газа в политропном процессе,
(11) представляет собой теплоёмкость идеального газа в политропном процессе,  (11)
(11)  (12)
(12)
Политропный процесс является обобщающим по отношению к основным обратимым термодинамическим процессам с идеальным газом. Рассмотренные выше термодинамические процессы представляют собой частные случаи политропного процесса
при  (изобарный процесс)
(изобарный процесс) 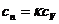 или
или  ; при
; при 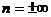 (изохорный процесс)
(изохорный процесс)  ;
;
при  (изотермический процесс)
(изотермический процесс)  ; при
; при 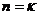 (адиабатный процесс)
(адиабатный процесс)  .
.
| <== предыдущая лекция | | | следующая лекция ==> |
| | | Классификация норм конституционного права. |
Не нашли, что искали? Воспользуйтесь поиском: