
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Приведите составы и способы тушения пожаров с участием указанного вещества.
К огнетушащим веществам относятся вещества и материалы, с помощью которых прекращается горение.
Огнетушащие вещества оказывают комбинированное воздействие на процесс горения вещества. Вода может охлаждать и изолировать источник горения; пенные средства действуют изолирующее и охлаждающе; порошковые составы изолируют и тормозят реакцию горения; наиболее эффективные газовые вещества действуют одновременно как разбавители и как тормозящие реакцию горение.
Все огнетушащие вещества в зависимости от принципа прекращения горения разделяются на виды:
ü Охлаждающие зону реакции или горючие вещества (вода, водные растворы солей, твердый диоксид углерода и др.)
ü Разбавляющие вещества в зоне реакции горения (инертные газы, водяной пар, тонкораспыленная вода, газоводяные смеси и др.)
ü
ü Изолирующие вещества от зоны горения (химическая и воздушно-механическая пены, огнетушащие порошки, негорючие сыпучие вещества и др.)
ü Химически - тормозящие реакцию горения.
Любое огнетушащее вещество обладает доминирующим свойством.
Быстро ликвидировать горение можно при правильном выборе средств и способов ликвидации горения. Для этого надо знать свойства горючих веществ и их характер горения.
Вывод: анализируя свойства вещества в можно сделать вывод, что самым оптимальным средством для тушения пожара с участием этого вещества будет являться распыленная вода, воздушно-механическая пена.
Заключение
Фталевый ангидрид - ангидрид 1,2-бензолдикарбоно-вой к-ты Представляет собой бесцветные орто-ромбичные кристаллы; легко возгоняется, плохо растворимы в этаноле и ди-этиловом эфире.Фталевый ангидрид обладает свойствами ароматических соединений. В составе фталевого ангидрида естькарбоксильная группа — одновалентная группа СООН, присутствие которой определяет принадлежность органического соединения к карбоновым кислотам в свою очередь состоящая из карбонильной -СО и гидроксильной группы - ОН.
Главным направлением использования фталевого ангидрида является применение его сложных эфиров в качестве пластификаторов и в виде алкидных смол для поверхностных покрытий. Реакция полного сгорания не возможна в реальных условиях, лишь в теории. В теории реакция будет проходить экзотермически и самопроизвольно. При полном сгорании 300 кг выделяется Q=66* 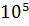 кДж теплоты. Стехиометрический коэффициент, показывающий число молей кислорода, необходимое для полного сгорания фталевого ангидрида в атмосфере кислорода и воздуха β=7,5.Фталевый ангидрид является горючим веществом, легковоспламеняющимся веществом. состоит из простых веществ, как водород, кислород и углерод. Процентное содержание углерода в веществе составляет
кДж теплоты. Стехиометрический коэффициент, показывающий число молей кислорода, необходимое для полного сгорания фталевого ангидрида в атмосфере кислорода и воздуха β=7,5.Фталевый ангидрид является горючим веществом, легковоспламеняющимся веществом. состоит из простых веществ, как водород, кислород и углерод. Процентное содержание углерода в веществе составляет 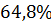 , водорода
, водорода 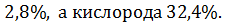 Фталевый ангидрид горит
Фталевый ангидрид горит 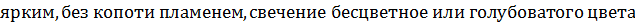
Если кислород в веществе отсутствует или его содержание не превышает 30%, но, в свою очередь, и массовая доля углерода не очень велика (менее 75%), то при термическом разложении будет выделяться значительное количество частиц углерода, но при нормальном доступе воздуха в зону горения они успевают окислиться до 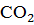 . Объём воздуха, необходимого для полного сгорания
. Объём воздуха, необходимого для полного сгорания 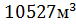 . Объем, занимаемый при t=1500˚С и Р=101325 Па равен
. Объем, занимаемый при t=1500˚С и Р=101325 Па равен 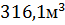 .Объем продуктов горения составляет
.Объем продуктов горения составляет 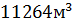 , процентное содержание
, процентное содержание 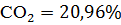 ,
,  . При полном горение вещества участвуют
. При полном горение вещества участвуют
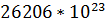 молекул воды и
молекул воды и 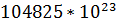 молекул
молекул  Давление насыщенного пара фталевого ангидрида
Давление насыщенного пара фталевого ангидрида 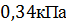 . Фталевый ангидрид получают при окислении воздухом о-ксилола или нафталина. Анализируя свойства фталевого ангидрида можно сделать вывод, что самым оптимальным средством для тушения пожара с участием этого вещества будет являться распыленная вода, воздушно-механическая пена.
. Фталевый ангидрид получают при окислении воздухом о-ксилола или нафталина. Анализируя свойства фталевого ангидрида можно сделать вывод, что самым оптимальным средством для тушения пожара с участием этого вещества будет являться распыленная вода, воздушно-механическая пена.
Список учебной литературы:
1. Антонов Н.С. Химическое оружие на рубеже двух столетий. - М.: "Прогресс", 1994. – 174 с.
3.http://www.chemweek.ru/spravka/catalog/el_577.htm
4. http://studopedia.org/1-33545.html
5. Бартенев Г.М., Зуев Ю.С., Прочность и разрушение высокоэластичных материалов. - М.: Химия, 1964. - 364 с.
6.Пупышев В.И. Современные представления о химической связи В: Современное естествознание: Энциклопедия в 10 т. – М.: Флинта: Наука, 1999-2000., т.1. Физическая химия. – 328 с.
7. Рабинович В. А., Хавин З. Я. Краткий химический справочник. - Л.: Химия, 1978
8. spravochnik-himika-tom-1-pocrb
9.Химия в интересах устойчивого развития (2011 г) ред.Новосибирский государственный университет под редакцией / А.Н.Михеев, В.Г.Макотченко.
10. Уравнения реакций обрыва - Справочник химика 21.
11. Киреев В.А. Краткий курс физической химии - М.: "Химия", 1970. - 640 с.
Не нашли, что искали? Воспользуйтесь поиском: