
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Для газа данной массы отношение объема газа к его температуре постоянно, если давление газа не меняется.
Графическое представление изобарного процесса:
- график, отражающий изобарный процесс, называется изобарой.
(математически – это линейная зависимость)
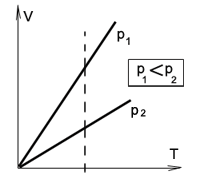
Изохорный процесс (V = const)
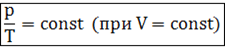 Изохорным процессом называются изменения состояния газа, протекающие при постоянном объеме.
Изохорным процессом называются изменения состояния газа, протекающие при постоянном объеме.
Изохорный процесс в идеальном газе подчиняется закону Шарля. Формула:
Графическое представление изохорного процесса:
- график, отражающий изохорный процесс, называется изохорой.
(математически – это линейная зависимость)

8)Уравнение идиального газа.
формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идиального газа.
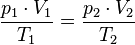
9)Внутренняя энергия идеального газа — в идиальных газах.
внутренняя энергия определяется как сумма кинетических энергий молекул. Между молекулами идеального газа отсутствуют силы притяжения и потенциальная энергия взаимодействия равна нулю. Это означает, что внутренняя энергия идеального газа рассматривается как сумма всех кинетических энергий молекул.
Если идеальный газ одноатомный, то кинетическая энергия обусловлена только поступательным движением молекулы, и ее средняя кинетическая энергия связана с температурой соотношением: E=0 2/3 kT. Где k-постоянное больцмана.
10)Применение первого закона термодинамики к идеальному газу.
При изотермическом процессе изменения внутренней энергии в идеальном газе не происходит и все подводимое к газу количество теплоты идет на совершение им работы.
Формула:
|
При изохорном процессе объем газа остается постоянным. Соответственно, не совершается работа и внутренняя энергия газа изменяется исключительно за счет теплообмена с окружающей средой.
Формула:
| V = const, Δ V = 0, A = 0, Δ U = QV. |
При изобарном процессе изменение внутренней энергии газа происходит как за счет теплообмена, так и за счет совершения механической работы. Если к газу подводится некоторое количество теплоты, то оно частично расходуется на увеличение внутренней энергии газа, частично на совершение газом работы при его расширении.
Формула:
| p = const, A = p Δ V, Qp = Δ U + p Δ V. |
11)Второй закон термодинамики
Процесс, при котором не происходит других изменений, кроме передачи теплоты от горячего тела к холодному, является необратимым, то есть теплота не может перейти от холодного тела к горячему без каких-либо других изменений в системе. Это явление называют рассеиванием или диссипацией энергии.
12)Работа в термодинамике.
При совершении работы меняется объем тела, а его скорость остается равной нулю. Нос корости молекул тела меняются! Поэтому меняется температура тела. Причина в том, что при столкновении с движущимся поршнем (сжатие газа) кинетическая энергия молекул изменяется - поршень отдает часть своей механической энергии. При столкновении с удаляющимся поршнем (расширение) скорости молекул уменьшаются, газ охлаждается. При совершении работы в термодинамике меняется состояние макроскопических тел: их объем и температура.
Геометрическое истолкование работы.
Не нашли, что искали? Воспользуйтесь поиском: