
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Водородная связь в полимерах
Много полимеров усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример - нейлон, где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина, хлопок и лён.
13.
Вандерваальсовы силы (Van-der-Vaalse force) -слабое взаимодействие между нейтральными молекулами на расстояниях, значительно превосходящих их размеры. Или: это силы взаимодействия, возникающие между электрически нейтральными атомами и молекулами и имеющие электрическую природу.(слабые силы взаимного притяжения, способствующие сцеплению между соседними АТОМАМИ или МОЛЕКУЛАМИ. Названы по имени Яна ВАН ДЕР ВААЛЬСА, который исследовал это явление в XIX в. Силы вызваны распространением электронов в соседние атомы или молекулы.)
Агрегатное состояние
Агрега́тное состоя́ние — состояние вещества, характеризующееся определёнными качественными свойствами: способностью или неспособностью сохранять объём и форму, наличием или отсутствием дальнего и ближнего порядка и другими. Изменение агрегатного состояния может сопровождаться скачкообразным изменением свободной энергии, энтропии, плотности и других основных физических свойств.
Выделяют три основных агрегатных состояния: твёрдое тело, жидкость и газ. Иногда не совсем корректно к агрегатным состояниям причисляют плазму. Существуют и другие агрегатные состояния, например, жидкие кристаллы или конденсат Бозе — Эйнштейна.
Изменения агрегатного состояния это термодинамические процессы, называемые фазовыми переходами. Выделяют следующие их разновидности: из твёрдого в жидкое — плавление; из жидкого в газообразное — испарение и кипение; из твёрдого в газообразное — сублимация; из газообразного в жидкое или твёрдое — конденсация; из жидкого в твёрдое — кристаллизация. Отличительной особенностью является отсутствие резкой границы перехода к плазменному состоянию.
Определения агрегатных состояний не всегда являются строгими. Так, существуют аморфные тела, сохраняющие структуру жидкости и обладающие небольшой текучестью и способностью сохранять форму; жидкие кристаллы текучи, но при этом обладают некоторыми свойствами твёрдых тел, в частности, могут поляризовать проходящее через них электромагнитное излучение.
Твёрдое тело
Состояние, характеризующееся способностью сохранять объём и форму. Атомы твёрдого тела совершают лишь небольшие колебания вокруг состояния равновесия. Присутствует как дальний, так и ближний порядок.
Жидкость
Состояние вещества, при котором оно обладает малой сжимаемостью, то есть хорошо сохраняет объём, однако не способно сохранять форму. Жидкость легко принимает форму сосуда, в который она помещена. Атомы или молекулы жидкости совершают колебания вблизи состояния равновесия, запертые другими атомами, и часто перескакивают на другие свободные места. Присутствует только ближний порядок.
Газ
Состояние, характеризующееся хорошей сжимаемостью, отсутствием способности сохранять как объём, так и форму. Газ стремится занять весь объём, ему предоставленный. Атомы или молекулы газа ведут себя относительно свободно, расстояния между ними гораздо больше их размеров.
Плазма
Часто причисляемая к агрегатным состояниям вещества плазма отличается от газа большой степенью ионизации атомов. Большая часть барионного вещества (по массе ок. 99,9 %) во Вселенной находится в состоянии плазмы.[2]
Сверхкритический флюид
Возникает при одновременном повышении температуры и давления до критической точки, в которой плотность газа сравнивается с плотностью жидкости; при этом исчезает граница между жидкой и газообразной фазами. Сверхкритический флюид отличается исключительно высокой растворяющей способностью.
Конденсат Бозе — Эйнштейна
Получается в результате охлаждения бозе-газа до температур, близких к абсолютному нулю. В результате этого часть атомов оказывается в состоянии со строго нулевой энергией (то есть в низшем из возможных квантовом состоянии). Конденсат Бозе — Эйнштейна проявляет ряд квантовых свойств, таких как сверхтекучесть и резонанс Фишбаха.
16.
Характерной особенностью аморфных тел является их изотропность, т. Е. Независимость всех физических свойств (механических, оптических и т. Д.) От направления внешнего воздействия. Молекулы и атомы в изотропных твердых телах располагаются хаотично, образуя лишь небольшие локальные группы, содержащие несколько частиц (ближний порядок). По своей структуре аморфные тела очень близки к жидкостям (см. §3.5). Примерами аморфных тел могут служить стекло, различные затвердевшие смолы (янтарь), пластики и т. Д. Если аморфное тело нагревать, то оно постепенно размягчается, и переход в жидкое состояние занимает значительный интервал температур.
В кристаллических телах частицы располагаются в строгом порядке, образуя пространственные периодически повторяющиеся структуры во всем объеме тела. Для наглядного представления таких структур используются пространственные кристаллические решетки, в узлах которых располагаются центры атомов или молекул данного вещества. Чаще всего кристаллическая решетка строится из ионов (положительно и отрицательно заряженных) атомов, которые входят в состав молекулы данного вещества. Например, решетка поваренной соли содержит ионы Na+ и Cl–, не объединенные попарно в молекулы nacl (рис. 3.6.1). Такие кристаллы называются ионными.
17.
Кристаллическая решётка
Составляющие данное твёрдое вещество частицы образуют кристаллическую решётку. Если кристаллические решётки стереометрически (пространственно) одинаковы или сходны (имеют одинаковую симметрию), то геометрическое различие между ними заключается, в частности, в разных расстояниях между частицами, занимающими узлы решётки. Сами расстояния между частицами называются параметрами решётки. Параметры решётки, а также углы геометрических многогранников определяются физическими методами структурного анализа, например методами рентгеновского структурного анализа.
Часто твёрдые вещества образуют (в зависимости от условий) более чем одну форму кристаллической решётки; такие формы называются полиморфными модификациями. Например, среди простых веществ известны ромбическая и моноклинная сера, графит и алмаз, которые являются гексагональной и кубической модификациями углерода, среди сложных веществ — кварц, тридимит икристобалит представляют собой различные модификации диоксида кремния.
18.
Виды кристаллов
Следует разделить идеальный и реальный кристалл.
Идеальный кристалл
Является, по сути, математическим объектом, имеющим полную, свойственную ему симметрию, идеализированно ровные гладкие грани.
Реальный кристалл
Всегда содержит различные дефекты внутренней структуры решетки, искажения и неровности на гранях и имеет пониженную симметрию многогранника вследствие специфики условий роста, неоднородности питающей среды, повреждений и деформаций. Реальный кристалл не обязательно обладает кристаллографическими гранями и правильной формой, но у него сохраняется главное свойство — закономерное положение атомов в кристаллической решётке.
Металлическая связь — химическая связь, обусловленная наличием относительно свободных электронов. Характерна как для чистых металлов, так и их сплавов и интерметаллических соединений.
19.
Дефектами кристалла называют всякое нарушение трансляционной симметрии кристалла — идеальной периодичности кристаллической решётки. Различают несколько разновидностей дефектов поразмерности. А именно, бывают нульмерные (точечные), одномерные (линейные), двумерные (плоские) и трёхмерные (объемные) дефекты.
20.
Атомно-молекулярное учение — совокупность законов и аксиом описывающих все вещества как набор молекул, состоящих из атомов. Атомно-молекулярное учение обосновал и развил русскийученый М.В.Ломоносов (корпускулярно-кинетическая теория).[1]
21.
Химия — это наука о веществах, их свойствах, строении и превращениях, происходящих в результате химических реакций, а также о фундаментальных законах, которым эти превращения подчиняются. Поскольку все вещества состоят из атомов, которые благодаря химическим связям способны формировать молекулы, то химия занимается в основном изучением взаимодействий между атомами и молекулами, полученными в результате таких взаимодействий. Моль — мера количества вещества, содержащая Число Авогадро (NA? 6,02?1023</sup) любых структурных частиц. (NA-кол-во атомов в 12 граммах углерода 12C.) Молярная масса — (г/моль) масса одного атома элемента
22.
 Закон Авога?Дро — одно из важных основных положений химии, гласящее, что «в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул». Было сформулировано ещё в 1811 году Амедео Авогадро (1776—1856), профессором физики в Турине. Закон кратных отношений — один из стехиометрических законов химии: если два вещества (простых или сложных) образуют друг с другом более одного соединения, то массы одного вещества, приходящиеся на одну и ту же массу другого вещества, относятся как целые числа, обычно небольшие. Закон постоянства состава (Ж.Л. Пруст, 1801—1808гг.) — любое определенное химически чистое соединение независимо от способа его получения состоит из одних и тех же химических элементов, причем отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами. Это один из основных законов химии.
Закон Авога?Дро — одно из важных основных положений химии, гласящее, что «в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул». Было сформулировано ещё в 1811 году Амедео Авогадро (1776—1856), профессором физики в Турине. Закон кратных отношений — один из стехиометрических законов химии: если два вещества (простых или сложных) образуют друг с другом более одного соединения, то массы одного вещества, приходящиеся на одну и ту же массу другого вещества, относятся как целые числа, обычно небольшие. Закон постоянства состава (Ж.Л. Пруст, 1801—1808гг.) — любое определенное химически чистое соединение независимо от способа его получения состоит из одних и тех же химических элементов, причем отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами. Это один из основных законов химии.
Закон постоянства состава не выполняется для бертоллидов (соединений переменного состава). Однако условно для простоты состав многих бертоллидов записывают как постоянный. Например, состав оксида железа(II) записывают в виде feo (вместо более точной формулы Fe1-xo). Закон сохранения массы — исторический закон физики, согласно которому масса как мера количества вещества сохраняется при всех природных процессах, то есть несотворима и неуничтожима. В метафизической форме закон известен с древнейших времён. Позднее появилась количественная формулировка, где в качестве меры массы объекта вначале использовался его вес.
В настоящее время известен ряд условий, при которых данный закон нарушается — например, при радиоактивном распаде совокупная масса вещества уменьшается. В современной физике закон сохранения массы является частным случаем закона сохранения энергии, и он выполняется только в консервативных физических системах, то есть при отсутствии энергообмена с внешней средой.
23.
Деление веществ на классы достаточно условно. Например, мы знаем, что кислоты подразделяются на одно-, двух- и трехосновные, но их обычно не выделяют в отдельные классы соединений. Точно также не являются отдельными классами сильные и слабые кислоты. Это же справедливо и для оснований.
Между классами существует важная связь, которую называют генетической ("генезиз" по-гречески обозначает "происхождение"). Эта связь заключается в том, что из веществ одного класса можно получить вещества других классов.
Существует два основных пути генетических связей между веществами: один из них начинается металлами, другой – неметаллами.
Например, сульфат кальция caso4 можно получить либо из металла кальция, либо другим путем – из неметалла серы
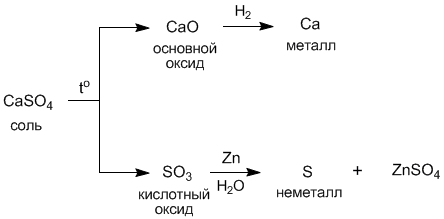 С другой стороны, из соли можно опять прийти к металлу и неметаллу:
С другой стороны, из соли можно опять прийти к металлу и неметаллу:
Одновременно существуют и другие пути взаимопревращений соединений разных классов. Таким образом, генетические связи между разными классами соединений очень многообразны.
24.
Массовая доля растворённого вещества w(B) - это безразмерная величина, равная отношению массы растворённого вещества к общей массе раствора m: w(B)= m(B) / m.
Массовую долю растворённого вещества w(B) обычно выражают в долях единицы или в процентах. Например, массовая доля растворённого вещества – cacl2 в воде равна 0,06 или 6%. Это означает,что в растворе хлорида кальция массой 100 г содержится хлорид кальция массой 6 г и вода массой 94 г.
Молярная концентрация C(B) показывает, сколько моль растворённого вещества содержится в 1 литре раствора.
C(B) = n(B) / V = m(B) / (M(B) • V), где М(B) - молярная масса растворенного вещества г/моль.
Молярная концентрация измеряется в моль/л и обозначается "M". Например, 2 M naoh - двухмолярный раствор гидроксида натрия. Один литр такого раствора содержит 2 моль вещества или 80 г (M(naoh) = 40 г/моль).
Концентрацию раствора можно выразить количеством молей растворённого вещества в 1000 г растворителя. Такое выражение концентрации называют моляльностью раствора.
Нормальность раствора обозначает число грамм-эквивалентов данного вещества в одном литре раствора или число миллиграмм-эквивалентов в одном миллилитре раствора.
Грамм - эквивалентом вещества называется количество граммов вещества, численно равное его эквиваленту. Для сложных веществ - это количество вещества, соответствующее прямо или косвенно при химических превращениях 1 грамму водорода или 8 граммам кислорода. Эоснования = Моснования / число замещаемых в реакции гидроксильных групп
Экислоты = Мкислоты / число замещаемых в реакции атомов водорода
Эсоли = Мсоли / произведение числа катионов на его заряд
25.
Способы выражения концентрации растворов.
1) Массовая доля раствора? (х). Выражается отношением массы растворенного вещества m(х) к массе раствора. 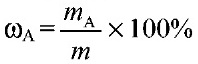
Является величиной безразмерной или выражается в процентах: 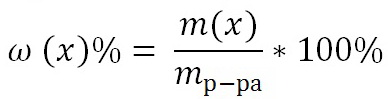
Например, 15%-ный раствор: массовая доля? (х) = 0,15
2) Молярная концентрация раствора С(х). Выражается отношением количества растворенного вещества n(x) к объему раствора, выраженному в литрах. 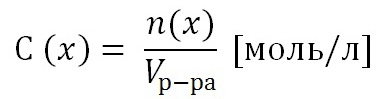
Т.к. Количество вещества n(x) выражается отношением массы вещества m(x) к его молярной массе M(x), то молярную концентрацию раствора удобно выразить как

26.
Электролиты - это вещества, которые в растворе и расплаве проводят электрический ток.
К электролитам относятся:1. Щёлочи
2. Кислоты
3. Растворимые соли
Основные положения ТЭД
1. Электролиты в растворах и расплавах распадаются на ионы "+" и "-"
Положительные ионы - катионы
Отрицательные ионы - анионы
2.Ионы отличаются от атомов стронием и свойствами.
3. Ионы в растворах и расплавах движутся хаотически, но если мы приложим напряжение, то ионы будут двигатся
Катионы -> катоду
Анионы -> аноду
27.
Электролиты. Известно, что существуют две основные причины прохождения электрического тока через проводники: либо за счет движения электронов в электрическом поле, либо за счет движения ионов. Электронная проводимость присуща, прежде всего, металлам.
Ионная проводимость присуща многим химическим соединениям, обладающим ионным строением, например солям в твердом или расплавленном состояниях, а также многим водным и неводным растворам. В связи с этим все вещества принято условно делить по их поведению в растворах на две категории: а) вещества, растворы которых обладают ионной проводимостью (электролиты); б) вещества, растворы которых не обладают ионной проводимостью (неэлектролиты). К электролитам относится большинство неорганических кислот, оснований и солей. К неэлектролитам относятся многие органические соединения, например спирты, углеводы.
Электролитическая диссоциация. Кроме хорошей электропроводности, растворы электролитов обладают более низкими значениями давления пара растворителя и температуры плавления и более высокими температурами кипения по сравнению с соответствующими значениями для чистого растворителя или для раствора неэлектролита в этом же растворителе. Для объяснения этих свойств шведский ученый С. Аррениус в 1887 г. Предложил теорию электролитической диссоциации.
Под электролитической диссоциацией понимается распад молекул электролита в растворе с образованием положительно и отрицательно заряженных ионов — катионов и анионов.
Процесс диссоциации во всех случаях является обратимым, поэтому при написании уравнений реакции диссоциации необходимо применять знак обратимости «. Различные электролиты, согласно теории Аррениуса, диссоциируют на ионы в различной степени. Полнота распада зависит от природы электролита, его концентрации, природы растворителя, температуры.
Степень диссоциации. Степенью диссоциации а называется отношение числа молекул, распавшихся на ионы (n'), к общему числу растворенных молекул (п): 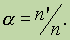
Из этого выражения очевидно, что а может изменяться от 0 (диссоциации нет) до 1 (полная диссоциация). Степень диссоциации часто выражают в процентах. Степень диссоциации электролита может быть определена только экспериментальным путем, например по измерению температуры замерзания раствора, по электропроводности раствора и т. Д.
Сильные и слабые электролиты. В зависимости от степени диссоциации различают электролиты сильные и слабые. Электролиты со степенью диссоциации больше 30% обычно называют сильными, со степенью диссоциации от 3 до 30% — средними, менее 3% — слабыми электролитами.
К сильным электролитам относятся почти все соли, некоторые кислоты (нсl, hbr, HI, НNО3, нсlo4, Н2SO4(разб.)) И некоторые основания (liон, naoh, КОН, Са(ОН)2, Sr(OH)2, Ва(ОН)2). К слабым электролитам относится большинство кислот (особенно органических) и оснований.
Степень диссоциации как сильных, так и слабых электролитов зависит от концентрации раствора (степень диссоциации тем выше, чем более разбавлен раствор).
Константа диссоциации. Более точной характеристикой диссоциации электролита является константа диссоциации, которая от концентрации раствора не зависит.
Выражение для константы диссоциации можно получить, если записать уравнение реакции диссоциации электролита АК в общем виде:
A K = A- + K+.
Поскольку диссоциация является обратимым равновесным процессом, то к этой реакции применим закон действующих масс, и можно определить константу равновесия как 
, где К — константа диссоциации, которая зависит от температуры и природы электролита и растворителя, но не зависит от концентрации электролита. Диапазон констант равновесия для разных реакций очень большой — от 10-16 до 1015. Например, высокое значение К для реакции  означает, что если в раствор, содержащий ионы серебра Ag+, внести металлическую медь, то в момент достижения равновесия концентрация ионов меди [Cu2+] намного больше, чем квадрат концентрации ионов серебра [Ag+]2. Напротив, низкое значение К в реакции
означает, что если в раствор, содержащий ионы серебра Ag+, внести металлическую медь, то в момент достижения равновесия концентрация ионов меди [Cu2+] намного больше, чем квадрат концентрации ионов серебра [Ag+]2. Напротив, низкое значение К в реакции 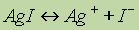 говорит о том, что к моменту достижения равновесия растворилось ничтожно малое количество иодида серебра agi.
говорит о том, что к моменту достижения равновесия растворилось ничтожно малое количество иодида серебра agi.
Если концентрации некоторых реагентов существенно не изменяются в процессе реакции, то они не записываются в выражение для константы равновесия (такие константы обозначаются К1).
Константы диссоциации малорастворимых солей и гидроксидов металлов называются произведением растворимости соответствующих веществ (обозначается ПР).
Для реакции диссоциации воды
Выражение константы будет:
, а не
Объясняется это тем, что концентрация воды во время реакций в водных растворах изменяется очень незначительно. Поэтому принимается, что концентрация [Н2О] остается постоянной и вводится в константу равновесия.
28.
Реакции между ионами в растворах электролитов идут практически до конца в сторону образования осадков, газов и слабых электролитов.
Следовательно, реакции идут с образованием веществ с меньшей концентрацией ионов в растворе в соответствии с законом действующих масс. Скорость прямой реакции пропорциональна произведению концентраций ионов реагирующих компонентов, а скорость обратной реакции пропорциональна произведению концентраций ионов продуктов. Но при образовании газов, осадков и слабых электролитов ионы связываются (уходят из раствора) и скорость обратной реакции уменьшается.
29.
Гидро?Лиз (от др.-греч.???? — вода и????? — разложение) — один из видов химических реакций сольволиза, где при взаимодействии веществ с водой происходит разложение исходного вещества с образованием новых соединений. Механизм гидролиза соединений различных классов: соли, углеводы, белки, сложные эфиры, жиры и др. Имеет существенные различия.
Гидролиз солей — разновидность реакций гидролиза, обусловленного протеканием реакций ионного обмена в растворах (преимущественно, водных) растворимых солей-электролитов. Движущей силой процесса является взаимодействие ионов с водой, приводящее к образованию слабого электролита в ионном или (реже) молекулярном виде («связывание ионов»
Различают обратимый и необратимый гидролиз солей[1]:
? 1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону):
CO32? + H2O = HCO3? + OH?
Na2CO3 + Н2О = nahco3 + naoh
(раствор имеет слабощелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
? 2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону):
Cu2+ + Н2О = cuoh+ + Н+
Cucl2 + Н2О = cuohcl + hcl
(раствор имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
? 3. Гидролиз соли слабой кислоты и слабого основания:
2Al3+ + 3S2? + 6Н2О = 2Al(OH)3(осадок) + ЗН2S(газ)
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
(равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа).
Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален.
Степень гидролиза
Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается? (или hгидр);
? = (cгидр/cобщ)•100 %
Где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли.
Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Является количественной характеристикой гидролиза.
30.
ТЕОРИЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ.
После открытия кислорода, французскому химику Лавуазье удалось выяснить, что горение есть реакция соединения с кислородом. В соответствии латинским наименованием кислорода "oxigenium" реакции соединения с кислородом были названы окислением.
2Mg0 +O20=2Mg+2O-2
Обратный процесс полного или частичного отнятия кислорода от веществ называется восстановлением. При восстановлении оксида элемент, соединённый с кислородом, меняет своё состояние - образует простое вещество, т.е. Восстанавливается.
Fe2+3O3-2+2Al0=Al2+3O3-2+2Fe0
Вы заметили, что в этих реакциях изменились степени окисления химических элементов. Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вешества, называют окислительно-восстановительными реакциями.
В соответствиии с теорией электронного строения атома окисление и восстановление легко объясняется как процесс отдачи или присоединения электронов. В окислительно-восстановительных реакциях электроны не уходят из сферы реакции, а переносятся от одного элемента к другому.
Рассмотрим реакцию взаимодействия магния с кислородом.
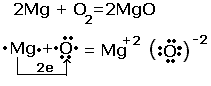
Из схемы видно, что атом магния отдал 2 электрона атому кислорода, за счёт такого перехода химические элементы изменили степени окисления. Протекают два процесса. Процесс отдачи электронов и процесс их присоединения, которые называются соответственно окислением и восстановлением.
Вещества, участвующие в окислительно-восстановительных реакциях, и у которых изменились степени окисления, являются либо окислителямия,либо восстановителями.
Окислитель - это атомы, ионы или молекулы, которые принимают электроны.
Восстановитель - это атомы, ионы или молекулы, которые отдают электроны.
Из уравнения реакции видно, что магний является восстановителем, а кислород - окислителем.
32.
Окислительно-восстановительные свойства вещества и степени окисления входящих в него атомов
Соединения, содержащие атомы элементов с максимальной степенью окисления, могут быть только окислителями за счет этих атомов, т.к. Они уже отдали все свои валентные электроны и способны только принимать электроны. Максимальная степень окисления атома элемента равна номеру группы в периодической таблице, к которой относится данный элемент. Соединения, содержащие атомы элементов с минимальной степенью окисления могут служить только восстановителями, поскольку они способны лишь отдавать электроны, потому, что внешний энергетический уровень у таких атомов завершен восемью электронами. Минимальная степень окисления у атомов металлов равна 0, для неметаллов - (n–8) (где n- номер группы в периодической системе). Соединения, содержащие атомы элементов с промежуточной степенью окисления, могут быть и окислителями и восстановителями, в зависимости от партнера, с которым взаимодействуют и от условий реакции.
Важнейшие восстановители и окислители
Восстановители: Металлы,водород, уголь. Окись углерода (II) (CO). Сероводород (H2S); оксид серы (IV) (SO2); сернистая кислота H2SO3 и ее соли. Галогеноводородные кислоты и их соли. Катионы металлов в низших степенях окисления: sncl2, fecl2, mnso4, Cr2(SO4)3. Азотистая кислота HNO2; аммиак NH3; гидразин NH2NH2; оксид азота(II) (NO). Катод при электролизе.
Окислтели: Галогены. Перманганат калия(kmno4); манганат калия (k2mno4); оксид марганца (IV) (mno2). Дихромат калия (K2Cr2O7); хромат калия (k2cro4). Азотная кислота (HNO3). Серная кислота (H2SO4) конц. Оксид меди(II) (cuo); оксид свинца(IV) (pbo2); оксид серебра (Ag2O);
пероксид водорода (H2O2). Хлорид железа(III) (fecl3). Бертоллетова соль (kclo3). Анод при электролизе.
Степень окисления - это условный заряд атома в молекуле, вычисленный в предположении, что молекула состоит из ионов и в целом электронейтральна. Наиболее электроотрицательные элементы в соединении имеют отрицательные степени окисления, а атомы элементов с меньшей электроотрицательностью - положительные.
Степень окисления - формальное понятие; в ряде случаев степень окисления не совпадает с валентностью.
Реакции без и с изменением степени окисления
Существует два типа химических реакций:
A Реакции, в которых не изменяется степень окисления элементов:
Реакции присоединения SO2 + Na2O ® Na2SO3
Реакции разложения Cu(OH)2 –t°® cuo + H2O
Реакции обмена agno3 + kcl ® agcl¯ + KNO3
naoh + HNO3 ® nano3 + H2O
B Реакции, в которых происходит изменение степеней окисления атомов элементов, входящих в состав реагирующих соединений:
2Mg0 + O20 ® 2Mg+2O-2
2kcl+5O3-2 –t°® 2kcl-1 + 3O20
2KI-1 + Cl20 ® 2kcl-1 + I20
Mn+4O2 + 4hcl-1 ® Mn+2Cl2 + Cl20 + 2H2O
Такие реакции называются окислительно - восстановительными.
В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс отдачи электронов - окисление. При окислении степень окисления повышается:
Процесс присоединения электронов - восстановление: При восстановлении степень окисления понижается.
Атомы или ионы, которые в данной реакции присоединяют электроны являются окислителями, а которые отдают электроны - восстановителями.
33.
Окислительно-восстановительный потенциал (ОВП) является мерой химической активности элементов или их соединений в обратимых химических процессах, связанных с изменением заряда ионов в растворах.
В зависимости от значения ОВП различают несколько основных ситуаций, встречающихся в природных водах:
Окислительная. Характеризуется значениями Еh > + (100 - 150) мв, присутствием в воде свободного кислорода, а также целого ряда элементов в высшей форме своей валентности (Fe3+, Mo6+, As5-, V5+, U6+, Sr4+, Cu2+, Pb2+). Ситуация, наиболее часто встречающаяся в поверхностных водах.
Переходная окислительно-восстановительная. Определяется величинами Еh от 0 до + 100 мв, неустойчивым геохимическим режимом и переменным содержанием сероводорода и кислорода. В этих условиях протекает как слабое окисление, так и слабое восстановление целого ряда металлов;
Восстановительная. Характеризуется значениями Еh < 0. Типична для подземных вод, где присутствуют металлы низких степеней валентности (Fe2+, Mn2+, Mo4+, V4+, U4+), а также сероводород.
Направление окислительно-восстановительных реакций определяется выигрышем энергии Гиббса.
Направление окислительно-восстановительных реакций во многом зависит от среды.
Предвидеть направление окислительно-восстановительной реакции можно с некоторой уверенностью лишь в том случае, если активный окислитель реагирует с активным восстановителем
При определении направления окислительно-восстановительных реакций пользуются следующим правилом: реакции окисления-восстановления всегда идут в сторону образования более слабых окислителя и восстановителя, но не наоборот.
34.
Составление уравнений окислительно-восстановительных реакций
A.Электронный баланс - метод нахождения коэффициентов в уравнениях окислительно-восстановительных реакций, в котором рассматривается обмен электронами между атомами элементов, изменяющих свою степень окисления. Число электронов, отданное восстановителем равно числу электронов, получаемых окислителем.
Уравнение составляется в несколько стадий:
1. Записывают схему реакции.
Kmno4 + hcl ® kcl + mncl2 + Cl2 + H2O
2. Проставляют степени окисления над знаками элементов, которые меняются.
Kmn+7O4 + hcl-1 ® kcl + Mn+2Cl2 + Cl20 + H2O
3. Выделяют элементы, изменяющие степени окисления и определяют число электронов, приобретенных окислителем и отдаваемых восстановителем.
Mn+7 + 5ē ® Mn+2
2Cl-1 - 2ē ® Cl20
4. Уравнивают число приобретенных и отдаваемых электронов, устанавливая тем самым коэффициенты для соединений, в которых присутствуют элементы, изменяющие степень окисления.
Mn+7 + 5ē ® Mn+2 2
2Cl-1 - 2ē ® Cl20 5
––––––––––––––––––––––––
2Mn+7 + 10Cl-1 ® 2Mn+2 + 5Cl20
5. Подбирают коэффициенты для всех остальных участников реакции.
2kmn+7O4 + 16hcl-1 ® 2kcl + 2Mn+2Cl2 + 5Cl20 + 8H2O
B. Электронно-ионный баланс (метод полуреакций) метод нахождения коэффициентов, в котором рассматривается обмен электронами между ионами в растворе с учетом характера среды:
2Cl1- – 2ē ® Cl20 5
Mno41- + 8H++ 5ē ® Mn2+ + 4H2O 2
7+ 2+
––––––––––––––––––––––––––––––––––––––
10Cl- + 2mno41- + 16H+ ® 5Cl20 + 2Mn2+ + 8H2O
(для уравнивания ионной полуреакции используют H+, OH- или воду)
35.
Эквивалентом называют реальную или условную частицу вещества, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или в данной окислительно-восстановительной реакции — одному электрону. Фактором эквивалентности служит число, обозначающее долю реальной частицы вещества, эквивалентной одному иону водорода в данной кислотно-основной реакции, или одному электрону в данной окислительно-восстановительной реакции. Фактор эквивалентности может быть равен или меньше единицы. Молярная масса эквивалента (ММЭ) вещества — масса одного моля эквивалента этого вещества, равная произведению фактора эквивалентности на его молярную массу. В соответствии с законом эквивалентов массы взаимодействующих без остатка веществ пропорциональны их эквивалентам.
36.
Эквивалентом элемента или вещества является такое ег количество в молях, которое соединяется с однм молем водорода или замещает то же количество атомов водорода в химических реакциях.
Масса одного эквивалента вещества (элемента), выраженная в граммах, называется молярной массой эквивалента вещества Мэ и выражается в г/моль. Молярная масса эквивалента элемента в соединении не является величиной постоянной,зависит от валентности элемента в данном соединении.
| Частица | Фактор эквивалентности | Примеры |
| Элемент | 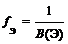 ,
Где В (Э) – валентность элемента ,
Где В (Э) – валентность элемента
| 

|
| Простое вещество | 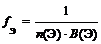 ,
Где n (Э) – число атомов элемента (индекс в химической формуле), В (Э) – валентность элемента ,
Где n (Э) – число атомов элемента (индекс в химической формуле), В (Э) – валентность элемента
| F э(H2) = 1/(21) = 1/2; F э(O2) = 1/(22) = 1/4; F э(Cl2) = 1/(21) = 1/2; F э(O3) = 1/(32) = 1/6 |
| Оксид | 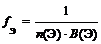 ,
Где n (Э) – число атомов элемента (индекс в химической формуле оксида), В (Э) – валентность элемента ,
Где n (Э) – число атомов элемента (индекс в химической формуле оксида), В (Э) – валентность элемента
| F э(Cr2O3) = 1/(23) = 1/6; F э(cro) = 1/(12) = 1/2; F э(H2O) = 1/(21) = 1/2; F э(P2O5) = 1/(25) = 1/10 |
| Кислота |  ,
Где n (H+) – число отданных в ходе реакции ионов водорода (основность кислоты) ,
Где n (H+) – число отданных в ходе реакции ионов водорода (основность кислоты)
| F э(H2SO4) = 1/1 = 1 (основность равна 1) Или F э(H2SO4) = 1/2 (основность равна 2) |
| Основание |  ,
Где n (ОH–) – число отданных в ходе реакции гидроксид-ионов (кислотность основания) ,
Где n (ОH–) – число отданных в ходе реакции гидроксид-ионов (кислотность основания)
| F э(Cu(OH)2) = 1/1 = 1 (кислотность равна 1) или F э(Cu(OH)2) = 1/2 (кислотность равна 2) |
| Соль | 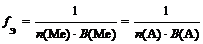 ,
Где n (Ме) – число атомов металла (индекс в химической формуле соли), В (Ме) – валентность металла; n (А) – число кислотных остатков, В (А) – валентность кислотного остатка ,
Где n (Ме) – число атомов металла (индекс в химической формуле соли), В (Ме) – валентность металла; n (А) – число кислотных остатков, В (А) – валентность кислотного остатка
| F э(Cr2(SO4)3) = 1/(23) = 1/6 (расчет по металлу) или F э(Cr2(SO4)3) = 1/(32) = 1/6 (расчет по кислотному остатку) |
| Частица в окислительно-восстановительных реакциях | 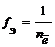 ,
Где ,
Где 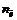 – число электронов, участвующих в процессе окисления или восстановления – число электронов, участвующих в процессе окисления или восстановления
| Fe2+ + 2  Fe0
F э(Fe2+) =1/2;
Mno4– + 8H+ + 5 Fe0
F э(Fe2+) =1/2;
Mno4– + 8H+ + 5  Mn2+ + 4H2O
F э(mno4–) = 1/5 Mn2+ + 4H2O
F э(mno4–) = 1/5
|
| Ион | 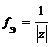 ,
Где z – заряд иона ,
Где z – заряд иона
| F э(SO42–) = 1/2 |
Современная формулировка закона: вещества реагируют и образуются согласно их эквивалентам. Все вещества в уравнении реакции связаны законом эквивалентов, поэтому:
| э(реагента1) = … = э(реагента n) = э(продукта1) = … = э(продукта n) |
Из закона эквивалентов следует, что массы (или объемы) реагирующих и образующихся веществ пропорциональны молярным массам (молярным объемам) их эквивалентов. Для любых двух веществ, связанных законом эквивалентов, можно записать:
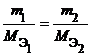 или или 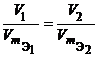 или или 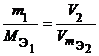 , ,
|
 ,
, 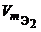 – молярные объемы эквивалентов реагентов и (или) продуктов реакции, л/моль.
– молярные объемы эквивалентов реагентов и (или) продуктов реакции, л/моль.
37.
Растворимость веществ. По растворимости в воде все вещества делятся на три группы: 1) хорошо растворимые, 2) малорастворимые и 3) практически нерастворимые. Последние называют также нерастворимыми веществами. Однако следует отметить, что абсолютно нерастворимых веществ нет. Если опустить в воду стеклянную палочку или кусочек золота или серебра, то они в ничтожно малых количествах все же растворяются в воде. Как известно, растворы серебра или золота в воде убивают микробов. Стекло, серебро, золото - это примеры практически нерастворимых в воде веществ (твердые вещества). К ним следует также отнести керосин, растительное масло (жидкие вещества), благородные газы (газообразные вещества).
Примером малорастворимых в воде веществ могут служить гипс, сульфат свинца (твердые вещества), диэтиловый эфир, бензол (жидкие вещества), метан, азот, кислород (газообразные вещества).
Многие вещества в воде растворяются весьма хорошо. Примером таких веществ могут служить сахар, медный купорос, гидроксид натрия (твердые вещества), спирт, ацетон (жидкие вещества), хлороводород, аммиак (газообразные вещества).
Из приведенных примеров следует, что растворимость прежде всего зависит от природы веществ. Кроме того, она зависит также от температуры и давления. Сам процесс растворения обусловлен взаимодействием частиц растворимого вещества и растворителя; это самопроизвольный процесс.
По соотношению преобладания числа частиц, переходящих в раствор и удаляющихся из раствора, различают растворы насыщенные, ненасыщенные и пересыщенные. С другой стороны, по относительным количествам растворенного вещества и растворителя растворы подразделяют на разбавленные и концентрированные.
Раствор, в котором данное вещество при данной температуре больше не растворяется, т. Е. Раствор, находящийся в равновесии с растворяемым веществом, называют насыщенным, а раствор, в котором еще можно растворить добавочное количество данного вещества, — ненасыщенным.
Отношение массы вещества, образующего насыщенный раствор при данной температуре, к массе растворителя называют растворимостью этого вещества, или коэффициентом растворимости:
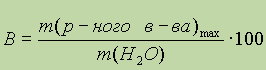
38.
Качественный анализ – раздел аналитической химии, посвященный установлению качественного состава веществ, то есть обнаружению элементов и образуемых ими ионов, входящих в состав и простых, и сложных веществ. Делают это с помощью химических реакций, характерных для данного катиона или аниона, позволяющих обнаружить их как в индивидуальных веществах, так и в смесях. Химические реакции, пригодные для качественного анализа, должны сопровождаться заметным внешним эффектом.
Это может быть
• выделение газа • изменение окраски раствора • выпадение осадка • растворение осадка • образование кристаллов характерной формы.
Результат качественного химического анализа - принятие решения о наличии или отсутствии искомого компонента в веществе объекта анализа.
• Химические методы качественного химического анализа объекта анализа – основанына проведении химических реакций с реагентом, дающим визуально наблюдаемый эффект – выпадение осадка, изменение окраски объекта, выделение газа, окрашивание пламени горелки:
• ∆ T
• 1. Pb2+ + KI → pbi↓ + K+ → pbi↓ + K+
• Желт. Желт.-золотист.
• Осадок кристаллы
• 4. Окрашивание б/цв пламени ионами К+ и Ga3+ в бледно-фиолетовый цвет и ионами Na+ в желтый цвет
• -- темно-красный цвет ионами Sr2+
• -- кирпично-красный цвет ионами Ca2+
• -- кармино-красный (малиновый) цвет ионами лития, стронция
• --желто-зеленый цвет ионами Ba2+, молибдена
• -- зелено-голубойцвет ионами Cu2+
• -- зелёный цвет ионами бора
• -- изумрудно-зелёный цвет ионами таллия, теллура
• -- синий цвет ионами In3+ и Tl+, сурьмы, мышьяка, свинца, селена
• -- бледно-фиолетовый цвет ионами К+ -- фиолет.-синий цвет ионами цезия
• -- сине-фиолетовый цвет ионами рубидия
39.
Количественный анализ — совокупность методов аналитической химии для определения количества (содержания) элементов (ионов), радикалов, функциональных групп, соединений или фаз в анализируемом объекте.
• Результат количественного химического анализа – значение количества определяемого (искомого) компонента или его массы, отнесенное к единице массы или объёма вещества объекта анализа.
• w (А) = [m (А)/ mвещ] × 100, %.
• Сm(А) = m (А)/ Vм.к. ,г/дм3
• Цели количественного анализа
• Количественный анализ позволяет установить элементный и молекулярный состав исследуемого объекта или содержание отдельных его компонентов.
• В зависимости от объекта исследования различают неорганический и органический анализ. В свою очередь их разделяют на элементарный анализ, задача которого — установить, в каком количестве содержатся элементы (ионы) в анализируемом объекте, на молекулярный и функциональный анализы, дающие ответ о количественном содержании радикалов, соединений, а также функциональных групп атомов в анализируемом объекте.
40.
Гравиметрический анализ (весовой анализ) — важнейший метод количественного химического анализа, в котором взвешивание является не только начальной, но и конечной стадией определения. Гравиметрический анализ основан на законе сохранения массы веществ при химических превращениях. Измерительным прибором служат аналитические весы. Результаты анализа выражают обычно в процентах. Гравиметрический анализ сыграл большую роль при становлении закона постоянства состава химических соединений, закона кратных отношений, периодического закона и др., применяется при определении химического состава различных объектов (горных пород и минералов), при установлении качества сырья и готовой продукции и т. Д.
• Методы гравиметрии -- проводят химическую реакцию с реагентом, вступающим в химическую реакцию с определяемым компонентом в строго определенных соотношениях (стехиометрично), и имеется возможность точно измерить массу образующегося продукта реакции.
• Например, содержание сульфатов в породе может быть определено после соответствующей пробоподготовки методом гравиметрии, где использовано свойство сульфатов образовывать малорастворимое соединение с ионами Ва2+
• SO42- + васl2 = ваso4↓ + 2Сl-
• Расчеты содержания неизвестного компонента производят на основе закона сохранения массы (количества) компонента при химических взаимодействиях.
• M(SO42 -) = M (SO42-) m( ва so42-)/ M (ваso42-)
• Пример: Руды железные. Гравиметрический метод определения окиси кальция и окиси магния
Титриметрический анализ (титрование) — методы количественного анализа в аналитической и фармацевтической химии, основанные на измерении объема раствора реактива известной концентрации, расходуемого для реакции с определяемым веществом.
Титриметрический анализ использует различные типы химических реакций:
§ Нейтрализации (кислотно-основное титрование) — нейтрализация — это реакции с изменением ph растворов.
§ Окисления-восстановления (перманганатометрия, иодометрия, хроматометрия) — реакции, которые происходят с изменением окислительно-восстановительных потенциалов в системе титрования.
§ Осаждения (аргентометрия) — реакции, протекающие с образованием малорастворимого соединения, при этом изменяются концентрации осаждаемых ионов в растворе.
§ Комплексообразования (комплексонометрия) — реакции, основанные на образовании прочных комплексных соединений ионов металлов (всех, кроме одновалентных) с комплексоном III (двунатриевой солью этилендиаминтетрауксусной кислоты), при этом изменяются концентрации ионов металлов в титруемом растворе.
- 1) методы титриметрии:
- -- проводят химическую реакцию с точно определённым (косвенно измеренным ) количеством реагента, вступающим в химическую реакцию с определяемым компонентом без побочных реакций, без остатка, в строго определенных соотношениях (стехиометрично).
- Aa + bb = cc + dd
- Реакция может быть переписана в условных единицах – эквивалентах, для которых стехиометрические коэффициенты для всех участников реакции равны 1. В этом случае можно приравнять число частиц всех составляющих реакции друг другу:
- Nэ( А ) = nэ(В) = nэ(С ) = nэ(D )
- - это запись закона эквивалентов или принципа эквивалентности.
- Тип применяемой химической реакции в титриметрии обусловлен химическими свойствами определяемого компонента. Условные частицы – эквиваленты устанавливаются для каждого типа химической реакции по своим правилам.
- Например, железо в руде может быть определено после соответствующей подготовки пробы методом перманганатометрии (окислительно-восстановительного титрования), где использованы окислительно-восстановительные свойства железа и марганца:
- 5Fe2+ + mno4- + 8H- =
- Расчеты содержания неизвестного компонента производят на основе закона эквивалентов:
Nэ( Fe2+ ) = nэ( mno4- ) → Cэ ( Fe2+ ) V( Fe2+ ) = Cэ( mno4- ) V( mno4- )
Калориметрические методы применяются в настоящее время для надежного и точного пассивного неразрушающего анализа ядерных материалов, особенно плутония и трития.
Ниже приведены важные характеристики и преимущества калориметрического анализа:
- может быть исследован весь образец;
- анализ не зависит от геометрии образца (существенно только время достижения теплового равновесия);
- анализ не зависит от состава и распределения материала матрицы, включая концентрацию влаги;
- анализ не зависит от распределения ядерного материала в образце с учетом эффектов самоэкранирования образца.
- измерение электрического тока и потенциалов осуществляется с использованием эталонных материалов;
- калориметрический анализ применим для широкого круга форм материалов (включая металлы, сплавы, оксиды, смешанные оксиды, отходы и скрап). Не требуются представительные плутониевые стандарты;
- калориметрический анализ сравним по сходимости и точности с химическим анализом, если хорошо определен изотопный состав;
- калориметрический анализ позволяет создать законченную процедуру неразрушающего анализа, когда он дополнен высокоразрешающим гамма- спектрометрическим изотопным анализом.
Важным недостатком калориметрического анализа являются значительные временные затраты на его реализацию. Вообще методика является более точной, но менее быстрой и менее портативной, чем методики неразрушающего анализа, которые применимы для измерений ядерного материала.
41.
Электрохимические методы анализа — группа методов количественного химического анализа, основанные на использованииэлектролиза.
Разновидностями метода являются электрогравиметрический анализ (электроанализ), внутренний электролиз, контактный обмен металлов (цементация), полярографический анализ, кулонометрия и др. В частности, электрогравиметрический анализ основан на взвешивании вещества, выделяющемся на одном из электродов. Метод позволяет не только проводить количественные определения меди, никеля, свинца и др., но и разделять смеси веществ.
Кроме того, к электрохимическим методам анализа относят методы, основанные на измерении электропроводности (кондуктометрия) или потенциала электрода (потенциометрия). Некоторые электрохимические методы применяются для нахождения конечной точкититрования (амперометрическое титрование, кондуктометрическое титрование, потенциометрическое титрование, кулонометрическое титрование).
К оптическим методам анализа относят физико-химические методы, основанные на взаимодействии электромагнитного излучения с веществом. Это взаимодействие приводит к различным энергетическим переходам, которые регистрируются экспериментально в виде поглощения излучения, отражения и рассеяния электромагнитного излучения. Оптические методы включают в себя большую группу спектральных методов анализа.
В методах атомной спектроскопии мы имеем дело с узкими линейчатыми спектрами, а в методах молекулярной спектроскопии – с широкими слабоструктурированными спектрами. Это определяет возможность их применения в количественном анализе и требования, предъявляемые к измерительной аппаратуре – спектральным приборам.
Хроматография широко применяется в лабораториях и в промышленности для качественного и количественного анализа многокомпонентных систем, контроля производства, особенно в связи с автоматизацией многих процессов, а также для препаративного (в т. Ч. Промышленного) выделения индивидуальных веществ (например, благородных металлов), разделения редких и рассеянных элементов.
В некоторых случаях для идентификации веществ используется хроматография в сочетании с другими физико-химическими и физическими методами, например с масс-спектрометрией, ИК-, УФ-спектроскопией и др. Для расшифровки хроматограмм и выбора условий опыта применяют ЭВМ.
Основные достоинства хроматографического анализа:
- Экспрессность; высокая эффективность; возможность автоматизации и получение объективной информации;
- Сочетание с другими физико-химическими методами;
- Широкий интервал концентраций соединений;
- Возможность изучения физико-химических свойств соединений;
- Осуществление проведения качественного и количественного анализа;
- Применение для контроля и автоматического регулирования технологических процессов.
В зависимости от природы взаимодействия, обусловливающего распределение компонентов между элюентом и неподвижной фазой, различают следующие основные виды хроматографии - адсорбционную, распределительную, ионообменную, эксклюзионную (молекулярно-ситовую) и осадочную.
.Полимер-неорганические и органические, аморфные и кристаллические вещества, состоящие из «мономерных звеньев», соединённых в длинные макромолекулы химическими или координационными связями. Полимер — это высокомолекулярное соединение: количество мономерных звеньев в полимере (степень полимеризации) должно быть достаточно велико. Во многих случаях количество звеньев может считаться достаточным, чтобы отнести молекулу к полимерам, если при добавлении очередного мономерного звена молекулярные свойства не изменяются. Как правило, полимеры — вещества с молекулярной массой от нескольких тысяч до нескольких миллионов.
Мономер-это вещество, способное к полимеризации. Также мономерами часто называют мономерные звенья в составе полимерных молекул.
Сополимер-разновидность полимеров, цепочки молекул которых состоят из двух или более различных структурных звеньев. Различают регулярные и нерегулярные сополимеры (коих большинство). Различные структурные звенья нерегулярных сополимеров беспорядочно расположены вдоль цепочки. В регулярных же сополимерах различные структурные звенья расположены упорядоченно и, следовательно, регулярные сополимеры могут быть представлены как обычные полимеры с большими структурными звеньями.
43.
Названия полимеров
Существуют два основных способа названий полимеров.
1. Название полимера строится по названию исходного мономера с добавлением приставки " поли " (полиэтилен, полистирол и т.п.). Этот способ используется обычно для полимеров, полученных путем полимеризации.
2. Полимеру дается тривиальное название (лавсан, нитрон, найлон и т.п.), которое не отражает строения макромолекул, но удобно своей краткостью. Данный способ применяют создатели полимерных материалов (фирмы, научные и производственные коллективы).
Так, название ЛАВСАН присвоено полимеру
[–O–CH2–CH2–O–CO–C6H4–CO–]n
полиэтиленгликольтерефталат
Как сокращенное название ла боратории В ысокомолекулярных С оединений А кадемии Н аук.
44.
1. По химическому составу все полимеры подразделяются на органические, элементоорганические, неорганические.
Органические полимеры. Образованы с участием органических радикалов (CH3, C6H5, CH2). Это смолы и каучуки.
Элементоорганические полимеры. Они содержат в основной цепи органических радикалов неорганические атомы (Si, Ti, Al), сочетающиеся с органическими радикалами. В природе их нет. Искусственно полученный представитель – кремнийорганические соединения.
Неорганические полимеры. Их основу составляют оксиды Si, Al, Mg, Ca и др. Углеводородный скелет отсутствует. К ним относятся керамика, слюда, асбест.
Следует отметить, что в технических материалах часто используют сочетания отдельных групп полимеров. Это композиционные материалы (например, стеклопластики).
2. По форме макромолекул полимеры делят на линейные, разветвленные, ленточные, пространственные, плоские.
45.
Благодаря ценным свойствам полимеры применяются в машиностроении, текстильной промышленности, сельском хозяйстве имедицине, автомобиле- и судостроении, авиастроении, в быту (текстильные и кожевенные изделия, посуда, клей и лаки, украшения и другие предметы). На основании высокомолекулярных соединений изготовляют резины, волокна, пластмассы, пленки и лакокрасочные покрытия. Все ткани живых организмов представляют высокомолекулярные соединения.
46.
Не нашли, что искали? Воспользуйтесь поиском: