
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Физические свойства предельных одноосновных кислот
Карбоновые кислоты
Карбоновыми кислотами называют производные углеводородов, в молекулах которых один или несколько углеродных атомов образуют карбоксильную группу или карбоксил: -C-OH, или –COOH
II
O
В этой сложной функциональной группе соединены друг с другом две простые кислородсодержащие группы: карбонильная >С=О и гидроксильная (или окси группа) –ОН; отсюда и происходит название – карбоксильная группа. Водород гидроксильной группы, входящей в карбоксильную группу, обуславливает кислотные свойства карбоновых кислот; поэтому число карбоксильных групп характеризует основность кислоты. В молекулах одноосновных (монокарбоновых) кислот – одна карбоксильная группа, двухосновных (дикарбоновых) кислот – две карбоксильные группы.
Насыщенные одноосновные кислоты
Насыщенные кислоты являются производными насыщенных углеводородов. Высшие гомологи этих кислот впервые были выделены из природных жиров, поэтому их, а затем и все другие кислоты с открытой целью углеродных атомов назвали жирными кислотами.
Строение, изомерия, номенклатура
В строении и изомерии предельных одноосновных кислот наблюдается определенная аналогия со строением и изомерией альдегидов. Мы знаем, что последние, окисляясь, превращаются в кислоты с тем же углеродным скелетом. Карбоксильная группа, как и альдегидная, может быть образована лишь первичным углеродным атомом.
Для простейших кислот широко используются тривиальные названия, происходящие от названий природных продуктов, из которых та или иная кислота была впервые получена.
Простейший представитель гомологического ряда насыщенных одноосновных кислот – муравьиная кислота, она была впервые обнаружена в выделениях муравьев, откуда и происходит ее название. В молекуле муравьиной кислоты имеется единственный углеродный атом, который и образует карбоксильную группу, соединенную с атомом водорода: Н-С-ОН
II
муравьиная кислота О
В молекулах всех других одноосновных кислот карбоксильная группа соединена не с водородом, а с тем или иным углеводородным остатком; их строение можно представить общей формулой R-C-OH
II
O
Для насыщенных одноосновных кислот более точной является общая формула CnH2n+1COOH, показывающая, что в этих кислотах карбоксил соединен с остатками насыщенных углеводородов.
Следующий за муравьиной кислотой гомолог содержит два углеродных атома и называется уксусной кислотой, т.к. впервые эта кислота была получена в виде натурального уксуса. Уксусная кислота имеет такой же углеродный скелет, как и углеводород этан. Кислота с тремя углеродными атомами по скелету аналогична пропану; она называется пропионовой кислотой:
CH3-C-OH CH3-CH2-C-OH
II II
O O
уксусная кислота пропионовая кислота
Для гомологов с большим числом углеродных атомов возможна изомерия углеродного скелета. Так, состав С3Н7-СООН (4 углеродных атома) имеют уже две изомерные по углеродному скелету кислоты, которые называют масляными кислотами:
СН3
½
СН3-СН2-СН2-С-ОН СН3-СН-С-ОН
II II
О О
масляная кислота изомасляная кислота
Кислоты состава С4Н9-СООН с пятью углеродными атомами называются валериановыми кислотами; они существуют в виде четырех изомеров (одна кислота нормального строения, т.е. с неразветвленной цепью, и три кислоты изостроения).
Наибольшее значение обычно имеют кислоты с нормальной цепью углеродных атомов. B таблице приведены тривиальные названия и формулы важнейших предельных одноосновных кислот нормального строения.
Предельные одноосные кислоты с нормальной цепью и их свойства.
| Кислота | Формула | Тпл., °С | Ткип., °С | Константы диссоциац. |
| Муравьиная | H—COOH | +8,25 | 100,5 | 21,4×10-5 |
| Уксусная | CH3—COOH | +16,6 | 118,5 | 1,76×10-5 |
| Пропионовая | CH3—CH2—COOH | -20,7 | 141,1 | 1,34×10-5 |
| Масляная | CH3—(CH2)2—COOH | -3,1 | 163,0 | 1,52×10-5 |
| Валериановая | CH3—(CH2)3—COOH | -34,5 | 186,0 | 1,50×10-5 |
| Капроновая | CH3—(CH2)4—COOH | -1,5 | 205,3 | 1,38×10-5 |
| Энантовая | CH3—(CH2)5—COOH | |||
| Лауриновая | CH3—(CH2)10—COOH | +44,3 | 225* | |
| Пальмитиновая | CH3—(CH2)14—COOH | +62,6 | 271* | |
| Маргариновая | CH3—(CH2)15—COOH | +60,8 | 277* | |
| Стеариновая | CH3—(CH2)16—COOH | +69,4 | 287* |
*При 100 мм рт.ст., т.е. при перегонке под уменьшенным давлением.
Рациональная номенклатура
Одноосновные кислоты более чем с двумя атомами углерода рассматривают как производные уксусной кислоты, образованные замещением атомов водорода в ее метильной группе углеводородного радикалами. Пропионовая кислота может быть названа метилуксусной, масляная – этилуксусная, изомасляная – диметилуксусной. Подобно альдегидам за основу рационального названия кислоты изостроения можно принять тривиальное название нормальной кислоты, соответствующей наиболее длинной цепи, включающей карбоксильный углерод. Например, изомасляная кислота может быть названа метилпропионовой.
Международная заместительная номенклатура
Кислоты называют, образуя прилагательное из заместительного названия, соответствующего по числу атомов углерода и по строению углеводорода. Так, заместительное название муравьиной кислоты–метановая кислота, уксусной - этановая, масляной – бутановая, изомасляной – 2-метилпропановая. Таким образом, для заместительных названий одноосных кислот характерно окончание – овая кислота. Нумерацию цепи всегда начинают от углерода, образующего карбоксильную группу, поэтому в названиях изомерных кислот цифру 1, относящуюся к карбоксильному углероду, не указывают. Например, два изомера валериановой кислоты по заместительной номенклатуре называют:
CH3 O O CH3
I II II I
4CH3—3CH—2CH2—1C—OH HO—1C—2CH—3CH2—4CH3
g b a a b g
3-метилбутановая к-та 2-метилбутановая к-та
3-метилбутановая кислотата иначе может быть названа изопропилуксусная или b-метилмасляная кислота, а 2-метилбутановая кислота –метилэтилуксусная или a-метилмасляная кислота. (Так должны быть названы эти кислоты по рациональной номенклатуре, если их рассматривать как производные уксусной кислоты, или если название производится от тривиального названия кислоты с нормальной цепью.)
Кислотные остатки
Остатки кислот, образованные отнятием гидроксильной группы карбоксила, общего строения R-C= O называют кислотными или ацильными
I
(от латинского слова acidum – кислота) остатками (ацилами). Названия их производят из корня латинского тривиального названия кислоты и окончания – ил. Так, остаток муравьиной кислоты (лат. acidum formicicum) называется формилом, уксусной (acidum aceficum) – ацетилом и т.д. Ниже сопоставлены важнейшие кислоты с формулами и названиями их остатков – ацилов:
| Кислота | Остаток | Кислота | Остаток |
| H—COOH муравьиная | H—CO— формил | СH3(CH2)2-COOH масляная | СH3(CH2)2-CO— бутирил |
| CH3—COOH уксусная | CH3—CO— ацетил | (CH3)2CH—COOH изомасляная | (CH3)2CH—CO— изобутирил |
| CH3CH2—COOH пропионовая | CH3CH2—CO— пропионил | CH3(CH2)3-COOH валериановая | CH3(CH2)3-CO— валерил |
Физические свойства предельных одноосновных кислот
Первые три представителя предельных одноосновных кислот – жидкости с острым характерным запахом. Они смешиваются с водой во всех отношениях. Масляная кислота исследующие за ней гомологи – маслянистые, неприятно пахнущие жидкости, хуже растворимые в воде.
Высшие кислоты – твердые, не растворимые в воде вещества. В органических растворителях (спирт, эфир) большинство кислот растворяются хорошо.
Температуры кипения жирных кислот нормального строения закономерно возрастают по мере увеличения числа углеродных атомов. Установлено, что молекулы кислот ассоциированы подобно тому, как ассоциированы молекулы воды или спиртов. Низшие кислоты хорошо перегоняются с водяным паром, поэтому их обычно называют летучими жирными кислотами.
Температуры плавления одноосновных кислот по мере увеличения в их молекулах числа углеродных атомов в общем также возрастают; но при этом наблюдается следующая закономерность: кислоты с нормальной цепью, имеющие четное число углеродных атомов, плавятся обычно при более высокой температуре, чем предыдущий и последующий члены гомологического ряда, имеющие нечетное число углеродных атомов.
Химические свойства
Химические свойства карбоновых кислот определяются свойствами карбоксильной группы и связанного с ней углеводородного радикала, а также их взаимным влиянием. Мы рассмотрим реакции кислот: а) обусловленные подвижностью атома водорода в карбоксиле; б) основанные на способности гидроксильной группы карбоксила замещаться различными атомами или группами и в) реакции за счет связанного с карбоксилом углеводородного остатка.
А) Подвижность водорода карбоксильной группы
(диссоциация карбоновых кислот)
Подобно неорганическим кислотам карбоновые кислоты в водных растворах диссоциируют, образуя катионы водорода и анионы кислот (карбоксилатанионы):
R—COOH ® R—COO- + H+
карбоновая к-та анион кислоты
(карбоксилатанион)
Поэтому растворимые в воде карбоновые кислоты окрашивают лакмус в красный цвет, проводят электрический ток, имеют кислый вкус, т.е. являются электролитами и проявляют кислотные свойства.
Склонность карбоновых кислот к диссоциации обусловлена подвижностью водорода гидроксильной группы карбоксила. Мы уже знаем, что водород гидроксильной группы спиртов тоже подвижен и спирты в некоторой степени проявляют кислотные свойства. Однако в спиртах гидроксильная группа связана с насыщенным углеводородным остатком, и под его влиянием подвижность водорода в гидроксиле столь мала, что спирты являются более слабыми кислотами, чем вода (константы диссоциации спиртов ниже 10-16), и практически нейтральны. В кислотах же гидроксил непосредственно связан не с углеводородным остатком, а с карбонильной группой, под влиянием этой группы подвижность водорода в гидроксиле настолько увеличивается, что он способен к отщеплению в виде протона. Константы диссоциации карбоновых кислот значительно больше констант диссоциации спиртов и достигают порядка 10-4-105.
Влияние карбонильной группы на кислотные свойства гидроксила в карбоксиле объясняется смещением p-электронов ее двойной связи к карбонильному кислороду (I):







 Od- O O1/2-
Od- O O1/2-






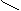 R ®d+C R—C R—C
R ®d+C R—C R—C
 O H O-: O1/2-
O H O-: O1/2-
I II III
Частичный положительный заряд (б+) карбонильного углерода компенсируется сдвигом электронов в связи С—О, что вызывает резкое смещения пары электронов в связи О—Н. Это и обуславливает значительно большую подвижность гидроксильного водорода в кислотах, чем в спиртах, возможность его ионизации. С отрывом иона Н+ образуется карбоксилатанион, отрицательный заряд которого в результате электронных смещений, показанных схемой (II), равномерно распределяется между обоими атомами кислорода. Таким образом, связи между атомом углерода и двумя атомами кислорода выровнены, т.е. являются промежуточными между простой и двойной связями; это представлено схемой (III). Поэтому в уравнениях ионных реакций карбоксилатанион правильнее изображать неразвернутой формулой R-COO- (минус относится ко всему аниону).
Способность карбоновых кислот к диссоциации зависит и от влияния связанного с карбоксилом углеводородного радикала. В таблице приведены константы диссоциации карбоновых кислот; самой сильной одноосновной карбоновой кислотой является муравьиная, в которой карбоксил не связан с радикалом. Кислоты, содержащие в соединении с карбоксилом предельные углеводородные остатки, значительно слабее муравьиной кислоты. Это объясняется электродонорными свойствами алкильных остатков; они вызывают смещение электронов связи R-C, как показано выше в схеме (I). А это в свою очередь в некоторой степени компенсирует положительный заряд карбонильного углерода и, следовательно, уменьшает его влияние на гидроксильную группу.
По сравнению с большинством неорганических кислот насыщенные карбоновые кислоты являются слабыми кислотами. Как мы увидим дальше, введение в радикал кислоты некоторых атомов или групп атомов может значительно повысить способность органических кислот к диссоциации.
Образование солей
При взаимодействии с основаниями (реакция нейтрализации), с окислами или с активными металлами водород карбоксильной группы кислоты замещается на металл и образуются соли карбоновых кислот. Например:
СH3—C—OH + NaOH ® CH3—C—ONa + H2O
II II
O О
уксусная кислота уксуснокислый натрий (ацетат Na)
СH3—C—OH + NH4OH (или NH3) ® CH3—C—ONH4 + H2O
II II уксуснокислый
O O аммоний
Соли карбоновых кислот и щелочных металлов как соли, образованные слабыми кислотами, сильно подвергаются гидролизу и в водных растворах имеют щелочную реакцию:
CH3—C—ONa + H2O ® CH3—C—OH + NaOH
II II
О O
Более сильные минеральные кислоты вытесняют карбоновые кислоты из их солей:
CH3—C—ONa + HCl ® CH3—C—OH + NaCl
II II
O О
В) Реакции замещения гидроксила в карбоксиле (образование функциональных производных карбоновых кислот)
Гидроксильная группа в карбоксиле кислот может быть замещена различными атомами или группами (Х); образующиеся при этом вещества обычно называют функциональными производными карбоновых кислот; строение их может быть представлено общей формулой R—C—X
II
O
Мы кратко рассмотрим образование и свойства таких производных кислот, или галогенангидриды, ангидриды, сложные эфиры.
Не нашли, что искали? Воспользуйтесь поиском: