
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Понятия обратимых и необратимых процессов 3 страница
dFi<0, dS≥0. (2.49)
В открытых системах изменение энтропии и свободной энергии выражается суммой энтропии и свободной энергии как внутри системы dSi, так и поступающей извне или уходящей во внешнюю среду dSе, то есть
dF=dFi+dFe; dS=dSi+dSe, (2.50)
где dSi - производство энтропии в результате внутренних химических реакций; всегда положительна, если поместить организм в изолирующую оболочку;
dSe зависит от конкретной ситуации.
Из уравнения (3.50) следует возможность стационарного, но неравновесного состояния открытой системы. В стационарном состоянии термодинамические величины, характеризующие систему, постоянны, но не имеют равновесных значений. Энтропия системы не является постоянной. При стационарном состоянии системыимеем:
dS=0, то есть dSe=-dSi<0. (2.51)
То есть производимая энтропия должна полностью уходить во внешнюю среду. Этого не происходит, так как свободная энергия открытой системы постоянно пополняется за счет поступлений из внешней среды, а энтропия продуцируется внутри организма и постоянно выводится во внешнюю среду:
dSe<0, dFe>0. (2.52)
Восполнение свободной энергии происходит за счет поступления в организм питательных веществ, а выделение энтропии осуществляется за счет удаления из организма конечных продуктов обмена и теплоты. Поэтому используется понятие отрицательной энтропии. Считают, что в организме постоянно продуцируется положительная энтропия, а из окружающей среды в организм поступает отрицательная энтропия. Таким образом, отрицательная энтропия - понятие условное, под которым понимают не запас упорядоченности, а свободную энергию, поступающую в пищу.
С другой стороны, энтропия в организме может оставаться постоянной величиной, если будет постоянно увеличиваться или уменьшаться поток отрицательной энтропии, образующейся в организме. Во всех случаях энтропия системы "организм-среда" возрастает, что находится в полном соответствии со вторым законом термодинамики. Уравнение Пригожина можно записать в следующем виде:
 . (2.53)
. (2.53)
Это значит, что скорость изменения энтропии в организме равна алгебраической сумме скорости производства энтропии внутри организма и скорости поступления отрицательной энтропии из среды в организм. При
 (2.54)
(2.54)
общее изменение энтропии и свободной энергии внутри системы равно нулю. Такое состояние системы, при котором параметры ее со временем не изменяются, но происходит обмен веществом и энергией с окружающей средой, называется стационарным. Уравнение (3.54) является уравнением стационарного состояния. Сходство стационарного состояния и термодинамического равновесия заключается в том, что параметры системы во времени не меняются как в том, так и в другом случае. Таким образом, живой организм представляет собой открытую термодинамическую систему, которая находится в стационарном состоянии. Для живого организма характерно постоянство параметров состояния во времени, которое в биологии называют гомеостазом.
Гомеостаз - это стационарное состояние организма. Для теплокровных стационарными поддерживаются такие показатели, как химический состав внутри среды, осмотическое давление, рН среды и т.д.
Процессы в живом организме представляют собой совокупность неравновесных процессов, при которых все параметры организма в течение длительного времени сохраняют постоянные величины. Так, с большим постоянством поддерживается температура отдельных органов и тканей у теплокровных животных, сохраняется неизменным солевой состав и кислотность различных биологических жидкостей, осмотическое давление и т.д.
В открытой системе при стационарном состоянии, несмотря на отсутствие термодинамического равновесия, сохраняются неизменными в течение длительного времени многие ее физические и химические свойства. В биологических системах свободная энергия и энтропия также поддерживаются на постоянных уровнях, что возможно только потому, что система получает свободную энергию из окружающей среды. Обозначим термодинамический поток, вызванный i-ой диффузией, теплопроводностью и т.д., через Ji, a градиенты различных веществ обозначим через Xk. Тогда все потоки, действующие в неравновесной системе, можно записать в следующем виде:
 , (2.55)
, (2.55)
где Lik — феноменологические коэффициенты;
k = 1, 2, 3, …, n – коэффициенты.
Уравнение (2.55) называют феноменологическим уравнением Онсагера. Смысл уравнения в том, что каждый из потоков влияет на величины других потоков. Например, химическая реакция окисления в клетках снижает концентрацию в них кислорода, что создает диффузионный поток кислорода внутрь клетки. Одновременно эта же реакция (в данном случае термодинамическая сила) создает диффузионный поток углекислого газа из клетки наружу, поток тепла, вызванный окислением, и целый ряд других потоков.
При стационарном состоянии наблюдается равенство перекрестных феноменологических коэффициентов, то есть
Lik=Lki. (2.56)
Это соотношение называется соотношением взаимности Онсагера, смысл которого заключается в том, что равновесные действия вызывают равную ответную реакцию в данной системе (это очень сходно с третьим законом Ньютона в механике). Стационарное состояние - признак не только внутренней среды организма, но и всех его клеток, которые характеризуются постоянностью концентрационных градиентов. Наконец, в стационарном состоянии находится вся сеть биохимических превращений в организме. Как было сказано выше, в организме протекают необратимые процессы. Поэтому скорость производства энтропии в организме
dSi/dt>0. (2.57)
Пригожин сформулировал основное свойство стационарного состояния, которое заключается в том, что в стационарном состоянии скорость возрастания энтропии, обусловливающая протекание необратимых процессов, имеет положительные и минимальные из всех возможных значений. Это свойство получило название теоремы Пригожина. Энтропия является мерой рассеяния свободной энергии, следовательно, при стационарном состоянии рассеяние свободной энергии является минимальным. Если система по какой-либо причине отклоняется от стационарного состояния, то, в силу стремления системы к минимальному производству энтропии, в ней наступают внутренние изменения, которые будут приближать систему к стационарному состоянию. Это свойство системы называется принципом Ле-Шателье-Брауна. Стационарные состояния поддерживаются с помощью механизмов ауторегулирования, которые имеют обратную отрицательную связь. Так, повышение температуры внешней среды приводит к увеличению теплоотдачи. Таким образом, если организм, его ауторегулирующие механизмы способны поддерживать стационарное состояние биологической системы при данном изменении внешних условий, то организм адаптируется к ним. В противном случае в организме происходят отдельные изменения, и наступает его гибель.
Подводя итог сказанному выше, приходим к выводу, что жизнь поддерживается в сравнительно узких интервалах температур, и чем более высоко организовано живое существо, тем более жесткие требования предъявляются к его термостабилизации.
Живой организм – открытая термодинамическая система, для которой справедливы все законы термодинамики.
В живом организме должен быть внутренний источник тепла. Тепловыделение в организме любого животного легко подсчитать, зная количество потребляемого им кислорода за определенный интервал времени.
В замкнутых системах все самопроизвольные процессы идут в направлении увеличения энтропии. В открытых системах (живых организмах), вследствие протекания в них биохимических процессов, наблюдается изменение свободной энергии, что может привести как к увеличению, так и к уменьшению энтропии. Считают, что в организме постоянно продуцируется положительная энтропия, а из окружающей среды в организм поступает отрицательная энтропия. Скорость изменения энтропии в организме можно определить согласно уравнению Пригожина.
Вопросы для самопроверки
1. Дайте определение понятию системы.
2. Какие виды термодинамических систем Вы знаете?
3. Сформулируйте первое начало термодинамики.
4. Каково его применение для газовых законов?
5. Дайте определение коэффициента Пуассона.
6. Каково применение первого начала термодинамики к открытым системам?
7. Сформулируйте закон Гесса.
8. Каков тепловой баланс организмов животных и человека?
9. Сформулируйте второе начало термодинамики.
10. Дайте определение свободной и связанной энергии. Что такое обратимые и необратимые процессы?
11. Что такое энтропия? Каков ее физический смысл?
12. Что такое термодинамические потенциалы?
13. Сформулируйте теорему Пригожина.
14. Дайте определение понятию стационарного состояния открытой системы.
15. Что такое аутостабилизирующие системы? Какова их роль в жизнедеятельности организма?
Задачи для закрепления изучаемого материала
1. Пары ртути массой 200 г нагреваются при постоянном давлении. При этом температура возросла на 100 К. Определить увеличение внутренней энергии паров и работу расширения. Молекулы паров ртути одноатомные.
2. Через сухожилие площадью 3 см2 за 2 часа проходит 12,6 Дж теплоты. Толщина сухожилия 5 мм. Определить разность температур между внутренней и внешней частями сухожилия. Коэффициент теплопроводности сухожилия 4,60·10-2 Вт/(м·К)
3. Какое количество теплоты затрачивает человек на парообразование, если за сутки он выделяет 0,5 кг пота? Каково полное количество теплоты, выделяемое человеком за суки, если его масса 70 кг и теплопродукция взрослого человека 1,6 Дж/(кг·с)? Удельная теплота парообразования пота 2,45 МДж/кг.
4. При непрямой калометрии энергетический расход человека за 10 мин составил 84 кДж. Какой объем кислорода он выдохнул, если известно, что в выдыхаемом воздухе содержалось 13 % кислорода и 7 % углекислого газа?
5. Вычислите изменение энтропии, создаваемое в сутки взрослым человеком и грудным ребенком. Сравните эти величины. Какая из них больше? Во сколько раз? Вычислите изменение энтропии в сутки, приходящееся на 1 кг тела человека. Какая из этих величин окажется больше? Массы ребенка и взрослого человека соответственно 7 и 70 кг.
6. Определить расход энергии человека в состоянии мышечного покоя, если за 10 мин он выдыхает 60 л воздуха, в котором содержится 15 % кислорода и 5 % углекислого газа.
7. Во сколько раз изменится теплоотдача с поверхности тела человека при понижении температуры воздуха в комнате от 26 °С до 16 °С? Среднюю температуру кожи человека принять равной 36,6 °С. На какую длину волны приходится максимум излучения тела человека?
8. Телом массой 60 кг в течение 6 часов была поглощена энергия 1 Дж. Найдите поглощенную дозу и мощность поглощенной дозы в единицах СИ.
9. Для лечения мастита на грудь накладывают парафиновую аппликацию при температуре 60 °С. Удельная теплоемкость парафина 3,23 кДж/(кг·К). Вычислить необходимую массу парафина, если для проведения процедуры необходимо передать груди 185 кДж теплоты. Температура груди 37 °С.
10. Спортсмен, пробегая дистанцию, выделяет за 1 мин 90 л воздуха, в котором содержится 12 % кислорода и 8 % углекислого газа. Каков расход энергии спортсмена за 5 мин дистанции?
11. За какое время через мышцу площадью 1 дм2 и толщиной 10 мм пройдет 2 кДж теплоты, если температура мышцы 38 °С, а температура окружающего воздуха 15 °С? Коэффициент теплопроводности мышцы 5,7-10-2 Вт/(м·К).
12. Лечение простудного заболевания у одного пациента проводили путем наложения озокеритовой аппликации массой 1 кг, а у другого - аппликации из горячей глины массой 1,5 кг. Температура озокерита и глины соответствено 68 и 60 ºС. Удельные теплоемкости озокерита и глины соответственно 3,35 и 2,09 кДж/(кг·К). Температура тела человека 37 °С. Во сколько раз теплота, переданная телу человека озокеритом, больше переданной глиной?
13. Во сколько раз теплоотдача (то есть количество теплоты, излучаемой с 1 м2 поверхности тела в секунду) тела человека отлична от теплоотдачи тела птицы при температуре окружающего воздуха 20 °С? Средние температуры кожи человека и птицы соответственно принять равными 36,6 °С и 25 °С. На какие длины волн приходятся максимумы излучения тел лошади и человека? Приведенный коэффициент излучения кожи равен 4,9-10-8 Вт/(м2 ·К4).
14.Тяжелоатлет поднимает штангу массой 150 кг с пола к груди (h = 65 см) в течение 1,5 с. Какая средняя мощнсть при этом развивается?
15. Какую среднюю мощность развивает человек при ходьбе, если продолжительность шага равна 0,5 с? Считать, что работа затрачивается на ускорение и замедление нижних конечностей. Угловое перемещение ног около 30 °. Момент инерции нижней конечности 1,7 кг·м2. Движение ног рассматривать как равнопеременное вращательное.
16. В медицине для диагностики ряда заболеваний получил распространение метод, называемый термографией. Он основан на регистрации различия теплового излучения здоровых и больных органов, обусловленного небольшим отличием их температур. Вычислите, во сколько раз отличаются термодинамические температуры и энергетические светимости участков поверхности тела человека, имеющих температуры 36,6 °С и 37,2 °С соответственно.
17. При адиабатическом расширении углекислого газа, с количеством вещества 2 моля, его температура понизилась на 20 °С. Какую работу совершил газ?
18. Тепловая энергия из внутренних органов человека проходит сначала через мышечную ткань толщиной 4,5 см, а затем через жировую ткань толщиной 1,2 см. температура на внешней поверхности жировой ткани 37 °С. Какова температура на внутренней поверхности мышцы? Вычисление провести, не учитывая теплоты, выделяющейся в самой мышце. Коэффициенты теплопроводности мышщ и жировой ткани соответственно равны 5,70·10-2 и 2,78·10-2 Bт/м·к.
19. В хирургии для местного обезболивания небольших участков тела применяют этиловый эфир. Какое количество теплоты расходует тело на испарение эфира, если на него налито 20 г эфира при температуре 20 °С? Удельная теплоемкость эфира 2,34 кДж/кг·К. Удельная теплота парообразования 355 кдж/кг. Температура кипения эфира 34,8 °С. Температура тела 36,6 °С.
20. Кролик массой 1,5 кг поглотил за час 1,5 л кислорода. Определите, сколько энергии расходует кролик за сутки, если средний колорический эквивалент кислорода 20,52 кДж.
Типовые тесты текущего контроля.
№ 1. Выберите уравнение представляющее первое начало термодинамики:
1.  3.
3. 
2.  4.
4. 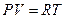
№ 2. Назовите органы или ткани в которых световая энергия превращается в химическую:
1. Мышечные ткани;
2. Внутреннее ухо;
3. Фоторецепторы сетчатки глаза;
4. светящиеся ткани рыб и насекомых;
5. Все клетки биоткани.
№ 3. Потребление одного литра кислорода или выделение одного литра углекислого газа организмом сопровождается выделением:
1. 25,5 кДж теплоты;
2. 21,35 кДж теплоты;
3. 20,08 кДж теплоты.
№ 4. Найдите выражение для свободной энергии (потенциал Гельмгольца):
1.  ;
;
2.  ;
;
3.  ;
;
4.  ;
;
5.  .
.
№ 5. Выберите выражение характеризующее значение удельной теплопроводности:
1.  ;
;
2.  ;
;
3.  ;
;
4.  ;
;
5.  .
.
ЛЕКЦИЯ 3. Молекулярная биофизика
Жизнь - это строение
белковых тел.
Ф. Энгельс
Организм животных и человека представляет собой сложную систему, состоящую из больших и малых молекул, клеточных органоидов, клеток и тканей. Молекулярная биофизика изучает строение и физико-химические вещества молекул, прежде всего полимеров – белков и нуклеиновых кислот.
Молекулярная биофизика органически вписывается в биофизику клетки, которая рассматривает строение и функциональность клеточных и тканевых систем.
Одним из теоретических аппаратов, как молекулярной биофизики, так и биофизики клетки является равновесная термодинамика, рассмотренная выше.
Живая клетка “живого” организма представляет собой химическую, биохимическую машину. Клетка существует благодаря химическим превращениям веществ, поступающих извне, и выделению веществ в окружающую среду в результате метаболизма. Таким образом, биология и биофизика неразрывно связаны с химией и биохимией. Так, в союзе биологии с физикой возникла молекулярная биофизика. Доказано, что живая природа характеризуется единством химического строения, а основные вещества и основные химические механизмы едины во всей живой природе. Так:
1) все белки строятся из двадцати аминокислот;
2) все нуклеиновые кислоты - из четырех нуклеотидов;
3) одни и те же атомные структуры существуют во всех организмах. Наблюдаются однотипные и фундаментальные биохимические процессы;
4) разнообразие организмов определяется также разнообразием сочетания одних и тех же атомных групп и их взаимодействием;
5) и, наконец, строение и свойства клетки диктуются нуклеиновыми кислотами ДНК и РНК, которые обладают «законодательной властью» в том смысле, что ими задается генетическая программа синтеза белков. В свою очередь, белки обладают «исполнительной властью», так как ни одна химическая реакция в клетке не идет без участия специального фермента.
3.1. Белковые молекулы. Структура белка
Изучение физических механизмов, которые ответственны за биологическую функциональность молекул, за каталитическую активность белков – ферментов, является одной из основных задач молекулярной биофизики. Белки – ферменты катализируют все химические, электрохимические и механические процессы в клетках и организмах. Белки – непрерывные участники всех процессов жизнедеятельности. Они определяют все метаболические процессы.
Молекулы белков – самые сложные из известных науке. Их биологически функциональная пространственная структура, а также структура надмолекулярных систем, содержащих белки, определяются как химическими связями в белковых цепях, так и целой гаммой слабых взаимодействий.
Химические, так называемые ковалентные, связи относятся к сильным взаимодействиям. Сильные связи образуются внешними электронами атомов. Теория ковалентных связей, относящихся к сильным взаимодействиям, основана на квантовой механике.
Ковалентные связи наблюдаются в ходе биохимических реакций, которые катализируются ферментами, вследствие чего происходит перестройка химических связей и электронных оболочек атома. К слабым, не химической природы, молекулярным взаимосвязям можно отнести:
1) ионные связи, которые описываются законом Кулона, согласно которому энергия взаимодействия между двумя ионами с зарядами е1 и е2 будет равна:
 , (3.1)
, (3.1)
где r - расстояние между ионами, Н·м;
 . (3.2)
. (3.2)
Ионные связи образуются между ионными группами в белках и между фосфатными группами в нуклеиновых кислотах;
2) ион-дипольные взаимодействия, которые образуются между ионами и полярными группами молекул; они определяются зарядом иона и дипольным моментом взаимодействующей с ним атомной группы;
3) ориентационные силы – электростатические взаимодействия между атомами, определяемые электрическим моментом атома  , где p – момент диполя, Кл·м; q – заряд, Кл; l – расстояние между зарядами, нм;
, где p – момент диполя, Кл·м; q – заряд, Кл; l – расстояние между зарядами, нм;
4) индукционные силы. Данные силы возникают в том случае, когда диполь атома или молекулы ионизирует в другой молекуле или группе атомов дипольный момент;
5) дисперсионные силы, или силы Ван-дер-Ваальса. Это взаимодействие валентных насыщенных электронных оболочек атомов и молекул. В данном случае силы взаимодействия не зависят от наличия электрических зарядов, дипольных моментов и т.д. Дисперсионные силы имеют квантово-механическую структуру. Они играют значительную роль в межмолекулярных взаимодействиях атомных групп и молекул с насыщенными валентными связями;
6) водородные связи. Это специфические донорно-акцепторные взаимодействия, определяющие строение и свойства воды. Они играют важную роль в формировании структур биополимеров в их взаимодействиях с малыми молекулами;
7) гидрофобные взаимодействия – силы специфического отталкивания между неполярными атомными группами и молекулами воды. Это энтропийный эффект, который определяется особенностями структуры воды как конденсированной системы. Гидрофобные взаимодействия играют важнейшую роль в формировании структуры белков.
В организме животных и человека белки выполняют особые функции. Они служат для хранения и переноса кислорода. Эти функции выполняет миоглобин, гемоглобин и гемоциалин. Низкомолекулярные белки (полипептиды) являются гормонами. Гамма–глобулины защищают организм от чужеродных биополимеров, функционируя в качестве антител в иммунных процессах.
Наконец, белки, входящие в состав соединительной ткани, хрящей и сухожилий, а также белки кожи волос выполняют опорную функцию, обеспечивая надежную и в то же время подвижную взаимосвязь органов, целостность организма и его защиту от внешних взаимодействий.
Таким образом, белки выполняют функцию запаса, передачи, транспортирования и рецепции химических сигналов.
Белки, входящие в состав рецепторных систем организма, обладают свойствами перекодирования внешних сигналов на химический и электротехнический язык.
С помощью специальных методов, в частности электрофореза, можно разделить белки сыворотки крови. Электрофоретическая скорость зависит от суммарного заряда его молекулы при данных значениях pH и ионной силы. Регистрация электрофоретической картины производится с помощью оптических методов (фотоэлектроколириметрии). Получаемая электрофореграмма, как правило, состоит из ряда пиков, которые ответственны за компоненты смеси. Площадь пика характеризует количество соответствующего компонента (рис.3.1).

Рис. 3.1. Электрофореграмма
Для электрофореза белков характерны следующие компоненты: альбумин, белок, имеющий положительный заряд, и глобулины, имеющие отрицательный заряд и которые разделяются на фрагменты [α1; α2; β; γ и δ], отличающиеся по массе.
Биологические молекулы и макромолекулы имеют строго определенный состав и строение. Биологические молекулы построены из атомов легких элементов: C, H, O, N, P, S. В организме универсальную роль играют ионы щелочных и щелочно-земельных металлов: Na, K, Ca, Мg, а также определенную роль малые количества металлов: Fe, Zn и т.д.
Организм человека содержит (в атомных процентах): H - 60,56; O - 25,67; C - 10,68; N - 2,44; Ca - 0,23; P - 0,13; S - 0,13; Na - 0,08; K - 0,04; Cl - 0,03; Mg - 0,01 и небольшое количество Fe, Zn, Cu, CO, Se, F.
Избыток H и O определяется большим содержанием воды. Как уже отмечалось, все белки построены из 20 типов аминокислот. В белках преимущественно фигурируют остатки α-аминокислоты, имеющие строение:
 ,
,
где R - углеводородный радикал, или содержащий помимо C и H и другие атомы: O, S, N.
Как показывает изучение электрических свойств аминокислот, их строение выражается формулой дипольного иона
 .
.
Образование белковой, или полипептидной, цепи происходит путем конденсации аминокислот, в результате чего образуются пептидные связи NH-CO – 20 канонических аминокислотных остатков -CO-CHR-NH-, которые классифицируются по электрохимическим составам, среди которых углеводородные остатки, остатки, содержащие гидроксид, амидную группу, карбонатную группу, серу и ароматические – π-электронные циклы. Это обусловливает все многообразие свойств и строений белков.
Денатурация белка – это утрата им биологической функциональности при нагревании, воздействии кислот и оснований и т.д. Она состоит в разрушении слабых взаимодействий и, вследствие этого, в превращении апериодического кристалла (глобутерного и фибриллярного) в статистический клубок.
Чаще всего молекулы белков состоят из одного или нескольких идентичных аминокислотных остатков. Характерные молекулярные массы отдельных полипептидных цепей в белках порядка 20000, что соответствует 150…180 остаткам. Молекулы, содержащие менее 100 остатков, считаются не белками, а полипидами. К ним относятся некоторые гармоны. Пептидная связь -CO-NH- соединяет аминокислотные остатки в белки и имеет специфическое строение. Это было установлено рентгеноструктурным анализом. Белок расщепляется на аминокислоты в результате гидролиза, который происходит при действии на белок щелочей, кислот, а также ферментов протеаз, катализирующих разрыв пептидных связей.
Гидролизат – раствор смеси аминокислот, который катализируется методом хроматографии. Протеапептический гидролиз происходит при пищеварении. Белки пищи расщепляются в пищеварительном тракте на аминокислоты, из которых строятся заново белки, которые необходимы организму. Состав белков неравномерен, так как различные аминокислотные остатки представлены в белках с разными частотами.
Последовательность аминокислотных остатков в белковой цепи называется ее первичной структурой. Определение первичной структуры производится путем частичного гидролиза белка с помощью протеаз, катализирующих расщепление пептидной связи лишь между определенными остатками. Зная строение пептидов, полученных при гидролизе различными ферментами, можно установить первичную структуру белков.
Первичная структура белка - это своего рода текст, написанный двадцатибуквенным алфавитом. Смысл и содержание этого текста состоит в биологическом функционировании белка, которое определяется структурой.
В белковых текстах запечатана биологическая эволюция - сопоставление гомологичных белков, которые выполняют одну и ту же функцию в разных видах, позволяющих выявить различия в текстах. Эти различия определяются мутационными замещениями аминокислотных остатков тем больше, чем дальше отстоят друг от друга биологические виды.
Первичная структура белка данного вида может изменяться в результате мутации. Возникают «опечатки» в белковом тексте, отрицательно сказывающиеся на функции белка. Так ряд наследственных заболеваний крови связан с мутациями гемоглобина.
Гемоглобин человека состоит из четырех цепей – двух цепей «α», содержащих по 141 остатку, и двух цепей «β», содержащих по 146 остатков. Таким образом, замена всего лишь двух остатков из 287 приведет к весьма серьезным последствиям. В этом случае некоторые нейтральные остатки изменяются кислотами. В настоящее время известно более 100 мутацитных гемоглобинов человека.
Рассмотрим связь между первичной и пространственной структурами белка.
Доказано, что построение молекулярных и немолекулярных структур всегда происходит в два этапа: 1) биосинтез соответствующих больших и малых молекул и 2) самосборка структуры. Биосинтез и самосборка, как показали эксперименты, основаны на «молекулярном узнавании», которое осуществляется благодаря слабым взаимодействиям. Самосборка осуществляется генетически, то есть кодируется биосинтез, формируется первичная структура белка. Причем естественный отбор белков идет по пространственным, третичным и четвертичным структурам. Все современные научно-исследовательские работы, как правило, посвящены структуре так называемой глобулы, то есть образованию апериодического кристалла, являющегося конечным результатом самосборки белка.
Доказано, что белок может быть разделен на спиральные формы с изгибами и петлями. Два или три соседних по цепи структурных сегмента, как правило, образуют элементарные комплексы – «шпильки» из аминокислотных α-спиралей. Так же возникают β-«шпильки», прикрытые α-спиралью. Далее возникает «домен», то есть компактная структура, построенная из нескольких элементарных комплексов и структурных сегментов. Глобулы малых белков состоят из одного домена.
Не нашли, что искали? Воспользуйтесь поиском: