
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Править]Физические свойства
Иприт
[править]
Материал из Википедии — свободной энциклопедии
У этого термина существуют и другие значения, см. Иприт (значения).
| Иприт | |
| |
| |
| Общие | |
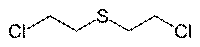
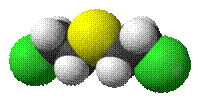
| Систематическое наименование | Иприт, горчичный газ, b-дихлордиэтилсульфид, 2,2'-дихлордиэтиловый тиоэфир, 2,2'-дихлордиэтилсульфид, 1-хлор-2-(2'-хлорэтилтио)-этан |
| Сокращения | B |
| Химическая формула | C4H8Cl2S |
| Молярная масса | 159 г/моль |
| Физические свойства | |
| Состояние(ст. усл.) | жидкость |
| Плотность | 1,280 г/см3(15 °С) г/см³ |
| Термические свойства | |
| Температура плавления | 14,5 °C |
| Температура кипения | 217 °C |
| Химические свойства | |
| Растворимостьв воде | 0,05% г/100 мл |
Ипри́т (или горчичный газ, синонимы: 2,2'-дихлордиэтиловый тиоэфир, 2,2'-дихлордиэтилсульфид, 1-хлор-2-(2'-хлорэтилтио)-этан, «Лост») — химическое соединение с формулой S(CH2CH2Cl)2. Является боевым токсическим отравляющим веществом кожно-нарывного действия. (по другой классификации — ОВ цитотоксического действия, общего алкилирующего свойства.)
| Содержание [убрать] · 1 История · 2 Получение · 3 Физические свойства · 4 Химические свойства · 5 Поражающее действие · 6 Первая помощь при поражении ипритом · 7 Защитные средства · 8 Примечания · 9 Литература · 10 Ссылки |
Править]История
Был синтезирован в Германии — Ниманом (в 1859 году) и (независимо) британским учёным Фредериком Гутри (Frederick Guthrie) в 1860 году[1]. Впервые иприт был применён Германией 12 июля 1917 года против англо-французских войск, которые были обстреляны минами, содержавшими маслянистую жидкость, у бельгийского города Ипр (откуда и произошло название этого вещества).
Во время Второй мировой войны иприт применялся только один раз Польшей, при этом погибли два немецких солдата, а двенадцать получили поражения разной степени тяжести[ источник не указан 851 день ]. Кроме того, иприт применялся во время подавленияСиньцзянского восстания
в 1934 году, в итало-эфиопскую войну 1935—1936 годов. В г. Дзержинске во время Второй мировой войны был секретный завод, на котором начиняли ипритом авиабомбы. Работники этого завода, получившие легочные поражения парами иприта, в послевоенное время вплоть до 90-х гг ХХ в. ежегодно проходили лечение в спецсанатории "Карасан" в 15 километрах к юго-западу от Алушты (между Алуштой и Ялтой)[ источник не указан 126 дней ].Править]Получение
Иприт получают двумя способами:
1. Из этилена CH2=CH2 и хлоридов серы, например S2Cl2 или SCl2:
SCl2 + 2 C2H4 → (ClCH2CH2)2S
2. Из тиодигликоля S(CH2CH2OH)2 и трихлорида фосфора PCl3:
3(HO-CH2CH2)2S + 2PCl3 → 3(Cl-CH2CH2)2S + 2P(OH)3
или тиодигликоля и соляной кислоты:
(HO-CH2CH2)2S + 2HCl → (Cl-CH2CH2)2S + 2H2O
править]Физические свойства
Иприт — бесцветная жидкость с запахом чеснока или горчицы. Технический иприт — тёмно-коричневая, почти чёрная жидкость с неприятным запахом. Температура плавлениясоставляет 14,5 °C, температура кипения — 217 °C (с частичным разложением), плотность 1,280 г/см³ (при 15 °C).
Иприт легко растворяется в органических растворителях — галогеналканах, бензоле, хлорбензоле — столь же хорошо, как и в растительных или животных жирах;растворимость
в воде составляет 0,05 %. В то время, как растворимость в абсолютном этаноле выше 16°С составляет почти 100 %, в 92%-ном этаноле она едва достигает 25 %.Вследствие некоторой поверхностной активности он уменьшает поверхностное натяжение воды и в небольшой мере растекается по ней тонким слоем, как плёнка масла. В результате добавления 1 % высокомолекулярного амина C22H38O2NH2 растекание иприта по воде увеличивается на 39 %.
Иприт очень медленно гидролизуется водой, скорость гидролиза резко возрастает в присутствии едких щелочей, при нагревании и перемешивании.
Иприт энергично реагирует с хлорирующими и окисляющими агентами. Так как при этом образуются нетоксичные продукты, указанные выше реакции используют для егодегазации
Не нашли, что искали? Воспользуйтесь поиском: