
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
В) Реакции окисления. Амины горят на воздухе с образованием углекислого газа, воды и азота.
Получение аминов. Основной способ получения аминов восстановление нитрогруппы (реакция Зинина).
Применение. Низшие алифатические амины используют для синтеза лекарств, пестицидов и пластмасс. Но еще шире используется анилин, прежде всего, для синтеза красителей (индиго, фуксин и т.д.). Сам анилин обладает жаропонижающим и обезболивающим действием, но он токсичен. На основе анилина синтезировано множество лекарственных препаратов, например, сульфаниламиды. Самые известные из них – стрептоцид и бисептол. К производным анилина можно отнести парацетамол и новокаин.
2.Аминоспиртами называют соединения, содержащие в молекуле одновременно амино- и гидроксогруппу.
У одного атома углерода эти группы удерживаются не прочно, происходит отщепление аммиака или воды, поэтому таких соединений не существует. Простейший представитель аминоспиртов-
 2-аминоэтанол - структурный компонент сложных липидов. Это вязкая жидкость с высокой температурой кипения. С сильными кислотами в реакцию вступает его аминогруппа и образуются устойчивые соли. Другой аминоспирт – холин – структурный элемент сложных липидов, имеет большое значение как витаминоподобное вещество, регулирующее жировой обмен. Его можно рассматривать как производное аминоэтанола. В организме холин может образовываться из аминокислоты серина.
2-аминоэтанол - структурный компонент сложных липидов. Это вязкая жидкость с высокой температурой кипения. С сильными кислотами в реакцию вступает его аминогруппа и образуются устойчивые соли. Другой аминоспирт – холин – структурный элемент сложных липидов, имеет большое значение как витаминоподобное вещество, регулирующее жировой обмен. Его можно рассматривать как производное аминоэтанола. В организме холин может образовываться из аминокислоты серина.


→
Биологическая роль сложных эфиров холина. Замещённые фосфаты холина (т.е. сложные эфиры спирта холина и фосфорной кислоты) являются важной структурной частью фосфолипидов – важнейшего строительного материала клеточных мембран. Сложный эфир холина и уксусной кислоты ( ацетилхолин ) – наиболее распространенный посредник при передаче нервного возбуждения в нервных тканях (нейромедиатор). Он образуется в организме при ацетилировании холина с помощью ацетилкофермента А.
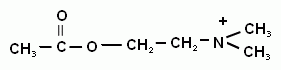
 При ингибировании ацетилхолинэстеразы (фермента, который катализирует разложение ацетилхолина), ацетилхолин накапливается в организме. Это приводит к непрерывной передаче нервных импульсов и, соответственно, к непрерывному сокращению мышечной ткани. На этом основано действие инсектицидов и нервнопаралитических ядов (например, зарина). В медицинской практике используется ряд производных холина: ацетилхолинхлорид, карбомоилхолинхлорид – сосудорасширяющие средства
При ингибировании ацетилхолинэстеразы (фермента, который катализирует разложение ацетилхолина), ацетилхолин накапливается в организме. Это приводит к непрерывной передаче нервных импульсов и, соответственно, к непрерывному сокращению мышечной ткани. На этом основано действие инсектицидов и нервнопаралитических ядов (например, зарина). В медицинской практике используется ряд производных холина: ацетилхолинхлорид, карбомоилхолинхлорид – сосудорасширяющие средства
сукцинилхолиниодид – мышечнорасслабляющее средство.

 Важную роль в организме играют аминоспирты, содержащие в качестве структурного фрагмента остаток пирокатехина (1,2-дигидроксибензол). Они носят общее название катехоламинов. Рядом вы видите формулы веществ, участвующих в образовании адреналина (фенилаланин, тирозин, ДОФА, дофамин, норадреналин, адреналин). Дофамин, норадреналин, адреналин выполняют роль нейромедиаторов. Адреналин является гормоном мозгового вещества надпочечников, а два других – его предшественники. Адреналин участвует в регуляции сердечной деятельности, в регуляции обменов углеводов, при физиологических стрессах он выделяется в кровь..
Важную роль в организме играют аминоспирты, содержащие в качестве структурного фрагмента остаток пирокатехина (1,2-дигидроксибензол). Они носят общее название катехоламинов. Рядом вы видите формулы веществ, участвующих в образовании адреналина (фенилаланин, тирозин, ДОФА, дофамин, норадреналин, адреналин). Дофамин, норадреналин, адреналин выполняют роль нейромедиаторов. Адреналин является гормоном мозгового вещества надпочечников, а два других – его предшественники. Адреналин участвует в регуляции сердечной деятельности, в регуляции обменов углеводов, при физиологических стрессах он выделяется в кровь..
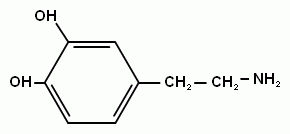 Структурно близки к катехоламинам некоторые природные и синтетические БАВ, применяемые в качестве лекарственных средств. Например :
Структурно близки к катехоламинам некоторые природные и синтетические БАВ, применяемые в качестве лекарственных средств. Например :
эфедрин (сосудорасширяющее действие ) и мезатон (повышающий давление).



3.Аминокислоты содержат в молекуле одновременно карбоксильную группу и аминогруппу. Например: 4-амино-бутановая кислота. Для аминокислот в биохимии и медицине часто используют традиционные названия. В зависимости от расположения этих групп различают  и т. д. аминокислоты. Нумерацию начинают со второго атома и используют греческий алфавит. Названия кислот в этом случае – тоже традиционные, т.е. уксусная, пропионовая, масляная, валерьяновая и т.д. 4-аминобутановая кислота будет называться
и т. д. аминокислоты. Нумерацию начинают со второго атома и используют греческий алфавит. Названия кислот в этом случае – тоже традиционные, т.е. уксусная, пропионовая, масляная, валерьяновая и т.д. 4-аминобутановая кислота будет называться  -аминомасляной кислотой. ГАМК принимает участие в обменных процессах головного мозга, является нейромедиатором. Применяется под названием гаммалон при лечении заболеваний ЦНС.
-аминомасляной кислотой. ГАМК принимает участие в обменных процессах головного мозга, является нейромедиатором. Применяется под названием гаммалон при лечении заболеваний ЦНС.
Структура ГАМК лежит в основе транквилизатора финилбута. Амид ГАМК (пирацетам, ноотропил) рассматривается как первый представитель ноотропных, т. е. влияющих на мышление веществ.


 Особое значение в органическом мире имеют
Особое значение в органическом мире имеют  -аминокислоты, из их остатков состоят пептиды и белки. Общее число встречающихся в живых организмах аминокислот около 300, однако, некоторые обнаружены только в определённых организмах. Можно выделить группу из 20
-аминокислоты, из их остатков состоят пептиды и белки. Общее число встречающихся в живых организмах аминокислот около 300, однако, некоторые обнаружены только в определённых организмах. Можно выделить группу из 20  -аминокислот постоянно встречающихся во всех белках (см. таблица аминокислот). Их называют природными аминокислотами. Причем почти все природные аминокислоты принадлежат L ряду оптических изомеров. Общую формулу
-аминокислот постоянно встречающихся во всех белках (см. таблица аминокислот). Их называют природными аминокислотами. Причем почти все природные аминокислоты принадлежат L ряду оптических изомеров. Общую формулу  -аминокислот можно записать так: Природные аминокислоты классифицируют по различным признакам. Например, по химической природе радикала: алифатические, ароматические и гетероциклические. В алифатическом радикале могут содержаться функциональные группы. Среди аминокислот выделяют нейтральные, основные и кислые, в зависимости от числа кислотных и основных групп. Характер бокового радикала может быть неполярный или полярный. Неполярные – это аминокислоты с алифатическим и ароматическим радикалом, полярные – имеют функциональные группы способные переходить в ионное состояние. Многие аминокислоты синтезируются в организме, но некоторые обязательно должны поступать извне, т.к. в организме они не могут синтезироваться. Такие аминокислоты называют незаменимыми: валин, лейцин, изолейцин, лизин, трионин, метионин,
-аминокислот можно записать так: Природные аминокислоты классифицируют по различным признакам. Например, по химической природе радикала: алифатические, ароматические и гетероциклические. В алифатическом радикале могут содержаться функциональные группы. Среди аминокислот выделяют нейтральные, основные и кислые, в зависимости от числа кислотных и основных групп. Характер бокового радикала может быть неполярный или полярный. Неполярные – это аминокислоты с алифатическим и ароматическим радикалом, полярные – имеют функциональные группы способные переходить в ионное состояние. Многие аминокислоты синтезируются в организме, но некоторые обязательно должны поступать извне, т.к. в организме они не могут синтезироваться. Такие аминокислоты называют незаменимыми: валин, лейцин, изолейцин, лизин, трионин, метионин,  фенилаланин, триптофан. Они обязательно должны содержаться в пище, т.к. нехватка даже одной из незаменимых кислот может привести к тяжелым нарушениям белкового обмена и серьезным заболеваниям.
фенилаланин, триптофан. Они обязательно должны содержаться в пище, т.к. нехватка даже одной из незаменимых кислот может привести к тяжелым нарушениям белкового обмена и серьезным заболеваниям.
Физические свойства. Все аминокислоты - это кристаллические вещества растворимые в воде, многие имеют сладкий вкус, некоторые безвкусны, есть кислые или имеют вкус мяса (глутаминовая).
Химические свойства.
А) Аминокислоты гетеро- функциональные соединения. За счет группы –СООН проходят реакции характерные для карбоновых кислот (т.е. кислотные свойства, образо-вание сложных эфиров…). За счет аминогруппы проходят реакции, в которых аминокислота проявляет основные свойства, т.е. участвует в реакциях нуклеофильного обмена аминогруппы.
Наличие основной и кислотной группы одновременно делает аминокислоты амфотерными соединениями, т.е. способными вступать в реакцию и с кислотами и со щелочами.
NH2- CH2 -CH2-COOH + NaOH →NH2- CH2 - CH2-COONa + H2O – кислотные свойства
NH2- CH2 CH2-COOH + HCl → Cl-[+NH3- CH2 -CH2-COOH] - основные свойства
В твёрдом состоянии и в водных растворах аминокислоты существуют в виде биполярных ионов. При этом среда в растворе остается нейтральной. Если, конечно, в радикале нет дополнительных кислотных или аминогрупп. В кислой или щелочной среде молекула аминокислоты существует в виде катиона или аниона.
NH2- CH2 CH2-COOH ↔ +NH3- CH2 -CH2-COO-
Б) Аминогруппа одной молекулы может взаимодействовать с карбоксильной группой другой молекулы. При этом образуется более сложная молекула и выделяется низкомолекулярное вещество – вода. Такую реакцию называют конденсацией, ее можно рассматривать, как реакцию нуклеофильного замещения гидроксогруппы в молекуле аминокислоты на нуклеофильный остаток другой молекулы аминокислоты. Если в реакцию вступают множество молекул ее называют реакцией поликонденсации. Рассмотрим реакцию конденсации ε-аминокапроновой кислоты.
NH2- CH2 - CH2-CH2 - CH2 - CH2- CO OH + Н NH- CH2 - CH2-CH2 - CH2 - CH2- COOH →
NH2- CH2 - CH2-CH2 - CH2 - CH2- CO- NH - CH2 - CH2-CH2 - CH2 - CH2- COOH + Н2О
Если эту реакцию повторить много раз в результате получится полимер капрон
nNH2- CH2 - CH2-CH2 - CH2 - CH2- COOH →[- NH- CH2 - CH2-CH2 - CH2 - CH2- CO-]n+ Н2О
Группа - CO- NH - называется пептидной группой, а связь между атомами углерода и азота в ней – пептидной связью. Молекулу полимера, в данном случае, можно назвать полипептидом.
Реакция поликонденсации является обратимой, проходит при нагревании в кислой среде, обратная реакция называется реакцией гидролиза.
Не нашли, что искали? Воспользуйтесь поиском: