
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Лабораторный практикум №2
Мониторинг атмосферного воздуха
Одним из важнейших объектов окружающей среды является атмосферный воздух. Устойчивость биосферы зависит от его чистоты. Загрязнение воздуха отрицательно влияет на растения, животных, людей, строения, оборудование и различные материалы.
В качестве наиболее распространенных и опасных были выявлены восемь категорий загрязнителей: 1 – взвешенные вещества, которые могут переносить другие загрязнители, растворенные в них или адсорбированные на поверхности частиц;
2 – углеводороды и другие летучие органические соединения; 3 – угарный газ (СО); 4 – оксиды азота (NOx); 5 – оксиды серы (в основном диоксид (SO2)); 6 – свинец и другие тяжелые металлы; 7 – озон и другие фотохимические окислители; 8 – кислоты (в основном серная и азотная).
Контроль за состоянием атмосферного воздуха включает в себя изучение источников загрязнения, исследование химических и фотохимических превращений загрязняющих веществ, выявление наиболее токсичных веществ, изучение распространения загрязнителей с воздушными потоками, отбор и анализ загрязнителей. Надежность контроля за загрязнением наряду с рассмотренными выше факторами зависит от способа отбора проб. В зависимости от предполагаемого загрязнения воздуха отбор проб может производиться с концентрированием или без него.
Лабораторная работа №1
Определение запыленности воздуха
Цель работы: обучение студентов правилам пробоотбора пыли и определению пылесодержания гравиметрическим методом.
Объем работы: 2 часа.
Пыль является аэрозолем. Аэрозоли представляют собой частицы вещества (твердые или жидкие) во взвешенном состоянии. Большое количество аэрозолей образуется в результате естественных природных процессов, но немалая их доля имеет антропогенное происхождение. Основной источник антропогенных аэрозолей- процесс горения. Энергетика и транспорт дают 2/3 общего количества антропогенных аэрозолей. Среди прочих источников аэрозолей – металлургические предприятия, производство строительных материалов, химические производства.
Для количественной характеристики запыленности воздуха в настоящее время используется преимущественно весовой метод (гравиметрия). Через аналитический фильтр просасывают определенный объем запыленного воздуха.
Массу всей витающей пыли без разделения на фракции рассчитывают по увеличению массы фильтра. Лучшими являются фильтры из ткани ФПП. Фильтры Петрянова обладают высокой эффективностью и малым аэродинамическим сопротивлением, их ткань обладает водоотталкивающими свойствами. Метод применяется для определения разовых и среднесуточных концентраций пыли в воздухе населенных пунктов и санитарно-защитных зон в диапазоне 0,04 – 10 мг/м3.
Ход работы. Фильтр из ткани ФПП выдерживают в течение 40 – 60 мин. в весовой комнате, взвешивают, помещают в пакет и доставляют на место пробоотбора, где его вкладывают в фильтродержатель, который крепко завинчивают. Перед отбором проб проверяют герметичность фильтродержателя, для чего его входное отверстие закрывают пробкой и включают прибор: при герметичном присоединении расходомер воздуха показывает ноль.
Отбор проб проводят со скоростью 250 – 400 л/мин, чтобы навеска пыли на фильтре была не менее 4 мг. Отбор ведется не более 30 мин. После протягивания воздуха фильтр пинцетом извлекают из держателя, складывают вчетверо запыленной поверхностью внутрь и помещают в тот же пакет, из которого он был взят. В лаборатории фильтр выдерживают в течение 40 – 60 мин. при комнатной температуре и доводят до постоянной массы. Если отбор пробы проводился при относительной влажности, близкой к 100%, то фильтр помещают в стеклянной чашке в эксикатор с плавленым хлористым кальцием на 30 – 50 мин., а затем уже выдерживают при комнатной температуре 40 – 50 мин.
Обработка результатов.
Концентрацию пыли С мг/м3 вычисляют по формуле:
С =  ,
,
где:
М – масса пыли на фильтре, равная разности масс запыленного и чистого фильтра, мг;
V0 – объем аспирированного воздуха, приведенный к нормальным условиям, м3.
Под нормальными условиями подразумевается температура 00С и атмосферное давление 1013 гПа (760 мм рт. ст.):
V0 = 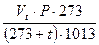 ,
,
где:
Vt – объем аспирированного воздуха при температуре t и атмосферном давлении
Р гПа, м3;
273 – коэффициент расширения газов;
1013 – нормальное давление, гПа.
Контрольные вопросы:
- С какой целью и как производится отбор проб воздуха?
- Какие требования предъявляются к процессу отбора проб воздуха?
- От чего зависит выбор способа отбора проб воздуха?
- Перечислите способы отбора проб воздуха при аспирационном методе? Какая для этого требуется аппаратура?
- Дайте характеристику фильтрам из ткани ФПП.
- При температуре воздуха 240С, давлении 750 мм рт. ст. отобран воздух для лабораторного исследования в течение 20 мин. со скоростью 25 дм3/мин. Рассчитайте объем протянутого воздуха и приведите объем воздуха к нормальным условиям.
- Как осуществляется отбор проб воздуха для определения в нем пыли?
- Как рассчитывается содержание пыли?
- Отобрано 100 дм3 воздуха. Масса фильтра до отбора – 0,3452 г, после отбора – 1,5848 г. Рассчитайте концентрацию пыли и сравните с ПДК (6 мг/м3).
- Пропущено 600 дм3 воздуха при температуре 160С, давлении 742 мм рт. ст. Масса задержанной пыли 10 мг. Рассчитайте концентрацию пыли, сопоставьте с гигиеническими нормами.
Лабораторная работа №2
Определение диоксида азота
Цель работы: обучение студентов правилам пробоотбора газов и определению концентрации загрязнителей по оптической плотности раствора.
Объем работы: 2 часа.
Азот образует смесь различных оксидов, но лишь NO и NO2 имеют значение как атмосферные загрязнители. Обычно суммарные концентрации NO и NO2 в атмосфере обозначаются как NOx.
Оксиды азота играют основную роль в образовании фотохимического «смога», влияют они и на разрушение озонового слоя, ведут также к образованию кислотных дождей. Загрязнение атмосферы оксидами азота в целом сравнительно невелико. Но в районах с развитой химической промышленностью имеются локальные зоны повышенного содержания NO и NO2 в воздухе.
Монооксид азота NO – бесцветный газ, образующийся в малых количествах в цилиндрах двигателей внутреннего сгорания при взаимодействии О2 с N2. В дальнейшем он окисляется кислородом до двуокиси азота NО2.
Диоксид азота представляет собой коричнево-бурый газ, ядовитый, с неприятным запахом. При растворении NO2 в воде образуется азотная кислота.
Газообразный NO2 токсичен (2 класс опасности), является также сильным коррозионно-активным агентом.
Предельно допустимая концентрация NO2 максимально разовая составляет 0,085 мг/м3, среднесуточная - 0,04 мг/м3.
Метод определения содержания диоксида азота в воздухе с реактивом Грисса-Илосвая основан на взаимодействии двуокиси азота и сульфаниловой кислоты с образованием диазосоединения, которое, реагируя с α-нафтиламином, дает азокраситель. Последний окрашивает раствор от бледно-розового до красно-фиолетового цвета. По интенсивности окраски раствора определяют количество NO2.
Чувствительность определения 0,1 мкг в анализируемом объеме пробы. Диапазон измеряемых концентраций составляет 0,03 – 0,64 мг/м3 при отборе пробы воздуха 5 л.
Ход работы. Для определения разовой концентрации NO2 исследуемый воздух протягивают через поглотитель Рыхтера, наполненный 6 мл поглотительного раствора, со скоростью 0,25 л/мин в течение 20 мин.
Во время отбора пробы следует избегать освещения поглотительного прибора солнечными лучами. Срок хранения отобранных проб не более 2 суток.

В лаборатории уровень раствора в поглотительном приборе доводят до метки 6 мл дистиллированной водой. Для анализа 5 мл раствора из каждой пробы переносят в пробирку и добавляют по 0,5 мл составного реактива.
Содержимое пробирок тщательно встряхивают и через 20 мин. (непосредственно перед измерением) в пробирки приливают по 5 капель 0,06%- ного раствора Na2SO3 и еще раз встряхивают. Оптическую плотность измеряют в кюветах толщиной 10 мм при длине волны 540 нм относительно воды. Время от добавления составного реактива до измерения оптической плотности всех проб должно быть одинаковым.

Количество NO2 в пробах находят по калибровочному графику. Одновременно проводятся измерения оптической плотности нулевой пробы.
Расчет концентраций диоксида азота в воздухе проводят по формуле:
С =  ,
,
где:
 – общий объем пробы в поглотительном приборе (6 мл);
– общий объем пробы в поглотительном приборе (6 мл);
b – объем пробы для анализа (5 мл);
m – количество NO2 в пробе, найденное по калибровочному графику, мкг;
V0 – объем протянутого воздуха, приведенный к нормальным условиям, л.
Построение калибровочного графика
В мерные колбы на 50 мл наливают 1, 2, 4, 6, 8, 10, 20 мл рабочего стандартного раствора (1 мкг/мл) разбавляют до метки поглотительным раствором. Концентрация NO2 в 5 мл стандартного раствора в мерных колбах составляет соответственно 0,1; 0,2; 0,4; 0,6; 0,8; 1,0; 2,0 мкг.
Для приготовления шкалы стандартов отбирают в пробирки по 5 мл каждого стандарта и определяют их оптическую плотность.

Контрольные вопросы:
- Дайте определение понятия ПДК.
- Напишите формулу приведения отобранного объема воздуха к нормальным (стандартным) условиям.
- Напишите формулу для расчета концентраций газов в воздухе (в мг/м3).
- В чем заключается принцип метода определения оксидов азота? Какие реактивы применяются в качестве стандартных и поглотительных растворов?
- Как проводится отбор проб воздуха и готовится шкала стандартов для определения оксидов азота?
- Для определения оксидов азота воздух со скоростью 0,2 дм/мин в течение
5мин протягивается через 10 см3 поглотительного раствора. При фотометрии
1 см3 пробы обнаружено 0,5 мкг оксида азота. Вычислите концентрацию оксида
азота и сопоставьте с ПДК.
7. Для определения ртути через гофрированную трубку протянуто 200 дм3
воздуха при температуре 150С и давлением 746 мм рт. ст. Общий объем
пробы составляет 2 см3. При фотометрии 1 см3пробы окраска совпала с про-
биркой стандартной шкалы, содержащей 1,0 мкг ртути. Определите концентра-
цию ртути и сопоставьте с ПДК.
8. Для определения аммиака воздух со скоростью 0,5 дм3/мин протягивают в те-
чение 5 мин через 10 см3 поглотительного раствора. При фотометрии 1 см3
пробы обнаружено 4,0 мкг аммиака. Определите концентрацию аммиака в воз-
духе и сопоставьте с ПДК.
9. Наметьте основные пути снижения концентрации токсичных веществ в атмос-
ферном воздухе и воздухе промышленных предприятий.
Не нашли, что искали? Воспользуйтесь поиском: