
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Альдегиды и Кетоны.
Эти два класса органических веществ — альдегиды и кетоны — характеризуются присутствием в молекуле карбонильной
группы, или радикала карбонила, >С=О. В альдегидах атом углерода этого радикала связан не менее чем с одним атомом водорода, так что получается одновалентный радикал
называемый также альдегидной группой. В кетонах карбонильная группа связана с двумя углеводородными радикалами и называется также кетогруппой или оксо-группой.
Простейший альдегид, называемый муравьиным альдегидом или формальдегидом, содержит альдегидную группу, связанную с атомом водорода, и имеет строение:

альдегид СН3—СНО называется уксусным альдегидом.
Получение альдегидов и кетонов
1.Окисление спиртов
Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот.

При окислении вторичных спиртов образуются кетоны.
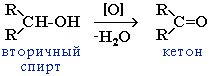
2.В промышлености альдегиды и кетоны получают дегидрированием спиртов, пропуская пары спирта над нагретым катализатором (Cu, соединения Ag, Cr или Zn).

3. Гидратация алкинов (реакция Кучерова)
Присоединение воды к ацетилену в присутствии солей ртути (II) приводит к образованию ацетальдегида:

Кетоны получают при гидратации других гомологов ряда алкинов:

4. Окисление алкенов (катализаторы - хлориды Pd и Cu):

1. Образование карбоновых кислот Благодаря тому, что в альдегидах имеется атом водорода, связанный с карбонильной группой, альдегиды чрезвычайно легко окисляются не только разными окислителями, но даже и кислородом воздуха. Продуктами окисления обыкновенно являются кислоты, содержащие в молекуле то же число атомов углерода, что и исходные альдегиды:

Для открытия альдегидов часто пользуются реакцией восстановления аммиачного раствора окиси серебра, причем серебро может выделяться на стенках стеклянного сосуда в виде зеркального слоя. Для этой же цели пользуются реакцией восстановления фелинговой жидкости; при этом из синего раствора осаждается при нагревании красный осадок закиси меди.
Кетоны окисляются значительно труднее альдегидов — только при действии сильных окислителей (например, KMnO4). При этом обыкновенно разрывается связь между карбонильной группой и одним из алкилов и получаются кислоты с меньшим числом атомов углерода в молекуле.
Реакция окисления кетонов может быть применена для определения их строения. Так как связь между углеродными атомами может разорваться с каждой стороны карбонильной группы (правила окисления кетонов А. Н. Попова), то в наиболее общем случае могут получиться четыре кислоты. Например, этилбутилкетон

может дать следующие четыре кислоты:

Фактически при окислении кетонов получаются не только ожидаемые согласно приведенной схеме кислоты, но и кислоты с меньшим числом атомов углерода. Это часто затрудняет установление строения исходного кетона.
2. Взаимодействие со спиртами. Альдегиды могут взаимодействовать с одной или двумя молекулами спирта, образуя соответственно полуацетали и ацетали.
Полуацеталями называются соединения, содержащие при одном атоме углерода гидроксильную и алкоксильную группы. Ацетали — это соединения, содержащие при одном атоме углерода две алкоксильные группы:

Взаимодействие со спиртами:
CH3COCH3 + 2C2H5OH → C2H5—O—C(CH3)2—O—C2H5
Реакция с циановодородной (синильной) кислотой. Реакция имеет важное значение в органической химии. Во-первых, в результате реакции можно удлинить углеродную цепь; во-вторых, продукты реакции — гидроксинитрилы — служат исходными соединениями для синтеза гидроксикарбоновых кислот:
СН3—СН=O + Н—CN -> СН3—CH(CN)—ОН
При взаимодействии с аммиаком образуются имины:

Ацето́н (диметилкето́н, систематическое наименование: пропан-2-о́н) — простейший представитель кетонов. Формула: CH3-C(O)-CH3. Бесцветная легкоподвижная летучая жидкость с характерным запахом. Полностью смешивается с водой и большинством органических растворителей. Ацетон хорошо растворяет многие органические вещества (ацетилцеллюлозу и нитроцеллюлозу, воск, резину и др.), а также ряд солей (хлорид кальция, иодид калия). Является одним из метаболитов, производимых человеческим организмом.
Качественная реакция на альдегиды:
Н-СОН + 2 Cu(OH)2 = HCOOH + Cu2O↓+ 2 H2O
27. При расщеплении АТФ на АДФ и неорганический фосфат (Фн) высвобождается энергия:

Из АДФ и фосфата может быть вновь синтезирован АТФ, но для этого требуется затратить 30,6 кДж энергии на 1 моль вновь образованного АТФ.

| <== предыдущая лекция | | | следующая лекция ==> |
| Удельная адсорбция зависит от следующих факторов. | | |
Не нашли, что искали? Воспользуйтесь поиском: