
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра называются газовыми законами.
Процессы же, протекающие при постоянстве одного из параметров, называются изопроцессами.
Критические температура и давление. Теоретически все газы можно сжижать при охлаждении их до определенной температуры или путем их сжатия. Некоторые газы необходимо предварительно охладить перед Их сжатием (табл. 18). Рассматривая этот вопрос подробнее, можно установить, что все газы имеют строго определенную температуру и давление, при которых их можно обратить в жидкость. Такие параметры называются критическими.
• Критическая температура газа — это температура, выше которой газ не может быть сжат до состояния жидкости, каким бы высоким ни было давление.
• Критическое давление газа — это минимальное давление, при котором газ, находящийся при критической температуре, может быть сжат до состояния жидкости.
Таблица 18. Значения критических давлений и температур некоторых газов
| Газ | Химическая формула | Критическая температура, °С | Критическое давление, бары |
| Аммиак | NHз | 132,4 | 112,0 |
| Гелий | Не | -268,0 | 2,3 |
| Водород | Н2 | -240,0 | 12,8 |
| Углекислый газ | С02 | 31,0 | 73,0 |
| Метан | СН4 | -82,1 | 45,8 |
| Азот | N2 | -147,1 | 33,9 |
| Кислород | O2 | -118,8 | 51,4 |
| Пропан | СзH8 | 96,8 | 42,1 |
| Вода | Н2O | 374,0 | 218,0 |
| Винилхлорид | С2НзСl | 156,5 | 56,9 |
 Уравнение состояния идеального газа (уравнение Менделеева—Клапейрона). Состояние идеального газа характеризуют три инструментально измеряемых параметра: давление Р, Па; удельный объем v, м ³ кг, или плотность ρ, кг/м3; Т— температура, К.
Уравнение состояния идеального газа (уравнение Менделеева—Клапейрона). Состояние идеального газа характеризуют три инструментально измеряемых параметра: давление Р, Па; удельный объем v, м ³ кг, или плотность ρ, кг/м3; Т— температура, К.
Существует общая зависимость, связывающая между собой эти параметры, которая называется уравнением состояния. Параметры состояния, изменяющиеся в термодинамическом процессе, не зависят от его хода и определяются только начальным и конечным состояниями.
Для идеального газа уравнение состояния имеет простой вид и называется уравнением Менделеева—Клапейрона:
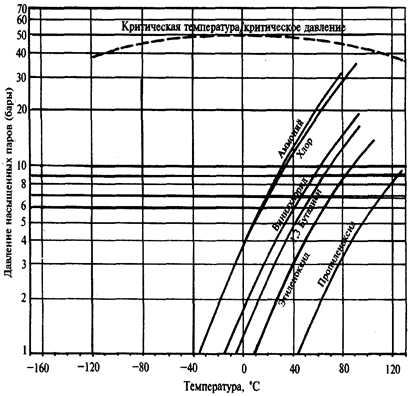
Рис. 55. Зависимость давления насыщения от температуры химических газов
pV-nRT или P=RT;
где п =т / М– количество вещества, моль;
т — масса вещества, г;
М — молярная масса вещества, г/моль,
R — 8,314 — массовая газовая постоянная;
µ
 Дж/(кг-К) = число 8,314 (Дж/кмоль К) — универсальная газовая постоянная для мольного количества газа, определенная Д. И. Менделеевым, µ — мольное число газа, равное его молярной массе.
Дж/(кг-К) = число 8,314 (Дж/кмоль К) — универсальная газовая постоянная для мольного количества газа, определенная Д. И. Менделеевым, µ — мольное число газа, равное его молярной массе.
Уравнение, устанавливающее связь между давлением, температурой и объемом газов, было получено французским физиком Бенуа Клапейроном. В форме уравнения состояния идеального газа его впервые использовал Д. И. Менделеев.
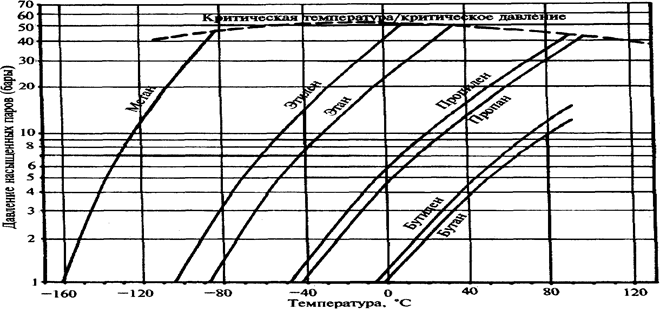
Рис. 56. Зависимость давления насыщения от температуры нефтяных газов
Как видно, два параметра определяют третий в любом термодинамическом процессе с неизменным количеством идеального газа.
Многие процессы, происходящие в природе и реализуемые в технике, можно приближенно рассматривать как процессы, в которых меняются лишь давление и температура.
Тщательная экспериментальная проверка газовых законов современными методами показала, что они достаточно точно описывают поведение реальных газов при небольших давлениях и высоких температурах, в противном случае наблюдаются значительные отступления от уравнения состояния. Что объясняется двумя причинами:
1) при сильном сжатии газов объем незанятого молекулами пространства становится сравним с объемом, занимаемым самими молекулами;
2) при низких температурах становится заметным взаимодействие между молекулами.
Пример 1: Какой объем займут 96 г кислорода при 3 барах (300000 Па) давления и температуре 77° С?
Решение: 1. Прежде всего определим, сколько молей составляют 96 г кислорода. Из Периодической таблицы элементов находим, что атомная масса кислорода составляет 15,9994. Это значит, что один моль кислорода (6,02 х 1023 атомов) будет иметь массу -16 г. Соответственно молекула кислорода, состоящая из двух атомов, будет иметь массу 32 г/моль.
2. Далее определим, сколько молей кислорода составляет 96 г.
96 г: 32 г/моль = 3 моля.
3. Теперь, используя уравнение Менделеева—Клапейрона, найдем объем:
рV = m•R•T откуда, V = m•R•T
M p
Заметим, что Дж = Н • м, а Па = Н/м3.
Пример 2: Определим, какое количество паров (масса) содержится в танке объемом 5000 м3 после выгрузки бутана (С6Н10), если манометрическое давление в танке составляет 0,1 бара, а температура 5°С?
Решение: Из уравнения состояния идеального газа рV = m • R • T
M
Определим искомую величину: m = р • V •M
R • T
Для нашего примера давление р будет равно сумме манометрического и атмосферного давлений: р = 1013 мбар + 100 мбар = 1,11 бара, или же 1,11 • 105 Па, а температура Т = 273 + 5° С.
Подставляя известные величины в выражение (1), получаем массу паров бутана, оставшихся в грузовом танке после выгрузки сжиженного газа:
m = 1.11 • 105 • 5 • 10³ • 58,1 = 0,0138 • 108 кг = 13 8 т
8,31434. 278
Не нашли, что искали? Воспользуйтесь поиском: