
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
А. Окисление пуриновых нуклеозидов
Аденозин ® (аденозиндезаминаза, +Н2О, –NH4+) инозин® ( пуриннуклеозидфосфорилаза, +Фн –рибозил-1-Ф) гипоксантин (6-оксопурин) ® (ксантиноксидаза, +О2, +Н2О → Н2О2) ксантин (или 2,6-диоксопурин) ®(ксантиноксидаза, +О2, +Н2О → Н2О2) мочевая к-та (или 2,6,8-триоксопурин)
Мочевая к-та – конечный продукт распада пуриновых оснований.
Б. Распад пиримидиновых нуклеозидов
Они распадаются до бета-аланина, который окисляется до СО2 и NH3. А также до бета-амилоизобутирата. Аммиак, образующийся при распаде, обезвреживается с образованием мочевины.
Повышение содержания мочевой к-ты в крови (гиперурикемия) наблюдается при повышенном распаде пуриновых нуклеотидов (как поступающих с пищей, так, возможно, и собственных).
Однако, мочевая к-та плохо растворима в кислой среде, поэтому может кристаллизоваться и осаждаться в суставах (подагра), в мочевыводящих путях (мочекаменная болезнь). Лечение – растворение с помощью содового питья (образуются хорошо растворимые ураты).
Образование креатинина
Креатинин образуется из креатина – азотистого соединения мышечной ткани. Креатин синтезируется в печени из АК: АРГ, МЕТ, ГЛИ. Затем креатин поступает в мышцу, где связывает фосфат с образованием креатинфосфата.
Иногда креатинфосфат "теряет" фосфат, тогда образуется креатинин – конечный продукт распада креатина (в креатинине образуется связь между азотом аминогруппы и углеродом карбокси-группы).
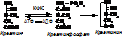
Количество креатинина в моче определяется как показатель клубочковой фильтрации почек (он не реабсорбируется). Также определяют клиренс креатинина – сравнение содержания его в крови и в моче.
Все конечные продукты, содержащиеся в крови, составляют остаточный азот крови – это азот, остающийся в растворе после осаждения белков. В норме остаточный азот 14-28 ммоль/л. Он состоит из азота промежуточных продуктов (пептиды, АК, билирубин, нуклеотиды, креатин, индол) и азота конечных продуктов (мочевина, мочевая кислота, креатинин, индикан).
Образование конечных безазотистых продуктов
I. Превращение ПВК
В результате непрямого дезаминирования из АК образуются аммиак и кетокислоты.
ЛЕЙ ® кетокислоты ® жиры.
ИЛЕ, ЛИЗ, ФЕН, ТРИ, ТИР ® углеводы и жиры.
АЛА, ЦИС, СЕР, ГЛИ, ТРЕ ® ПВК.
ГЛУ ® альфа-КГ.
АСП ® оксалоацетат (ЩУК).
Пировиноградная к-та (ПВК) подвергается окислительному декарбоксилированию (Ох-ДК), протекающему в четыре реакции. При этом молекула ПВК [СН 3 -СО-СООН] превращается в ацетил-КоА [СH 3 -CO-S-KoA] и углекислоту [СО 2 ]. Пируват-дегидрогеназный комплекс ферментов: пируватДК, ацетилТФ, ДГ липоевой к-ты. Коферменты: НАД, ФАД, ТДФ, HSKoA, липоевая к-та. НАД переходит в восстановленную форму НАД·Н 2, который поступает в дыхательную цепь митохондрий, где дает 3 АТФ.
Ацетил-КоА вступает в ЦТК (цикл трикарбоновых кислот, или цикл Кребса, или цикл лимонной кислоты).
II. Цикл Кребса:

[НАД·Н 2 поступает в дыхательную цепь митохондрий, где каждая молекула дает три АТФ; ФАД·Н 2 – аналогично, но дает две АТФ]
Суммарно ЦТК выглядит так:
СН 3 -СО-SКoA + 2H 2 O + Фн + АДФ ®2СО 2 + 3НАД·Н 2 + ФАД·Н 2 + АТФ + HSКоА
Функции ЦТК:
1. катаболическая – распад белков, жиров, углеводов;
2. интегративная – взаимосвязь обменов Б, Ж, У;
3. анаболическая – использование метаболитов ЦТК в синтезе необходимых организму соединений (напр., альфа-КГ ® глу; ЩУК ® асп);
4. энергетическая – выделение АТФ.
5. водород-генерирующая – образование восстановленных форм коферментов (3 НАД·Н 2 + ФАД·Н 2 ® 4 Н 2)
III. Биологическое окисление.
Биологическое окисление – это совокупность реакций окисления, протекающих в живом организме.
Лавуазье сравнивал биологическое окисление с «медленным горением», но это ограниченная аналогия, так как биологическое окисление:
а) протекает при низкой температуре,
б) протекает без появления пламени,
в) протекает в присутствии воды.
Существует несколько теорий биологического окисления:
1. Теория “активации” кислорода (Бах)
Образуются пероксиды: а) О=О®–О–О–
б) –О–О– + S ® SOO [треугольник, в углах которого три указанные буквы; S = субстрат; над стрелочкой реакции надпись “оксигеназы”]
в) SOO + S ’ ® SO + S ’ O [фермент пероксидаза]
Эта теория не объясняет окисление в животных тканях.
2. Теория активирования водорода (Палладин)
В клетках животных окисление идет благодаря дегидрированию:
А·Н 2 + Ко® А + Ко·Н 2 [фермент дегидрогеназа]
Ко·Н 2 + ½ О 2 ® Ко + Н 2 О
3. Современные представления (Палладин и Бах)
Биологическое окисление – это процесс переноса электронов. Если акцептором электронов выступает молекулярный кислород, то его называют “тканевым дыханием”:
RH 2 ® R + 2H + + 2e --
2H + + 2e -- + ½ O 2 ® H 2 O + 210 кДж
Биологическое окисление – многоступенчатый полиферментативный процесс, заключающийся в многократной передаче протонов и электронов по цепи ферментов. При этом химическая энергия выделяется небольшими порциями (постепенно, без взрывов).
Не нашли, что искали? Воспользуйтесь поиском: