
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Сингонии высшей группы
Кубическая сингония. Кристаллы кубической сингонии обладают наибольшим количеством элементов симметрии. Несколько осей выше второго порядка. Обязательно есть 4 L3. Пример – куб (рисунок 1е).
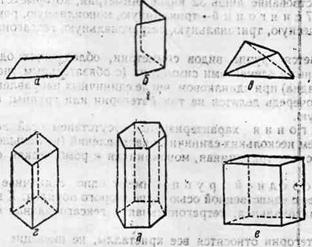
Рисунок 1 Простые формы, возможные в кристаллах
а – моноэдр, триклиниая сингония; б – диэдр, моноклинная сингония; в – ромбический тетраэдр, ромбическая сингония; г – тетрагональная призма, тетрагональная сингония: д – гексагональная призма, гексагональная сингония; е – куб, кубическая сингония
Совокупность элементов симметрии, характерную для того или иного вида симметрии, можно записать весьма кратко в виде своего рода формулы. В таблице 1 перечислены все 32 вида симметрии с соответствующими им формулами.
Таблица 1 32 вида симметрии кристаллов
| Триклинная сингония | ||
| нет элементов симметрии | моноэдрический вид симметрии | |
| С | пинакоидальный вид симметрии | |
| моноклинная сингония | ||
| L2 | диэдрический осевой вид симметрии | |
| P | диэдрический безосевой вид симметрии | |
| L2PC | призматический вид симметрии | |
| ромбическая сингония | ||
| 3L2 | ромбо-тетраэдрический вид симметрии | |
| L22P | ромбо-пирамидальный вид симметрии | |
| 3L23PC | ромбо-дипирамидальный вид симметрии | |
| тетрагональная сингония | ||
| Л4 | тетрагонально-тетраэдрический вид симметрии | |
| L4 | тетрагонально-пирамидальный вид симметрии | |
| L44P | дитетрагонально-пирамидальный вид симметрии | |
| L44L2 | тетрагонально-трапецоэдрический вид симметрии | |
| 2L2Л42Р | тетрагонально-скаленоэдрический вид симметрии | |
| L4PC | тетрагонально-дипирамидальный вид симметрии | |
| L44L25PC | дитетрагонально-дипирамидальный вид симметрии | |
| тригональная сингония | ||
| L3 | тригонально-пирамидальный вид симметрии | |
| L33P | дитригонально-пирамидальный вид симметрии | |
| L33L2 | тригонально-трапецоэдрический вид симметрии | |
| Л6С | ромбоэдрический вид симметрии | |
| Л63L23PC | дитригонально-скаленоэдрический вид симметрии | |
| гексагональная сингония | ||
| L3P | тригонально-дипирамидальный вид симметрии | |
| L33L24P | дитригонально-дипирамидальный вид симметрии | |
| L6 | гексагонально-пирамидальный вид симметрии | |
| L66P | дигексагонально-пирамидальный вид симметрии | |
| L66L2 | гексагонально-трапецоэдрический вид симметрии | |
| L6PC | гексагонально-дипирамидальный вид симметрии | |
| L66L27PC | дигексагонально-дипирамидальный вид симметрии | |
| кубическая сингония | ||
| 4L33L2 | пентагон-тритетраэдрический вид симметрии | |
| 4L33L26P | гексатетраэдрический вид симметрии | |
| 4L33LL23PC | дидодекаэдрический вид симметрии | |
| 3L44L36L2 | пентагон-триоктаэдрический вид симметрии | |
| 3L44L36L29PC | гексаоктаэдрический вид симметрии |
Изучение внешних форм минералов и отнесение их к тому или иному виду симметрии имеет существенное значение по той причине, что все свойства минералов тесно связаны с их структурой. Эмпирическим путем выведены законы, касающиеся особенностей кристаллов: закон плоскогранности и прямореберности кристаллов, закон постоянства углов, закон рациональности отношений параметров и ряд других. Эти законы позволяют ближе понять процессы роста и развития кристаллических форм, присущих тем или иным минералам.
Особенно большое значение имеет закон постоянства углов. Этот закон, известный как закон Стено-Ломонсова-Роме-Делиля, формулируется следующим образом: углы между соответственными гранями (и ребрами) во всех кристаллах одного и того же вещества постоянны. При росте кристаллов, в зависимости от условий, форма, число и размеры граней могут
изменяться, углы же между соответственными гранями растущего кристалла остаются неизменными.
Материальные частицы, слагающие кристаллические вещество, расположены в определенном порядке, они не заполняют полностью все пространство, а отстоят на некотором расстоянии друг от друга, образуя как бы скелет каждого кристалла. Расстояния между частицами (атомами, ионами и молекулами) для каждого данного направления в кристалле постоянны.
Такое правильное, закономерное расположение частиц в кристалле, называется кристаллической или пространственной решеткой.
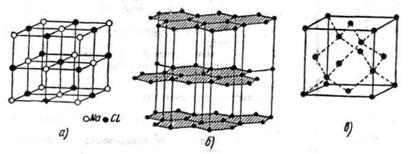
Рисунок 2 Структура кристаллической решетки некоторых минералов
а – галит; б—графит; в – алмаз
В зависимости от характера частиц, лежащих в узлах решетки, последняя бывает атомной, ионной и молекулярной. Так, кристаллическая решетка галита (каменной соли) состоит из ионов металла Na и галоида СI, располагающихся в вершинах элементарных кубов попеременно, в шахматном порядке (рисунок 2).
Решетка кристаллов графита состоит из атомов углерода С, расположенных плоскими слоями, причем в каждом слое они находятся в вершинах правильных шестиугольников. Расстояние между атомами в плоскости равно i, 43 А (знаком А обозначается единица длины, ангстрем; 1А=10-8 см), расстояние между плоскостями = 3,35, А (см. рисунок 2). Поэтому слои легко скользят один относительно другого. Те же атомы С, расположенные так, что каждая частица окружена четырьмя соседними, образующими вершины тетраэдра, дают вещество с совершенно иными свойствами, а именно алмаз (см. рисунок 2). Способность одного и того же химического соединения при изменении внешних факторов (главным образом температуры) кристаллизоваться в различных кристаллографических форумах с изменением физических свойств называется. Кроме того, в природных условиях достаточно широко распространено явление изоморфизма, под которым понимается, свойство родственных по химическому составу веществ кристаллизоваться в близких формах, образуя кристаллы переменного состава, так называемые смешанные кристаллы. Примером такого замещения одного элемента другим может служить MgCO3 – FeCO3 (магнезит и сидерит). Изоморфные замещения при высоких температурах происходят в более широких пределах, чём при низких.
Многие кристаллы построены чрезвычайно сложно; выяснение строения кристаллической решетки для естественных, а также и искусственных кристаллов составляет важную задачу современной кристаллографии.
Не нашли, что искали? Воспользуйтесь поиском: