
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Основные газовые и стехиометрические законы.
Пример 1. Какому количеству вещества соответствует 56 г азота и сколько молекул азота содержится в этом количестве?
Решение. Молярная масса атома азота (N) равна 14 г, молярная масса молекулы азота (N2) равна 28 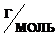 . Следовательно, 56 г соответствует двум моль.
. Следовательно, 56 г соответствует двум моль.
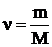 , (1)
, (1)
где ν – количество вещества;
m – масса вещества;
M – молярная масса вещества.
 = 2 моль
= 2 моль
Пример 2. Найти массу 200 л хлора при н. у.
Решение. Из закона Авогадро следует, что один моль любого газа при н. у. занимает объем 22,4 л (молярный объем). Один моль газообразного хлора Cl2 имеет массу 71 г (молярная масса атома хлора – 35,5 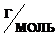 ).
).
71 г – 22,4 л
x г – 200 л
 = 633,2 г.
= 633,2 г.
Задания
1. Сопоставить числа молекул, содержащихся в 1 г NH3 и в 1 г N2. В каком случае и во сколько раз число молекул больше?
2. Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
3. Исходя из молярной массы углерода и воды, определить абсолютную массу атома углерода и молекулы воды.
4. Выразить в молях: а) 6,02·1022 молекул С2Н6; б) 1,8·1024 атомов азота; в) 3,01·1023 молекул NH3. Чему равны молярные массы указанных веществ?
5. Определить массу (в граммах) порции гидроксида бария, в котором содержится 1,806·1023 атомов водорода.
6. Определить массовую долю кислорода (в процентах) в оксиде азота (IV).
7. Определить количество вещества (моль) в порции аммиака, содержащей 2,408·1023 молекул.
8. Определить массу 11,2 л (н.у.) хлороводорода.
9. Определить число атомов водорода в 6,72 л (н.у.) метана (СН4).
10. Определить массовую долю (в процентах) кислорода, входящего в состав хлората калия.
11. Определить массу (в граммах) порции сульфата калия, в котором содержится 6,02·1023 атомов кислорода.
12. Сколько литров водорода, взятого при н.у., можно получить из 360 г воды?
13. Определить количество вещества (моль) в порции оксида натрия, содержащей 1,806·1023 атомов натрия.
14. Определить молярную массу хлора, если масса 500 мл (н.у.) его равна 1,585 г.
15. Определить число атомов азота в 52,2 г нитрата бария.
16. Какой объем при н.у. занимает смесь 1,35 моль Н2 и 0,6 моль О2?
17. Какой из газов легче воздуха: 1) фтор; 2) оксид азота (II); 3) аммиак; 4) кислород; 5) оксид азота (IV). Ответ подтвердите расчетом.
18. Рассчитайте массовую долю кальция в карбонате кальция (%).
19. Вычислите массовую долю кристаллизационной воды в дигидрате сульфата кальция (в процентах) – CaSO4·2H2O.
20. Какова масса водорода, содержащего 1·1023 молекул?
21. Какой объем займет смесь, состоящая из хлора количеством вещества 0,5 моль и кислорода количеством вещества 1,25 моль?
Моль – количество простого или сложного вещества, содержащее такое число структурных частиц: атомов, молекул, ионов или электронов, которое равно числу атомов в 12 г изотопа углерода 12 С и составляет 6,022·1023 (постоянная Авогадро, NА).
1 моль – 6,022·1023 молекул
2 моль – х
 = 12,044·1023 молекул.
= 12,044·1023 молекул.
Не нашли, что искали? Воспользуйтесь поиском: