
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
ИДЕАЛЬНЫЕ ГАЗЫ, ПАРАМЕТРЫ СОСТОЯНИЯ, ОСНОВНЫЕ ЗАКОНОМЕРНОСТИ
Величины, характеризующие тело в данном состоянии, называются параметрами состояния. Чаще всего состояние тела определяется следующими параметрами: удельным объемом (v), абсолютным давлением (p) и абсолютной температурой (T).
1. Удельный объем (v)тела представляет собой объем единицы его массы. Это величина, обратная плотности тела (r).
Если V — объем в м 3 занимаемый телом массой М кг, то удельный объем
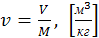 (1)
(1) 
Очевидно, что
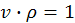 (2)
(2)
2. Абсолютное давление р измеряют силой, приходящейся на единицу поверхности. Так как за единицу силы принимают 1 ньютон, а за единицу поверхности — квадратный метр, то давление измеряют вньютонах на квадратный метр (Н/м2 или Па). Во всех термодинамических уравнениях пользуются этой единицей, и поэтому в применяемые формулы следует подставлять числовое значение давления в Н/м2.
Для практических целей удобнее измерять давление в кН/м2 (килоньютон на квадратный метр или кПа), МН/м2 (меганьютон на квадратный метр или МПа). Часто давление замеряется в Барах. Эта единица в 105 раз больше 1 Н/м2.
Соотношения между используемыми в технике единицами измерения давления даны в таблице 1.
Абсолютное давление может быть определено по формуле:

где B – атмосферное или барометрическое давление, а 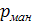 – избыточное давление, замеренное манометром.
– избыточное давление, замеренное манометром.
Если абсолютное давление p меньше барометрического давления B, то возникает вакуум или разряжение. Величину вакуумного давления  можно определить по формуле:
можно определить по формуле:

Таблица 1 - Соотношения между единицами давления
| Единицы | Ньютон на квадратный метр Н/м2 | Бар (105 Н/м2) | Техническая атмосфера am | Физическая атмосфера атм |
| 1 кГ/см2 (1 am) 1 атм (физ.) 104 мм вод. ст. 103 мм рт. ст. 10 lbf/ in2 | 98066,5 98066,5 133322 | 0,980665 1,01325 0,980665 1,33322 0,68948 | 1,03323 1,35951 0,70307 | 0,96784 0,96784 1,31579 0,68046 |
Продолжение таблицы 1 - Соотношения между единицами давления
| Единицы | Миллиметр водяного столба мм вод. cm. | Миллиметр ртутного столба мм рт. cm. | Английским фунт-сила на квадратный дюйм |
| 1 кГ/см2 (1 am)1 атм (физ.) 104 мм вод. ст. 103 мм рт ст. 10 lbf/in2 | 104 104 1,35951×104 | 785,56 735,56 103 517,149 | 14,223 14,696 14,223 19,336 10,000 |
3. Третьей основной величиной, характеризующей состояние тела, является абсолютная температура (Т). Она измеряется в градусах Кельвина (К), кроме того в быту и технике широко используется температура (t), определяемая по шкале Цельсия. Связь между этими температурами вытекает из следующей зависимости:

В США и Англии для измерения температуры применяют шкалу Фаренгейта. Для перевода показаний этой шкалы в градусы Цельсия служат соотношения:
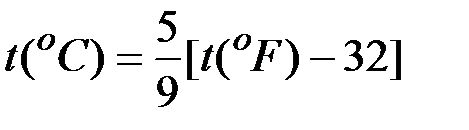
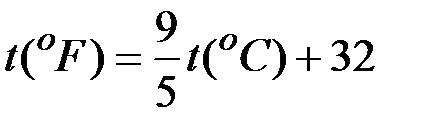
Под идеальным газом понимают воображаемый газ, в котором отсутствуют силы притяжения между молекулами, а собственный объем молекул исчезающе мал по сравнению с объемом междумолекулярного пространства. Таким образом, молекулы идеального газа принимаются за материальные точки. Все существующие газы при высоких температурах и малых давлениях по своим свойствам приближаются к свойствам идеального газа. Поэтому такие газы можно также считать идеальными. Если же притяжением молекул и их объемом пренебречь нельзя, то такой газ называют реальным (пар). Все идеальные газы подчиняются законам Бойля-Мариотта и Гей-Люссака.
pv = const (T = const);

Уравнения состояния идеального газа связывают между собой основные параметры состояния p, v и t и могут быть представлены следующими зависимостями:
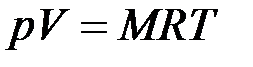
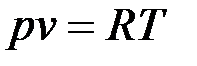
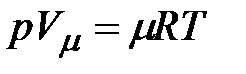 ,
,
где M – масса газа в кг, R – газовая постоянная исследуемого газа (Дж/кгК),  - объем одного киломоля газа,
- объем одного киломоля газа, 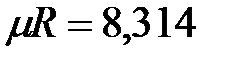 кДж/кмольК – универсальная газовая постоянная
кДж/кмольК – универсальная газовая постоянная
Для усвоения материала используются следующие задания (Л. 2 № 1, 2, 3, 5, 6, 8, 10, 11, 12, 13, 16-23, 25-30, 32-43, 46, 47, 48, 50, 51, 53-58, 60, 62-66, 68-76).
Отчетность по результатам данного занятия проводится письменно в соответствии с заданием или в устной форме в виде опроса.
Не нашли, что искали? Воспользуйтесь поиском: