
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Программа дисциплины для студентов (Силлабус) составлена на основании _________________Биохимия____________________________________
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА
РЕСПУБЛИКИ КАЗАХСТАН
Казахский агротехнический университет им. С. Сейфуллина
Кафедра физики
Учебно-методический комплекс
По биологической химии
для специальности 5В072700 – Технология продовольственных
продуктов
5В072800 – Технология перерабатывающих
производств
Астана 2010
Рассмотрено и одобрено «Утверждаю»
к изданию на заседании Председатель Методического
методического совета совета Казахского агротехнического
Казахского агротехнического университета им. С.Сейфуллина
университета им. С. Сейфуллина А. М. Абдыров
протокол №____от_ ___________________________ «______»_______2010 г. «_____»_______________2010 г.
УМК по дисциплине «Биохимия»
Составитель: Оспанова Сауле Гельмановна – доцент кафедры
физики и химии Казахского агротехнического
университета им. С. Сейфуллина, кандидат
биологических наук
Рецензент: Себряева Надежда Сергеевна - доцент кафедры
физики и химии Казахского агротехнического
университета им. С.Сейфуллина, кандидат
химических наук
Учебно-методический комплекс содержит глоссарий, силлабус, тезисы лекций, лабораторно-практические работы, задания для самосто-ятельной работы студентов, вопросы рубежного и итогового контроля в соответствии с типовой программой дисциплины.
Рассмотрено и одобрено на заседании кафедры физики и химии
протокол № 5 от 29.11. 2010 г.
Рассмотрено и рекомендовано на заседании методической комиссии
факультета компьютерных систем и профессионального образования
протокол № от 12. 2010г.
Содержание
Стр.
1 Глоссарий 4
2 Силлабус 6
3 Тезисы лекций 13
3.1 Введение в биохимию 13
3.2 Липиды 14
3.3 Углеводы 17
3.4 Белки 18
3.5 Нуклеиновые кислоты 20
3.6 Ферменты 21
3.7 Витамины 22
3.8 Гормоны 24
3.9 Введение в обмен веществ 25
3.10 Метаболизм углеводов 27
3.11 Метаболизм липидов 30
3.12 Метаболизм белков 36
3.13 Общие пути катаболизма. Обмен энергии 41
3.14Биосинтез белка и нуклеиновых кислот 51
4 Лабораторные занятия: 52
4.1 Введение. Структура клетки. 52
4.2 Структура липидов 55
4.3 Структура углеводов 57
4.4 Структура и свойства крахмала 58
4.5 Структура белков 60
4.6 Физико-химические свойства белков: реакции осаждения, диализ 63
4.7 Определение изоэлектрической точки белков 69
4.8 Методы анализа белков: хроматография, электрофорез 71
4.9 Структура нуклеиновых кислот 76
4.10Изучение свойств ферментов 77
4.11Определение витамина С в биологических объектах 78
4.12Изучение химического состава молока 79
4.13Изучение химического состава мяса, крови, мочи 81
5 Тесты промежуточного контроля 84
Список литературы 89
Приложения: справочный материал 90
ГЛОССАРИЙ
Биологическая химия - наука, изучающая химический состав и химические процессы, протекающие в живых организмах
Анаболизм - процесс синтеза веществ в организме
Катаболизм – процесс распада сложных веществ на простые вещества
Метаболизм – совокупность процессов катаболизма и анаболизма
Белки – высокомолекулярные полипептиды, состоящие из остатков 20 природных аминокислот
Ферменты – биологические катализаторы белковой природы
Витамины – низкомолекулярные вещества различной химической природы, регуляторы процессов метаболизма
Гормоны - регуляторы процессов метаболизма, роста и развития организмов
Липиды – обширная группа органических соединений, объединяемых общим свойством – гидрофобностью, большинство из которых по химической природе являются сложными эфирами
Углеводы – полифункциональные органические вещества, содержащие карбонильную и спиртовые группы
Жиры – простые липиды, сложные эфиры трехатомного спирта глицерина и высших жирных кислот
Энзимология – учение о ферментах
Эндокринология – учение о гормонах
Клетка – элементарная функциональная единица живого
Гликолиз – процесс распада глюкозы
Гликогенолиз – процесс распада гликогена
Переваривание – процесс гидролитического распада питательных веществ, под действием ферментов- гидролаз
АТФ – аденозинтрифосфат
АМФ – аденозинмонофосфат
АДФ-аденозиндфосфат
Биосинтез – процесс синтеза веществ, протекающий в живых организмах
Липолиз – процесс распада липидов
Протеолиз – процеcc распада белков
Кофермент- небелковая часть сложных ферментов
Протеины – простые белки
Протеиды- сложные белки
Стерины (стеролы) – полициклические спирты, производные циклопентанпергидрфенантрена
Стериды – сложные эфиры – стеринов и высших жирных кислот (ВЖК)
Воска- простые липиды, сложные эфиры высших одно (двух) атомных спиртов и ВЖК
Репликация – процесс самоудвоения молекулы ДНК
ДНК – дезоксирибонуклеиновая кислота
РНК- рибонуклеиновая кислота
Транскрипция – процесс синтеза и-РНК
Трансляция – процесс биосинтеза белка
и (м) -РНК-информационная (матричная) РНК
рРНК – рибосомальная РНК
тРНК-транспортная РНК
Инициация – образование первой связи между мономерами, начало процесса биосинтеза полимера
Элонгация – процесс удлинения полимерной цепи
Терминация - окончание процесса биосинтеза полимера, обрыв синтезированной полимерной цепи
ЦТК – цикл трикарбоновых кислот
БО-биологическое окисление – последовательность окислительно-восстановительных реакций, в результате которых осуществляется передача водорода от окисляющихся субстратов к кислороду
ОФ-окислительное фосфорилирование- процесс биосинтеза АТФ за счет энергии биологического окисления
НАД-никотинамидадениндинуклеотид
ФАД-флавинадениндинуклеотид
ДГ – дегидрогеназа, фермент осуществляющий перенос водорода
Оксидоредуктазы – ферменты, катализирующие реакции переноса электронов
Трансферазы - ферменты, катализирующие реакции переноса групп атомов
Гидролазы – ферменты, катализирующие реакции гидролиза с участием воды
Лиазы - ферменты, катализирующие реакции негидролитического распада с образованием двойных связей и присоединения по месту двойной связи
Изомеразы - ферменты, катализирующие реакции образования изомеров
Лигазы (синтетазы) - ферменты, катализирующие реакции синтеза
Программа дисциплины для студентов (Силлабус) составлена на основании _________________Биохимия____________________________________
_________РУМО 22.06.2006 г._______________________
(название типовой программы дисциплины, кем и когда утверждена)
для высших учебных заведений для специальности (направления)
BIO 2211 – Технология перерабатывающих производств
BIO 2210 – Технология продовольственных продуктов
(код и наименование)
и в соответствии с рабочим учебным планом специальности, утвержденным «_____» _______________ 2010 г.
Рассмотрена на заседании кафедры физики и химии_______
___________________________________________________________
(наименование кафедры)
«30» _09_ 2010г., протокол № _03_____
Заведующий кафедрой
к.п.н., доцент ___________ Э. Ж. Алимкулова
(подпись) (Ф.И.О.)
Рекомендована комитетом по учебным программам факультета ВиТЖ «_ _» ____ 2010 г., протокол № ____
Председатель
комитета ______________ ____________ (подпись) (Ф.И.О.)
1. ДАННЫЕ О ПРЕПОДАВАТЕЛЕ:
Преподаватель кафедры физики и химии:
Оспанова С.Г., к.б.н., доцент
Приемные часы: по расписанию
Аудитории: 0412, 0404
2.ДАННЫЕ О ДИСЦИПЛИНЕ:
Код дисциплины BIO 2211 BIO 2210
для специальности 5В072700 5В072800
Дисциплина: Биологическая химия
Форма обучения: очная
Курс:2
Семестр - 4
Кредиты: 2
Лекции (в час) 15
Лабораторные (в час) 30
СРСП 15
СРС 30
Всего: 90
Форма контроля: экзамен
РАСПРЕДЕЛЕНИЕ УЧЕБНОГО ВРЕМЕНИ
| Недели Семестра | Всего | |||||||||||||||
| Лекции (в час) | ||||||||||||||||
| ЛПЗ (в час) | ||||||||||||||||
| СРСП | ||||||||||||||||
| СРС | ||||||||||||||||
| Итого |
3. Пререквизиты: Неорганическая химия, органическая химия, физическая и коллоидная химия, аналитическая химия.
4. Постреквизиты: Физиология растений и животных, микробиология, специальные дисциплины биологического и технического направления.
5. Краткое описание курса: Дисциплина биологическая химия изучает химический состав, закономерности протекания биохимических реакций в организме растений, животных и человека. Является теоретической основой специальных дисциплин.
Цели дисциплины: Изучить принципы организации биологических систем, химический состав, свойства и функции химических соединений, являющихся структурной и функциональной основой жизнедеятельности биосистем.
Задачи изучения: Освоить теоретические знания по основным разделам биохимии; навыки постановки биохимических исследований, умение применять полученные теоретические знания и практические навыки в профессиональной деятельности.
6. СОДЕРЖАНИЕ КУРСА
6.1 Перечень лекционных занятий
| Наименование темы | Объем, час | Литература | Текущий контроль, балл |
| Введение. Структурная организация клетки и систем органов, связанных с питанием. Химический состав организма. | Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы биохимии», М.Высшая школа, 1985; Оспанова С.Г. «Пищевая биохимия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана 2010. | 0,6 | |
| Липиды | Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы биохимии», М.Высшая школа, 1985; Оспанова С.Г. «Пищевая биохимия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана 2010. | 0,6 | |
| Углеводы. Строение, свойства, значение в питании | 0,6 | ||
| Белки. Строение, свойства, функции в организме. | 0,6 | ||
| Нуклеиновые кислоты. | Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы биохимии», М.Высшая школа, 1985; Оспанова С.Г. «Пищевая биохимия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана 2010. | 0,6 | |
| Ферменты. | 0,6 | ||
| Витамины | 0,6 | ||
| Гормоны. | Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы биохимии», М.Высшая школа, 1985; Оспанова С.Г. «Пищевая биохимия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана | ||
| Введение в обмен веществ. Обмен углеводов | 0,6 | ||
| Обмен липидов | 0,6 | ||
| Обмен белков и аминокислот | |||
| Общие пути катаболизма. Обмен веществ и энергии | 0,6 |
6.2 Перечень лабораторных занятий
| Наименование лабораторных занятий | Объем, час | Литература | Тек. контр. балл |
| Техника безопасности. Техника постановки биохимического эксперимента. Входной контроль. | С.Г. Пищевая биохимия, Астана 2004г. С.Г. Оспанова УМКД по биологической химии для специальностей ТПП –Астана 2010 | ||
| Липиды. Изучение липидов на примере лецитина куриного яйца. Качественные реакции на жиры: дегидратация глицерина, реакция с гидроксидом меди. Качественные реакции на углеводы: реакция Троммера, Фелинга, реакция с йодом на крахмал. Пектиновые вещества | С.Г. Пищевая биохимия, Астана 2004г. С.Г. Оспанова УМКД по биологической химии для специальностей ТПП –Астана 2010 | ||
| Качественные реакции на углеводы: реакция Троммера, Фелинга, реакция на многоатомные спирты. Гидролиз крахмала. Виды брожения. | |||
| Качественные реакции на белки: биуретовая реакция, нингидриновая реакция, определение полноценности белка – обнаружение незаменимых аминокислот (реакция Фоля, ксантопротеиновая реакция). | |||
| Структура нуклеопротеидов. Гидролиз нуклеопротеидов. | |||
| Биохимия молока РК-1 | С. Г. Пищевая биохимия, Астана 2004г. С.Г. Оспанова УМКД по биологической химии для специальностей ТПП – Астана 2010 | ||
| Биологически активные вещества. Витамины. Количественное определение витамина С в овощах и фруктах. Общие свойства ферментов. Химическая природа гормонов и их функции. | |||
| Физико-химические изменения белков пищевых продуктов под воздействием температуры, рН среды, ферментов. | С. Г. Пищевая биохимия, Астана 2004г. С.Г. Оспанова УМКД по биологической химии для специальностей ТПП – Астана 2010 | ||
| Метаболизм углеводов, белков, липидов. Основы рационального питания. РК2 |
7. ГРАФИК ВЫПОЛНЕНИЯ И СДАЧИ ЗАДАНИЙ СРС ПО ДИСЦИПЛИНЕ
| № | Тема занятия | Задания срс, цель и содержание | Рекомендуемая литература | Форма контроля | Срок сдачи | Оце-ночные бал-лы |
| 1. | Структурная орга-низация клетки и систем органов, связанных с пита-нием. Химический состав организма. | Зарисовать строение клетки, нервной и пищеварительной системы. Знать химический состав растений, микроорганизмов, животных и человека, роль органических веществ, воды и минеральных солей в жизнедеятельности. | Анисимов А.А. «Основы био-химии», М.Высшая школа, 1986; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы био-химии», М.Высшая школа, 1985; Оспанова С.Г. «Пищевая биохи-мия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана 2010.. Комов В.Б., Шведова В.И. Биохимия, М., Дрофа, 2004. | Проверка письм. задания, устный опрос | 2-неде-ля | |
| 2. | Липиды | Знать структуру, классификацию и био-логическую роль липидов в организме. Письменно составить таблицу. Знать прев-ращения липидов в технологическом процессе. | Проверка письм. задания, устный опрос | 3-неде-ля | ||
| Углеводы. Строение, свойства, значение в питании. Белки. Строение, свойства, функции в организме | Знать структуру, классификацию и био-логическую роль углеводов в организме. Письменно составить таблицу. Знать превращения белков в технологическом процессе. Знать структуру, классификацию и био-логическую роль белков в организме. Письменно составить таблицу. Написать реакцию образования пентапептида. Знать превращения белков в технологическом процессе. | Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М. Вы-сшая школа, 1985; Филиппович Ю.В. «Основы биохимии», М.Высшая шко-ла, 1985; Оспанова С.Г. «Пищевая био-химия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, а 2010.. Комов В.Б., Шведова В.И. Биохимия, М., Дрофа, 2004. | Проверкаписьм. задания, устный опрос | 4-неде-ля 5-неде- Ля | ||
| Нуклеиновые кислоты. | Знать структуру и биологическую роль нуклеиновых кислот. Зарисовать первичную и вторичную структуру. Показать положение химических связей в молекуле. | Проверка письм. задания, устный опрос | 6-неде-ля | |||
| Ферменты. | Знать номенклатуру, структуру, классифи-кацию и функции ферментов. Механизм катализа. Типы ферментных систем. Активный центр, аллостерический центр. | Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы биохимии», М.Высшая школа, 1985; Оспанова С.Г. «Пищевая биохимия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана 2010. Комов В.Б., Шведова В.И. Биохимия, М., Дрофа, 2004. | Проверкаписьм. задания, устный опрос | 7-неде-ля | ||
| 7. | Витамины. | Знать номенклатуру и биологические функции витаминов. Письменно составить таблицу, записать формулы витаминов и биологические функции. | Проверкаписьм. задания, устный опрос | 8-неде- ля | ||
| 8. | Биологически ак-тивные вещества. Гормоны. Антиби-отики. Алкалоиды. | Составить таблицу биологически активных веществ. Знать структуру, классификацию, биологическую роль. | Проверкаписьм. устный опрос | 9-неде-ля | ||
| Обмен липидов | Составить таблицу по обмену липидов. Знать процессы катаболизма и анаболизма липидов. Ферменты, витамины, гормоны участвующие в метаболизме липидов. Окисление глицерина, β-окисление ВЖК, функции желчных кислот биосинтез жиров. | Анисимов А.А. «Основы биохи-мии», М.Высшая школа, 1986.; Сеитов З.С. «Биохимия», Алматы 2000; Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985; Филиппович Ю.В. «Основы биохи-мии», М. Высшая школа, 1985; Оспанова С.Г. «Пищевая биохи-мия», Астана 2004; «Биохимия ч.1», «Биохимия ч.-2» Астана 2008, Астана 2010. | Проверкаписьм. задания, устный опрос Устный опрос устный опрос | 10-неде- Ля | ||
| Обмен углеводов. | Знать процессы метаболизма углеводов. | |||||
| Обмен белков и аминокислот | Знать процессы метаболизма белков и нуклеиновых кислот. | |||||
| Обмен воды и минеральных ве-ществ, энергии | Знать биологическую роль воды и минеральных веществ., БО и ОФ. Взаимосвязь обменных процессов. | |||||
| Физиологические основы питания | Понимать химические основы технологии пи-щевых продуктов. Составить меню рац. питания | 14-15 |
СПИСОК ЛИТЕРАТУРЫ
ОСНОВНАЯ ЛИТЕРАТУРА:
1. Анисимов А.А. «Основы биохимии», М.Высшая школа, 1986.;
2.Комов.В.П,, В.Н.Шведова Биохимия., М., «Дрофа» 2004г.
4.Сеитов З.С. Биологическая химия Алматы,2000.
5. Кретович В.Л., «Биохимия растений», М.Высшая школа, 1985
6.Оспанова С.Г. Пищевая биохимия, Астана, 2004
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
1. Ленинджер А. Биохимия, М. 1974
2.Филлипович Ю.Б. Основы биохимии. М., «Высшая школа», 1985.
3.Страйер А. Биохимия т.1-2. М., «Мир», 1984-1985.
4.Оспанова С.Г. Биохимия - ч-1, Астана 2008
5. Оспанова С.Г. Биохимия-ч.2 Астана 2010
9. ПОЛИТИКА КУРСА - Не опаздывать на занятия, не пропускать занятия. Отключать сотовые телефоны во время занятий. Своевременно выполнять задания СРС. Соблюдать правила внутреннего распорядка университета, культуру общения.
10. ИНФОРМАЦИЯ ПО ОЦЕНКЕ ЗНАНИЙ
| Виды занятий и работ студентов | Количество баллов: min/ max | |||
| I | ТЕКУЩИЙ КОНТРОЛЬ: Лекции ЛПЗ СРС | 20/40 4/8 8/16 8/16 | ||
| II | ПРОМЕЖУТОЧНЫЙ КОНТРОЛЬ: Рубежный контроль 1 Рубежный контроль2 | 10/20 5/10 5/10 | ||
| ИТОГО: | 30/60 | |||
| III | ИТОГОВЫЙ КОНТРОЛЬ Экзамен | 20/40 | ||
| ВСЕГО | ||||
| СХЕМА ОЦЕНКИ ЗНАНИЙ СТУДЕНТОВ НА ЭКЗАМЕНЕ | ||||
| Экзаменационная оценка | Оценка в баллах (в %) | |||
| 1. | Удовлетворительно | 50-74 | ||
| 2. | Хорошо | 75-89 | ||
| 3. | Отлично | 90-100 | ||
ШКАЛА ОЦЕНКИ ЗНАНИЙ СТУДЕНТОВ
| Оценка по буквенной системе | Цифровой эквивалент баллов | Процентное содержание Баллов | Оценка по традиционной системе |
| А | 4,0 | 95-100 | ОТЛИЧНО |
| А- | 3,67 | 90-94 | |
| В+ | 3,33 | 85-89 | ХОРОШО |
| В | 3,0 | 80-84 | |
| В- | 2,67 | 75-79 | |
| С+ | 2,33 | 70-79 | УДОВЛЕТВОРИТЕЛЬНО |
| С | 2,0 | 65-69 | |
| С- | 1,67 | 60-64 | |
| Д+ | 1,33 | 55-59 | |
| Д | 1,0 | 50-54 | |
| F | 0 | 0-49 | НЕУДОВЛЕТВОРИТЕЛЬНО |
11. Политика выставления оценок: объективность, прозрачность.
Тезисы лекций по дисциплине
1 - ВВЕДЕНИЕ
Биологическая химия - наука, изучающая химическую природу веществ, входящих в состав живых организмов, их превращения, а также связь этих превращений с деятельностью органов и тканей, т.е. физиологическими функциями.
Постоянство химического состава организма обеспечивается способностью живых клеток воссоздавать, ресинтезировать разрушенные вещества - самообновляться. Основным субстратом для синтеза служат поступающие в организм из окружающей среды питательные вещества - белки, липиды, углеводы, витамины, кислород, минеральные веществ и вода. В живых клетках расщепление веществ (диссимиляция, катаболизм) постоянно сочетается с их синтезом (ассимиляция, анаболизм). Совокупность сопряженных процессов распада веществ и синтеза новых, необходимых для организма называют обмен веществ – метаболизм.
Элементарной функциональной единицей живого является клетка.
Биологическая химия, как самостоятельная научная дисциплина обозначилась во второй половине ХIХ в., когда в ряде университетов были созданы кафедры биохимии, написаны учебники, начали издаваться научные журналы, и курс биохимии стал обязательной составной частью учебных планов при подготовке биологов, медиков и зооветеринарных специалистов. Развитие биохимии тесным образом связано с потребностями практики – медицины, сельского хозяйства, промышленности, науки.
Исключительную роль в расширении возможностей научного поиска в биохимии сыграло внедрение в практику биохимических работ рентгеноструктурного анализа, инфракрасной и ультрафиолетовой спектрофотометрии, флуоресцентного и полярографического анализа, электрофореза, хроматографии, массспектрометрии, разделения веществ в гравитационном поле ультрацентрифугированием, электронного пара-магнитного резонанса, ядерного магнитного резонанса, электрофореза, хроматографии и др. Биохимические методы используются главным образом для изучения закономерностей процессов катаболизма и анаболизма в живых организмах с тем, чтобы направленно влиять на эти процессы.
Биологическая химия является теоретической основой и фундаментом для изучения профильных дисциплин многих специальностей.
Для понимания химических процессов, протекающих в организме, следует хорошо знать структуру веществ, входящих в его состав, т.е. изучить статическую биохимию, а затем их превращения – динамическую биохимию.
Липиды
ЛИПИДЫ - органические вещества, характерные для живых организмов, нерастворимые в воде, но растворимые в органических растворителях и друг в друге.
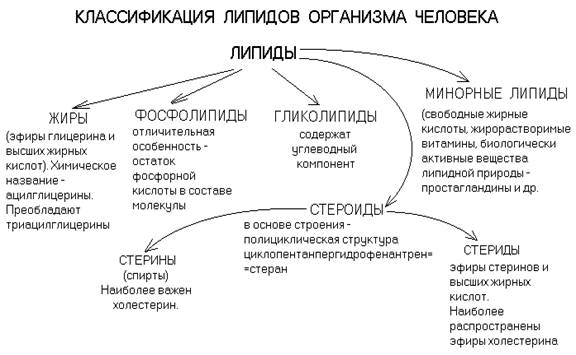
Группы липидов отличаются по степени гидрофобности. Фосфолипиды и гликолипиды являются полярными липидами. Холестерин занимает промежуточное положение между полярными и абсолютно гидрофобными липидами. Абсолютно гидрофобными являются триглицериды и эфиры холестерина. Большинство липидов (кроме стеринов и некоторых минорных липидов) содержат высшие жирные кислоты (ВЖК).
В состав мембран входят только ФОСФОЛИПИДЫ, ГЛИКОЛИПИДЫ и ХОЛЕСТЕРИН.
ЖИРНЫЕ КИСЛОТЫ, ХАРАКТЕРНЫЕ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА
Кислота называется жирной, если число углеродных атомов в ее молекуле больше четырех. Преобладают длинноцепочечные жирные кислоты (число атомов углерода 16 и выше). Количество углеродных атомов и двойных связей обозначается двойным индексом. Например: С18:1 (9-10). В данном случае 18 – число атомов углерода и 1 – количество двойных связей. В скобках указывается местоположение двойных связей (по номерам углеродных атомов). Самые распространенные ВЖК:
1. С18:0 - стеариновая,
2. С18:1 – олеиновая (9:10),
3. С18:2 – линолевая (9-10,12-13),
4. С18:3 - линоленовая (9-10, 12-13, 15-16),
5. С20:4 - арахидоновая (5-6, 8-9, 12-13, 15-16).
Жирные кислоты, имеющие двойную связь в положении w3, обладают очень выраженным антиатеросклеротическим действием (линоленовая). Особенно много w3-содержащих жирных кислот находится в рыбьем жире и других морепродуктах. В организме человека такие жирные кислоты не синтезируются.
Жирные кислоты, входящие в состав организма человека, имеют общие черты строения:
1. Чётное число атомов углерода.
2. Линейная (неразветвлённая) углеродная цепь.
3. Полиненасыщенные жирные кислоты имеют только изолированные двойные связи (между соседними двойными связями не меньше двух одинарных).
4. Двойные связи имеют только цис-конфигурацию.
ФОРМЫ СУЩЕСТВОВАНИЯ ЛИПИДОВ В ОРГАНИЗМЕ ЧЕЛОВЕКА
1. Жировые включения, которых больше всего в адипоцитах. Это форма существования триглицеридов.
2. Биомембраны. Они не содержат триглицеридов, в них присутствуют фосфолипиды, гликолипиды и холестерин.
3. Липопротеины. Могут включать в себя липиды всех классов.
ЛИПОПРОТЕИНЫ
Липопротеины - это сферические частицы, в которых можно выделить гидрофобную сердцевину, состоящую из триглицеридов (ТРГ) и эфиров холестерина (ЭХС) и амфифильную оболочку, в составе которой – фосфолипиды, гликолипиды и белки.

Белки оболочки называются апобелками. Холестерин обычно занимает промежуточное положение между оболочкой и сердцевиной. Компоненты частицы связаны слабыми типами связей и находятся в состоянии постоянной диффузии – способны перемещаться друг относительно друга.
Основная роль липопротеинов – транспорт липидов, поэтому их можно обнаружить в биологических жидкостях.
У разных липопротеинов наблюдается различное соотношение липидов и белка в составе частицы, поэтому их разделяют по плотности методом ультрацентрифугирования, при этом они не осаждаются, а всплывают (флотируют). Мерой всплывания является константа флотации, обозначаемая Sf (сведберг флотации). В соответствии с этим показателем различают следующие группы липопротеинов:

Все эти липопротеины отличаются по своей функции.
1. Хиломикроны (ХМ) - образуются в клетках кишечника, их функция: перенос экзогенного жира из кишечника в ткани (в основном - в жировую ткань), а также - транспорт экзогенного холестерина из кишечника в печень.
2. Липопротеины Очень Низкой Плотн ости (ЛОНП) - образуются в печени, их роль: транспорт эндогенного жира, синтезированного в печени из углеводов, в жировую ткань.
3. Липопротеины Низкой Плотно сти (ЛНП) - образуются в кровеносном русле из ЛОНП через стадию образования Липопротеинов Промежуточной Плотности (ЛПП). Их роль: транспорт эндогенного холестерина в ткани.
4. Липопротеины Высокой Плотно сти (ЛВП) - образуются в печени, основная роль - транспорт холестерина из тканей в печень, то есть удаление холестерина из тканей, а дальше холестерин выводится с желчью.
РОЛЬ АПОБЕЛКОВ В СОСТАВЕ ЛИПОПРОТЕИНОВ
Белковые компоненты липопротеинов особенно важны. Они называются " аполипопротеинами " и обозначаются латинскими буквами (апоА, апоВ, апоС и так до апоG).
ФУНКЦИИ АПОБЕЛКОВ.
1. Апобелки выполняют функцию эмульгаторов, потому что являются амфифильными веществами.
2. Некоторые из аполипопротеинов являются регуляторами активности ферментов липидного обмена.
3. Могут обладать собственной ферментативной активностью.
4. Могут выступать в качестве лигандов клеточных рецепторов для липопротеинов.
5. Многие апобелки осуществляют транспорт липидов из одного липопротеина в другой.
Качество и чистота жиров характеризуются физическими и химическими константами. Физические константы: плотность, температура плавления и застывания, коэффициент рефракции (для жидких жиров); химические константы: число омыления, Рейхарда -Мейсля, йодное, кислотное. Число омыления определяется количеством миллиграммов КОН, израсходованного на нейтрализацию жирных кислот, которые образуются при омылении 1 г жира.
Число Рейхарда-Мейсля характеризуется количеством 0,1 н раствора КОН, затраченного на нейтрализацию летучих жирных кислот (масляной, капроновой и каприловой), образованных при гидролизе 5 г жира и отогнанных с водным паром.
Йодное число характеризует наличие в составе жара ненасыщенных жирных кислот и определяется количеством граммов йода, способным присоединиться к 100 г жира.
Кислотное число определяется числом миллиграммов КОН, затраченного на нейтрализацию свободных жирных кислот, которые содержатся в 1 г жира.
Задание: Написать уравнения реакции образования молекул простых и сложных липидов.
Тема 3 –Углеводы
Углеводы входят в состав клеток и тканей всех организмов, причем количественно и качественно они особенно широко представлены у растений, составляют основную часть их тканей (в листьях, стеблях, корнях, клубнях, семенах, плодах — 90% веса на сухое вещество). Все углеводы являются теми продуктами, которые образуются первично в зеленом растении из углекислого газа и воды за счет энергии солнечного света и дают начало другим органическим веществам живых организмов. Функции углеводов в организме: энергетическая, пластическая, защитная, опорная, регуляторная, определяют антигенную специфичность, обуславливают различие групп крови.
Важнейшие производные моносахаридов: Аминосахара, фосфорные эфиры углеводов, гликозиды, уроновые кислоты
Важнейшие представители углеводов:
Моносахариды – пентозы: рибоза, дезоксирибоза, гексозы: глюкоза, галактоза, фруктоза, манноза.Олигосахариды – наиболее широко распространены дисахариды. Они делятся две группы: восстанавливающие и невосстанавливающие.
К восстанавливающим дисахаридам относится мальтоза (солодовый сахар), целлобиоза и лактоза (молочный сахар), у которых гликозидная связь образуется также как у мальтозы. К невосстанавливающим дисахаридам относятся сахароза (свекловичный или тростниковый сахар) и трегалоза (грибной сахар). Трегалоза встречается в грибах, рожках спорыньи, водорослях и в некоторых высших растениях, состоит из двух молекул α –Д-глюкозы, соединенных 1 → 1 гликозидной связью, в образовании связи участвуют оба гликозидных гидроксила. Сахароза содержится в сахарном тростнике, сахарной свекле (до 28% от сухого вещества), соках.
Раффиноза (С18Н32О16) — трисахарид, встречается в семенах хлопчатника, сахарной свеклы и других растениях.
Все моносахариды и олигосахариды обладают сладким вкусом, однако, сладость их неодинакова. Для характеристики степени сладости различных углеводов обычно сладость сахарозы принимают за 100, сравнительно сладость фруктозы составляет 173, инвертного сахара —130, глюкозы — 74, рамнозы —32, мальтозы — 32, лактозы — 40, ксилозы —16.
Высокомолекулярные полисахариды построены из большого числа остатков одного моносахарида глюкозы, фруктозы, маннозы, ксилозы и др. Они являются запасными питательными веществами (крахмал, гликоген, инулин), служат структурной основой тканей (клетчатка), выполняют защитные функции (хитин). Для гомосахаридов характерны высокая молекулярная масса и сложные физико-химические свойства.
Важнейшие из гомополисахаридов (состоят из одинаковых струк-турных единиц) - это крахмал, целлюлоза (клетчатка), гликоген.
Гетерополисахариды. Это сложные углеводы, молекулы которых построены из остатков различных моносахаридов, их производных и других соединений. Гиалуроновая кисло та. Это гетерополисахарид, построенный из остатков молекул глюкуроновой и уксусной кислот, глюкозамина. Хондроитинсерная кислота — составная часть хрящей (до 40% сухой массы), костей, основного вещества соединительной ткани, сердечных клапанов, сухожилий, хрящей. Гепарин. В организме вырабатывается тучными клетками и частично базофилами.
Задание: Написать примеры различных изомеров углеводов, уравнения реакций образования дисахаридов, полисахаридов.
Тема 4 – Белки
БЕЛКИ или ПРОТЕИНЫ - это высокомолекулярные азотсодержащие органические вещества, линейные гетерополимеры, структурным компонентом которых являются аминокислоты, связанные пептидными связями.
Не нашли, что искали? Воспользуйтесь поиском: