
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Строение и свойства. Натрия тиосульфат - соль, образованная катионом натрия и анионом тиосерной кислоты:
Натрия тиосульфат - соль, образованная катионом натрия и анионом тиосерной кислоты:
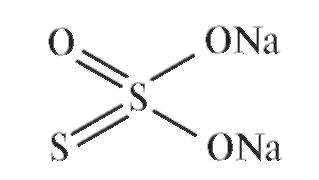
Соль образует пентагидрат: Na2S2O3 • 5H2O. Сера в тиосульфатионе находится в разной степени окисления (+4 и 0), поэтому окислительно-восстановительные превращения тиосульфат-иона весьма разнообразны и широко используются в фармацевтическом анализе.
В водном растворе натрия тиосульфат гидролизуется по аниону:
S2O2- + H2O ↔ HS2O3- + OH-. На воздухе субстанция разлагается:
2Na2S2O3 + O2 (воздух) = 2Na2SO4 + 2S.
Получение
Впервые натрия тиосульфат был получен в 1799 г. способом, который применяется и в настоящее время, - кипячением раствора сульфита натрия с серой:
Na2SO3 + S - Na2S2O3
Окончание реакции устанавливают по отрицательной пробе на сульфит-ионы с раствором хлорида кальция: не образуется осадок СаSО3. Затем избыток серы отфильтровывают и раствор выпаривают. При этом образуется кристаллогидрат
Na2S2O3 • 5H2O.
Исходными веществами для получения натрия тиосульфата могут служить сульфиды (Na2S, CaS) и полисульфиды (CaS2), которые участвуют в окислительно-восстановительном процессе с диоксидом серы или кислородом:
2Na2S + 3SO2 → 2Na2S2O3 + S;
2CaS2 + 3O2 → 2CaS2O3.
Не нашли, что искали? Воспользуйтесь поиском: