
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Методичні вказівки.
Маса кожного хімічного елемента у складі речовини може бути виражена в частках від одиниці або у відсотках. Отже, за формулою можна знайти масову частку елемента в речовині.
Масова частка елемента - це відношення його маси до маси речовини, до складу якої він входить (позначається w, читається дубль-ве):
w = 
Розглянемо приклад.
Треба визначити масову частку заліза в оксиді заліза (ІІІ), який входить до складу руди.
М (Fe2O3) = 56 × 2 + 16 × 3 = 160 г/моль
w (Fe) =  = 0,7 або 70%.
= 0,7 або 70%.
Отже, у складі оксиду заліза (ІІІ) Fe2O3 масова частка заліза становить 0,7 або 70%.
За законом Авогадро однакові об'єми газів (н.у.) містять однакове число молекул. Звідси виходить, що маси однакових об'ємів двох газів повинні відноситись одна до одної, як їхні молекулярні маси або як чисельно такі самі молярні маси:

де m1, m2 - маси першого і другого газів;
М1, М2 - молярні (або молекулярні) маси першого і другого газів.
Відношення маси певного газу до маси такого самого об'єму іншого газу, взятих за однакових температур і тиску, називають відносною густиною першого газу за другим (позначається D).
D = 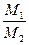
Задача 1 Масова частка карбону в молекулі вуглеводню дорівнює 85,7%. Густина речовини за повітрям 1,45. Визначіть молекулярну формулу речовини.
І спосіб розв'язування:
1. Приймемо масу речовини за 100 г:
m (C) = 85,7 г. m (H) = 14,3 г.
2. Знайдемо кількість речовини карбону і гідрогену, які містяться в цій масі:
М =  ; n =
; n =  ; n (C): n (H) =
; n (C): n (H) =  = 7,14: 14,3 = 1: 2;
= 7,14: 14,3 = 1: 2;
CH2 - емпірична формула.
3. Знайдемо молярну масу вуглеводню:
Dпов =  , М (СхНу) = Dпов × 29 = 42 г/моль.
, М (СхНу) = Dпов × 29 = 42 г/моль.
4. Визначимо молекулярну формулу речовини, порівнюючи її з емпіричною формулою:
(СН2)n = 42; 14n = 42; n = 3
(СН2)3 ® C3H6
Відповідь: молекулярна формула речовини - C3H6
ІІ спосіб розв'язування:
1. Знайдемо молярну масу вуглеводню:
М (СхНу) = 1,45 × 29 = 42 г/моль.
2. Розрахуємо, яка маса карбону міститься в молекулі:
m (C) = 42 × 0,857 = 36; n (C) = 36 /12 = 3 атоми.
3. Розрахуємо, яка маса гідрогену міститься в молекулі:
m (H) = 42 × 0,143 = 6, або 42 - 36 = 6, n (H) = 6 атомів.
Відповідь: молекулярна формула речовини - C3H6
Задача 2. При згорянні 4,2 г речовини утворюється 13,2 г оксиду карбону (ІV) і 5,4 г води. Густина пари цієї речовини за повітрям (н.у.) становить 2,9. Виведіть молекулярну формулу речовини.
І спосіб розв'язування
1. За формулою Dпов =  , визначимо молярну масу невідомої речовини:
, визначимо молярну масу невідомої речовини:
М = Dпов × 29; М = 2,9 × 29 = 84 г/моль.
2. Розрахуємо кількість речовин газу, що прореагувала, а також кількість речовини оксиду карбону (ІV) та води, що утворилися в результаті реакції:
n (СхНу) =  = 0,05 моль,
= 0,05 моль,
n (СО2) =  = 0,3 моль, n (Н2О) =
= 0,3 моль, n (Н2О) =  = 0,3 моль.
= 0,3 моль.
3. На підставі рівняння реакції горіння невідомої речовини (СхНу) та відношення кількості речовини знаходимо молекулярну формулу речовини:
0,05 0,3 моль 0,3 моль
(СхНу) + О2 ® СО2 + Н2О
1 моль 6 моль 6 моль
(СхНу) + О2 ® 6СО2 + 6Н2О
х = 6; у = 12; С6Н12 - найпростіша формула.
4. Визначимо, чи був у молекулі оксиген:
М(С6Н12) = 84 г/моль - оксигену немає.
Відповідь: молекулярна формула речовини - C6H12
ІІ спосіб розв'язання
1. Розрахуємо кількість карбону і гідрогену, що містяться відповідно у 13,2 г оксиду карбону (ІV) і 5,4 г води:
18 г Н2О - міститься 2 г Н, 44 г СО2 - міститься 12 г С,
5,4 г Н2О - міститься у г Н, 13,2 г СО2 - міститься х г С,
у =  = 0,6 г х =
= 0,6 г х =  = 3,6 г.
= 3,6 г.
2. Перевіримо наявність оксигену:
m (O) = 4,2 - (3,6 + 0,6) = 0 - оксигену немає.
3. Найпростіша формула має вигляд СхНу:
n (C): n (H) =  : 0,6 = 0,3: 0,6 = 1: 2;
: 0,6 = 0,3: 0,6 = 1: 2;
СН2 - емпірична формула.
4. Визначимо молекулярну формулу речовини, порівнюючи її з емпіричною формулою:
(СН2) × n = 84; 14n = 84; n = 6
(СН2)6 ® С6Н12.
Відповідь: молекулярна формула С6Н12.
Задача 3. При спалюванні 5,6 л газу добуто 5,6 л оксиду карбону (ІV) і 4,5 г води. Густина газу за воднем становить 15 (н.у). Знайдіть молекулярну формулу речовини.
Розв’язання.
1. Розрахуемо молярну масу газу:
М = D  × М (Н2) = 15 × 2 = 30 г/моль.
× М (Н2) = 15 × 2 = 30 г/моль.
2. Визначимо кількість речовини газу, що прореагувала, а також кількість речовини оксиду карбону (ІV) та води, що утворилися в результаті реакції:
n(газу): n (СО2): n (Н2О) =  :
:  :
:  = 0,25: 0,25: 0,25 = 1: 1: 1.
= 0,25: 0,25: 0,25 = 1: 1: 1.
3. Знаходимо найпростішу молекулярну формулу речовини:
1 моль 1 моль 1 моль
(СхНуОz) + О2 ® СО2 + Н2О;
х = 1, у = 2;
4. Визначимо кількість атомів оксигену:
М (СН2) = 14,
Dm (О) = 30 - 14 = 16 - речовина містить 1 атом оксигену.
Відповідь: молекулярна формула речовини - СН2О.
Завдання для самостійної роботи.
1. Деякий алкан має відносну густину парів за повітрям 3,931. Визначте емпіричну формулу цього алкану та назвіть його.
2. Відносна густина парів деякого циклоалкану за воднем дорівнює 42. Молекула циклоалкану не має бокових розгалуджень від головного вуглецевого ланцюга. Визначте формулу циклоалкану та назвіть його.
3. У вуглеводні масова частка вуглецю дорівнює 84%. Відносна густина парів вуглеводнів за повітрям дорівнює 3,45. Визначте емпіричну формулу вуглеводню.
4. Визначте формулу циклоалкану, на спалювання якого витрачається об'єм кисню у 9 раз більше, чим об'єм парів циклоалкану. Назвіть цей циклоалкан, якщо відомо, що його вуглецевий скелет має нерозгалуджену будову.
ЛІТЕРАТУРА.
1. С. А. Сєргєєв "Хімія. Теми шкільного курсу", М."Акваріум" 1997р.
2. М. В. Горский "Обучение основам общей химии", М."Просвещение" 1991г.
3. Ф. Г. Фельдман, Г. Е. Рудзите "Химия 9 кл.", М."Просвещение"1990г.
4. Д. П. Яригін, Е. А. Шишкін "Методика розв'язання задач з хімії", М."Просвещение" 1989р.
5. І. Г. Хомченко "Загальна хімія" К. "Вища школа"1993р.
6. Р. І. Агамова "Хімія - 10", робочий зошит учня К. "Абрис"1998р.
7. І. Г. Хомченко "Общая химия" Сборник задач и упражнений: М.:, "Издательство Новая Волна", 1999.
8. Н. М. Буринська "Хімія"Проб. навч. посібник для 8 кл. серед загальноосвіт. шк. - Ірпінь: Перун, 1994.
Не нашли, что искали? Воспользуйтесь поиском: