
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Виды химической связи
Ковалентная связь – это химическая связь, осуществляемая за счет обобществления электронных пар. Теорию ковалентной связи предложил в 1916 г. американский ученый Гилберт Льюис. За счет ковалентной связи образуется большинство молекул, молекулярных ионов, свободных радикалов и атомных кристаллических решеток. Ковалентная связь характеризуется длиной (расстояние между атомами), направленностью (определенная пространственная ориентация электронных облаков при образовании химической связи), насыщаемостью (способность атомов образовывать определенное число ковалентных связей), энергией (количество энергии, которое необходимо затратить для разрыва химической связи).
Ковалентная связь может быть неполярной и полярной. Неполярная ковалентная связь возникает между атомами с одинаковой электроотрицательностью (ЭО) (H2, O2, N2 и т. д.). В этом случае центр общей электронной плотности находится на одинаковом расстоянии от ядер обоих атомов. По числу общих электронных пар (т.е. по кратности) различают одинарные, двойные и тройные ковалентные связи. Если между двумя атомами образуется только одна общая электронная пара, то такая ковалентная связь называется одинарной. Если между двумя атомами возникают две или три общие электронные пары, образуются кратные связи – двойные и тройные. Двойная связь состоит из одной σ-связи и одной π-связи. Тройная связь состоит из одной σ-связи и двух π-связей.
Ковалентные связи, при образовании которых область перекрывания электронных облаков находится на линии, соединяющей ядра атомов, называются σ - связями. Ковалентные связи, при образовании которых область перекрывания электронных облаков находится по обе стороны от линии, соединяющей ядра атомов, называются π-связями.
В образовании σ-связей могут участвовать s- и s-электроны (Н2), s-и p-электроны (HCl), р- и р-электроны (Cl2). Кроме того, σ-связи могут образовываться за счет перекрывания «чистых» и гибридных орбиталей. В образовании π-связей могут участвовать только р- и d-электроны.
Ниже линиями показаны химические связи в молекулах водорода, кислорода и азота:
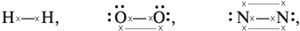
где пары точек (:) – спаренные электроны; «крестики» (х) – неспаренные электроны.
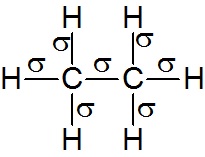

а) б)
Рис. 1.3.2. σ- и π-связи в молекулах этана С2Н6 (а) и этилена С2Н4 (б).
Если ковалентная связь образуется между атомами с различной ЭО, то центр общей электронной плотности смещен в сторону атома с большей ЭО. В этом случае имеет место ковалентная полярная связь. Двухатомная молекула, связанная ковалентной полярной связью, представляет собой диполь – электронейтральную систему, в которой центры положительного и отрицательного зарядов находятся на определенном расстоянии друг от друга.
Графический вид химических связей в молекулах хлороводорода и воды следующий:
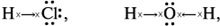
где стрелками показано смещение общей электронной плотности.
Полярная и неполярная ковалентные связи образованы по обменному механизму. Кроме того, существует донорно-акцепторный механизм образования ковалентной связи. В этом случае один атом (донор) предоставляет неподеленную пару электронов, которая становится общей электронной парой между ним и другим атомом (акцептором). Акцептор при образовании такой связи предоставляет свободную электронную орбиталь.
Донорно-акцепторный механизм образования ковалентной связи проиллюстрирован на примере образования иона аммония:

Таким образом, в ионе аммония все четыре связи являются ковалентными. Три из них образованы по обменному механизму, одна – по донорно-акцепторному. Все четыре связи равноценны, что обусловлено sp3-гибридизацией орбиталей атома азота. Валентность азота в ионе аммония равна IV, т.к. он образует четыре связи. Следовательно, если элемент образует связи и по обменному, и по донорно-акцепторному механизмам, то его валентность больше числа неспаренных электронов и определяется общим числом орбиталей на внешнем электронном слое. Для азота, в частности, высшая валентность равна четырем.
Ионная связь – химическая связь между ионами, осуществляемая за счет сил электростатического притяжения. Ионная связь образуется между атомами, имеющими большую разность ЭО (> 1,7); другими словами, это связь между типичными металлами и типичными неметаллами. Теория ионной связи была предложена в 1916 г. немецким ученым Вальтером Косселем. Отдавая свои электроны, атомы металлов превращаются в положительно заряженные ионы – катионы; атомы неметаллов, принимая электроны, превращаются в отрицательно заряженные ионы – анионы. Между образовавшимися ионами возникает электростатическое притяжение, которое называется ионной связью. Ионная связь характеризуется ненаправленностью и ненасыщаемостью; для ионных соединений понятие «молекула» не имеет смысла. В кристаллической решетке ионных соединений вокруг каждого иона располагается определенное число ионов с противоположным зарядом. Для соединений NaCl и FeS характерна кубическая кристаллическая решетка.
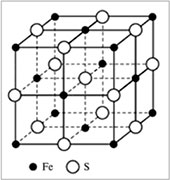
|
Рис. 1.3.3. Ионная кристаллическая решетка сульфида железа FeS
Ниже показано образование ионной связи на примере хлорида натрия:
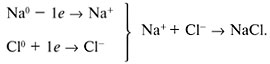
Ионная связь является крайним случаем полярной ковалентной связи. Резкой границы между ними не существует, тип связи между атомами определяется по разнице электроотрицательности элементов.
При образовании простых веществ – металлов – атомы достаточно легко отдают электроны внешнего электронного уровня. Таким образом, в кристаллах металлов часть их атомов находится в ионизированном состоянии. В узлах кристаллической решетки находятся положительно заряженные ионы и атомы металлов, а между ними – электроны, которые могут свободно перемещаться по всей кристаллической решетке. Эти электроны становятся общими для всех атомов и ионов металла и называются «электронным газом». Связь между всеми положительно заряженными ионами металлов и свободными электронами в кристаллической решетке металлов называется металлической связью.
Наличием металлической связи обусловлены физические свойства металлов и сплавов: твердость, электропроводность, теплопроводность, ковкость, пластичность, металлический блеск. Свободные электроны могут переносить теплоту и электричество, поэтому они являются причиной главных физических свойств, отличающих металлы от неметаллов, – высокой электро- и теплопроводности.
Водородная связь возникает между молекулами, в состав которых входит водород и атомы с высокой ЭО (кислород, фтор, азот). Ковалентные связи H–O, H–F, H–N являются сильно полярными, за счет чего на атоме водорода скапливается избыточный положительный заряд, а на противоположных полюсах – избыточный отрицательный заряд. Между разноименно заряженными полюсами возникают силы электростатического притяжения – водородные связи. Водородные связи могут быть как межмолекулярными, так и внутримолекулярными. Энергия водородной связи примерно в десять раз меньше энергии обычной ковалентной связи, но тем не менее водородные связи играют большую роль во многих физико-химических и биологических процессах. В частности, молекулы ДНК представляют собой двойные спирали, в которых две цепи нуклеотидов связаны между собой водородными связями.
Межмолекулярные водородные связи между молекулами воды и фтороводорода можно изобразить (точками) следующим образом:

Вещества с водородной связью имеют молекулярные кристаллические решетки. Наличие водородной связи приводит к образованию ассоциатов молекул и, как следствие, к повышению температур плавления и кипения.
Кроме перечисленных основных видов химической связи существуют также универсальные силы взаимодействия между любыми молекулами, которые не приводят к разрыву или образованию новых химических связей. Эти взаимодействия называются вандерваальсовыми силами. Они обусловливают притяжение молекул данного вещества (или различных веществ) друг к другу в жидком и твердом агрегатном состояниях.
Вещества, состоящие из молекул, имеют молекулярное строение. К таким веществам относятся все газы, жидкости, а также твердые вещества с молекулярной кристаллической решеткой, например йод. Твердые вещества с атомной, ионной или металлической решеткой имеют немолекулярное строение, в них нет молекул.
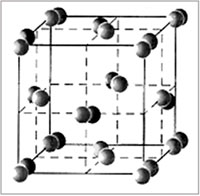
|
Рис.1.3.4. Молекулярная кристаллическая решетка йода I2
Не нашли, что искали? Воспользуйтесь поиском: