
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Химические свойства. Соли тесно связаны со всеми остальными классами неорганических соединений и могут быть получены практически из любого класса.
Получение солей
Соли тесно связаны со всеми остальными классами неорганических соединений и могут быть получены практически из любого класса.
1. Взаимодействие основных, кислотных и амфотерных оксидов друг с другом:
BaO + SiO2 = BaSiO3
P2O5 + Al2O3 = 2AlPO4
2. Взаимодействие оксидов с гидроксидами (с кислотами и основаниями):
ZnO + H2SO4 = ZnSO4 + H2O
CO2 + 2KOH = K2CO3 + H2O
3. Взаимодействие оснований со средними и кислыми солями:
CuSO4 + 2KOH = Cu(OH)2↓ + K2SO4
Cu(OH)2 + 2NaHSO4 = CuSO4 + Na2SO4 +2H2O
4. Соли бескислородных кислот, кроме того, могут быть получены при непосредственном взаимодействии металлов и неметаллов:
2Mg + Cl2 = MgCl2
18. Алюминий — элемент 13-й группы периодической таблицы химических элементов, третьего периода, с атомным номером 13. Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости химический элемент в земной коре.
Простое вещество алюминий — лёгкий парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия.
Получение
Алюминий образует прочную химическую связь с кислородом. Современный метод получения, процесс Холла—Эру был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых анодных электродов. Такой метод получения требует очень больших затрат электроэнергии, и поэтому получил промышленное применение только в XX веке.
Лабораторный способ получения алюминия предложил Фридрих Вёлер в 1827 году восстановлением металлическим калием безводного хлорида алюминия (реакция протекает при нагревании без доступа воздуха):
AlCl3+3K=3KCl+Al
В природе
По распространённости в земной коре Земли занимает 1-е место среди металлов и 3-е место среди элементов, уступая только кислороду и кремнию. Массовая концентрация алюминия в земной коре, по данным различных исследователей, оценивается от 7,45 до 8,14 %.
Природные соединения алюминия
В природе алюминий, в связи с высокой химической активностью, встречается почти исключительно в виде соединений. Некоторые из природных минералов алюминия:
Бокситы, берилл (изумруд, аквамарин), хризоберилл (александрит)
Химические свойства
При нормальных условиях алюминий покрыт тонкой и прочной оксидной плёнкой и потому не реагирует с классическими окислителями: с H2O, O2, HNO3 (без нагревания). Легко реагирует с простыми веществами:
· с кислородом, образуя оксид алюминия:
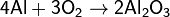
· с серой, образуя сульфид алюминия:

Со сложными веществами:
со щелочами:


Легко растворяется в соляной и разбавленной серной кислотах:


Применение
Широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость, высокая теплопроводность. Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому для упрочнения его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий).
| <== предыдущая лекция | | | следующая лекция ==> |
| V Осмотические диуретики | | | организационная культура в концепции кадровой политики предприятия |
Не нашли, что искали? Воспользуйтесь поиском: