
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Вода как сырье на КЭС
Содержание
Вопросы…………………………………………………………………………...3
2. Опишите воду как технологическое сырье на КЭС…………………..……………………3
7. Охарактеризуйте показатели качества воды…………………………..……………………6
29. Приведите конструкцию и опишите эксплуатацию мех.фильтров…………………..…..9
37. Опишите H-катионирование воды, его назначение,
приведите реакции, протекающие при работе и регенерации………………….....…………13
46. В чем заключается важность применения
трёхступенчатой схемы для обессоливания и обескремнивания
воды? Дайте схему и подробное описание процессов,
проходящих в каждой установке схемы ……………………………………………...……….16
48. Перечислите мембраны для обратного осмоса и приведите
их характеристики…………………..…….…………………………………………..…………19
Список используемой литературы………………………....…………………….25
Вода как сырье на КЭС
Вода, получаемая из источников водоснабжения, используется на тепловых электростанциях: а) в качестве технологического сырья для получения пара в парогенераторах, испарителях и паропреобразователях;
б) для конденсации отработавшего пара в конденсаторах паровых турбин и других производственных теплообменных аппаратах;
в) для охлаждения продувочной воды и подшипников дымососов;
г) для охлаждения воздуха, газов и масла в охладительных установках;
д) в качестве рабочего теплоносителя в теплофикационных отопительных сетях и сетях горячего водоснабжения.

На рис. 0-1 изображены типичные принципиальные схемы обращения воды в рабочем цикле ТЭС с конденсационной турбиной (КЭС) и промышленной теплоэлектроцентрали с теплофикационной турбиной (ТЭЦ).
Исходная природная вода, получаемая из источников водоснабжения и направляемая в качестве технологического сырья па водоподготовительную установку либо используемая для каких-либо других целей в процессе получения электрической энергии.
Добавочная вода, используемая для восполнения потерь пара и конденсата в пароводяном цикле электростанции; в качестве добавочной воды к питательной воде парогенераторов могут быть использованы хи-
мически обработанная вода или дистиллят (конденсат вторичного пара испарителей).
Конденсат турбин, содержащий незначительное количество растворенных веществ, является наиболее ценной составляющей питательной воды; поэтому следует всемерно стремиться к минимальным потерям его иа ТЭС.
Обратный конденсат внешних потребителей пара используется, как составная часть питательной воды после его предварительной очистки от посторонних примесей.
Питательная вода, подаваемая насосами в парогенераторы для восполнения убыли испарившейся котловой воды и представляющая собой обычно смесь конденсата турбин, регенеративных н теплофикационных подогревателей, обратного конденсата внешних потребителей и добавочной воды.
Котловая вода, испаряемая в парогенераторах; воду, испаряемую в испарителях и паропреобразователях, называют концентратом.
Продувочная вода или концентрат, выпускаемые из парогенераторов, испарителей и паропреобразователей с целью поддержания в них иа заданном уровне концентрации примесей, непрерывно поступающих в цикл ТЭС.
Охлаждающая или циркуляционная вода, используемая в конденсаторах паровых турбин для конденсации отработавшего пара.
Подпиточная вода, подаваемая в теплофикационную сеть для восполнения потерь циркулирующей в ней сетевой воды.
В рабочем цикле ТЭС имеют место внутристанционные потери пара и конденсата, основными источниками которых являются:
а) парогенераторы, где теряется пар, расходуемый на привод вспомогательных механизмов, иа обдувку наружных поверхностей нагрева от золы и шлака, на грануляцию шлаков в топке, на распыливание в форсунках жидкого топлива, при периодическом открытии предохранительных клапанов, при продувке пароперегревателей во время растопки парогенераторов и с непрерывной и периодической продувкой парогенераторов с многократной циркуляцией;
б) турбоагрегаты, где имеют место непрерывные потери пара через лабиринтовые уплотнения и в воздушных насосах, отсасывающих из конденсаторов вместе с воздухом и некоторое количество пара;
в) конденсатные и питательные баки, где происходит потеря воды через перелив и испарение горячего конденсата;
г) питательные насосы, где происходят утечки воды через неплотности сальниковых уплотнении;
д) трубопроводы, где происходят утечки воды через неплотности фланцевых соединении, запорной и регулирующей арматуры;
е) термические деаэраторы, где происходит потеря пара с выпаром;
ж) турбонасосы — с выхлопом пара;
з) пробоотборочиые точки — с конденсатом и водой.
Внутристанционные потери пара и конденсата могут быть значительно уменьшены путем установки дренажных и сливных баков для сбора конденсата, путем правильного выбора габаритов конденсатных баков, путем применения сварки трубопроводов и обеспечения высокой плотности фланцевых соединений, ликвидации пареня предохранительных клапанов, отказа от использования паровых форсунок, паровых приводов и паровых обдувочных аппаратов, а также путем применения теплообменных аппаратов с приспособлениями для конденсирования и улавливания отработавшего пара. При соблюдении этих условий внутристанцнонные потери пара и воды составляют незначительную величину, не превышающую 0,5—1,0% общей производительности парогенератора. Следовательно, на КЭС основной составляющей питательной воды является конденсат турбин, что видно из водного баланса КЭС:
Dп.в= Dк.т+ Dд.пD (0-1)
где Dп.в— часовой расход питательной воды, т/ч; Dк.т— часовой расход конденсата турбин, т/ч; Dд.в — часовой расход добавочной воды, т/ч, причем величина Dк.т почти а 100 раз больше, чем Dд.в
Аналогичное положение имеет место и на чисто отопительных ТЭЦ.
Солесодержание питательной воды ап.в на КЭС, определяемое из солевого баланса, равно:

 +
+ 
 (0-2)
(0-2)
где ак.т и ад.в — солесодержание соответственно конденсата турбин и добавочной воды, г/т, т. е. определяется в основной солесодержаннем конденсата турбин.
Показатели качества воды
Важнейшими показателями качества воды, определяющими пригодность ее для использования на тепловых электростанциях, являются содержание взвешенных веществ, сухой остаток, общая жесткость и ее составляющие, общая щелочность и ее составляющие, окисляемость, концентрация водородных ионов и содержание коррозионноагрессивных газов О2 и CO2. Для получения более полной качественной характеристики воды дополнительно определяют содержание в ней катионов кальция, магния и натрия, анионов хлора, карбонатных, сульфатных и силикатных, а также соединений железа и алюминия, выраженных в виде суммы их «полуторных» окислов
Содержание взвешенных веществ выражается в мг/кг.
Сухим остатком воды называется суммарное количество растворенных в ней нелетучих молекулярнодисперсных и коллоидных веществ минерального и органического происхождения, выраженное в миллиграммах на килограмм. Сухой остаток определяется путем выпаривания предварительно профильтрованной пробы воды и последующего высушивания остатка при температуре 110°С до постоянного веса. В сухой остаток не входят взвешенные вещества, растворенные в воде газы и летучие вещества (например, НСО3- NH3 и др.). Если сухой остаток прокаливать при температуре 800 °С, вес его уменьшится в получится прокаленный остаток. Уменьшение веса получится вследствие сгорания органических веществ, разложения карбонатов и удаления остатков влаги.
Минеральным остатком называется сумма концентраций всех содержащихся в воде катионов, анионов и полуторных окислов
Аl2O3 + Fе2О3 с учетом превращения при выпаривании воды
НСО3- и ОН- в  - и H2SiO3 в SiO2
- и H2SiO3 в SiO2
MO = CCa2++CMg2++CNa++  -+C
-+C 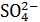 +CCl-+CNO3-+CNO2-+CSiO3+
+CCl-+CNO3-+CNO2-+CSiO3+
+CAl2O3+CFe2O3. мг/кг (1 -9)
Жесткость воды является одним из наиболее важных показателей качества воды, используемой на тепловых электростанциях. Общая жесткость воды Жо равна сумме концентраций в ней катионов кальция (кальциевая жесткость ЖCa) и магния (магниевая жесткость ЖMg) и выражается в миллиграмм-эквивалентах на килограмм (мг-экв/кг) или грамм-эквивалентах на тонну
(г-экв/т) при измерении больших жесткостей и в микрограмм-эквивалентах на килограмм (мкг-экв/кг) при измерении малых жесткостей.
Для пересчета выраженных в мг/кг концентраций кальция и магния в мг-экв/кг их делят иа эквивалентные веса этих катионов,
т. е.

Где C  и C
и C  — концентрация в воде катионов кальция и магния, мг/кг; 20,04 и 12,16—эквивалентные веса кальция и магния. Общая жесткость воды подразделяется на карбонатную и некарбонатную. Карбонатная жесткость воды Жк в основном обуславливается присутствием в воде бикарбонатов кальция и магния Са(НСO3)2 и Мg(НСО3)2 так как СаСО3 и MgCO3 малорастворимы в воде. В том случае, когда концентрация ионов НСО3- выраженная в мг-экв/кг, меньше обшей жесткости воды, величина карбонатной жесткости определяется концентрацией НСО3-
— концентрация в воде катионов кальция и магния, мг/кг; 20,04 и 12,16—эквивалентные веса кальция и магния. Общая жесткость воды подразделяется на карбонатную и некарбонатную. Карбонатная жесткость воды Жк в основном обуславливается присутствием в воде бикарбонатов кальция и магния Са(НСO3)2 и Мg(НСО3)2 так как СаСО3 и MgCO3 малорастворимы в воде. В том случае, когда концентрация ионов НСО3- выраженная в мг-экв/кг, меньше обшей жесткости воды, величина карбонатной жесткости определяется концентрацией НСО3-
 |
где Жк —карбонатная жесткость, мг-экв/кг; С  - концентрация бикарбонатных ионов, мг/кг 61,02 —эквивалентный вес
- концентрация бикарбонатных ионов, мг/кг 61,02 —эквивалентный вес 
Некарбонатная жесткость воды Жнк обусловливается наличием в воде хлоридов, сульфатов и других некарбонатных солей кальция и магния: СаС12, MgCl2, CaSO4 MgSO4 CaSiO3. MgSiO2 и др.
Таким образом, общая жесткость воды равна сумме кальциевой и магниевой жесткостей, с одной стороны, и сумме карбонатной и некарбонатной жесткостей с другой.
По величине общей жесткости природных вод установлена следующая классификация:
Ж0<1,5 мг-экв/кг— жесткость малая;
Ж0 =1,5/3,0 мг-экв/кг — средняя;
Ж0=3,0/6,0 мг-экв/кг — повышенная
Ж0= 6,0/ 12,0 мг-экв/кг — высокая;
Ж0 >12 мг-экв/кг — очень высокая.
Общей щелочностью воды Щ0 называется выраженная в мг-экв/кг суммарная концентрация содержащихся в воде анионов ОН-, НСО3-, С 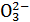 , Р
, Р  , HSiO3- Si
, HSiO3- Si  и некоторых солей слабых органических кислот (гуматов).
и некоторых солей слабых органических кислот (гуматов).
Так как все перечисленные вещества реагируют с кислотой, то общая щелочность воды определяется количеством кислоты, затраченной на титрование с индикатором метилоранжем. В природных водах щелочность обусловливается обычно присутствием бикарбонатов, гидратов и гуматов. В зависимости от анионов, обусловливающих щелочность, различают: а) гидратиую щелочность Щг, обусловленную концентрацией в воде гидроксильных ионов ОН-; б) карбонатную щелочность Щк, обусловленную концентрацией в воде карбонатных ионов С 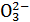 ; в) бикарбонатную щелочность Щб, обусловленную концентрацией бикарбонатных ионов НСОз-.
; в) бикарбонатную щелочность Щб, обусловленную концентрацией бикарбонатных ионов НСОз-.
В простейшем случае при отсутствии в воде фосфатного и других анионов слабых кислот, кроме карбонатного, гидроксильного или бикарбонатиого, общая щелочность воды может состоять только из гидратиой щелочности; из суммы гидратной н карбонатной щелочностей; только из карбонатной щелочности; из суммы карбонатной и бикарбонатной щелочностей; только из бикарбонатной щелочности.
Карбонатную жесткость воды часто называют щелочностью, поскольку карбонатная жесткость обусловливается наличием в воде бикарбонатов и карбонатов кальция и магния, т. е. соединений, дающих в растворе анионы НСОз- и С 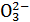 . В том случае, когда концентрация этих ионов в воде, выраженная в мг-экв/кг. больше общей жесткости воды, разность между
. В том случае, когда концентрация этих ионов в воде, выраженная в мг-экв/кг. больше общей жесткости воды, разность между
(СНСОз- + CС  )и Ж0 определяет натриевую щелочность воды, т. е. суммарную концентрацию в воде бикарбоната и карбоната натрия.
)и Ж0 определяет натриевую щелочность воды, т. е. суммарную концентрацию в воде бикарбоната и карбоната натрия.
Стабильность воды. Стабильной называется вода, не способная к выделению отложений карбоната кальция и не являющаяся агрессивной, что обусловливается состоянием равновесия между растворенной в воде свободной углекислотой и ионами кальция. Степень отклонения от стабильности воды характеризуется ее нестабильностью DЩ, равной разности между щелочностями воды до и после фильтрования через слой мраморной крошки.
Органические вещества. Непосредственное определение концентрации органических веществ в воде практически невозможно, поэтому содержание их принято характеризовать косвенным путем, определяя окисляемость воды с применением в качестве окислителя марганцовокислого калия КМп04 (перманганата калия) в кислой среде.
Не нашли, что искали? Воспользуйтесь поиском: